Introduction
Depuis 2011, 1.473 cas de cancers du sein ont été pris en charge au CHR de Verviers.
Parmi ceux-ci, deux patientes ont souffert d’un angiosarcome suite à la radiothérapie adjuvante à la chirurgie.
L’angiosarcome post-radique du sein est une tumeur endothéliale qui survient chez 0.1% des patientes ayant eu une irradiation mammaire adjuvante. (4)
Ce type de tumeur correspond à <0.05% des cancers invasifs mammaires. L’angiosarcome primaire, dont aucune cause n’a été identifiée, correspond à < 0.04% des néoplasies mammaires. (7)
Le premier cas d’angiosarcome post-radique du sein fut décrit en 1981 par J.Hamels et al. au niveau de la cicatrice de mastectomie de leur patiente. (6)
Ce type de cancer survient en moyenne 8 ans après l’irradiation causale, selon une étude de large cohorte menée aux Pays-Bas publiée en 2019. (5)
On peut distinguer les deux types d’angiosarcomes grâce à des marqueurs immunohistochimiques tels que c-Myc et FLT4 qui sont positifs en cas d’angiosarcome post-radique. (1)
La tumeur a la particularité d’être très envahissante, d’abord au niveau du derme et du tissu sous-cutané mais peut également s’étendre dans le tissu mammaire et finalement devenir métastatique. Les sites de métastases les plus fréquents sont : le sein controlatéral, les ganglions lymphatiques, les poumons, la plèvre, les os, le foie et la peau. (7)
Le traitement de ce type de cancer fait, encore à l’heure actuelle, l’objet de controverse.
Nous essayerons d’exprimer ci-après à l’aide de deux cas cliniques et d’une revue de la littérature, les évidences qui permettent de décider de la prise en charge médicale et chirurgicale la plus adaptée.
Vignette clinique
Cas clinique 1
Il s’agit d’une patiente de 47 ans qui ne présentait pas d’antécédent familial de cancer du sein. Elle était par ailleurs atteinte d’une sclérose en plaque traitée par Interferon bêta depuis 2002.
En 2014, suite à un examen clinique suspect, un bilan sénologique (mammographie, échographie et IRM) avait objectivé deux lésions nodulaires au niveau du sein droit qui furent biopsiées.
Un carcinome intracanalaire associé à une lésion papillaire atypique intra-kystique fut mis en évidence.
La première lésion fut donc stadifiée cTis cNo cMo et hormonosensible (90% RO, 90% RP, HER2-, P53-, Ki67 20%). La deuxième lésion révéla une cytologie atypique et non interprétable. Vu la taille de la lésion à l’IRM (6.5cm de grand axe) on proposa une mastectomie associée au prélèvement du ganglion sentinelle. L’analyse anatomopathologique post-opératoire révéla un carcinome intracanalaire formant une large plage de 10cm de diamètre contenant un papillome intra kystique de 7mm ainsi que 4 foyers de carcinome canalaire infiltrant de 2.5 à 4mm. La stadification finale conclut à un pT1 pN0sn cM0 (RO 90%, RP 40% HER2 -, Ki67 20%).
La concertation multidisciplinaire proposa une radiothérapie adjuvante de 50 Grays délivrée en 25 séances de 2 Grays au niveau de la paroi ainsi qu’un traitement par tamixofène pendant 5 ans. Un suivi sénologique par échographie et mammographie annuel ainsi qu’un suivi clinique par le radiothérapeute tous les 6 mois fut réalisé entre 2014 et mai 2020.
En juillet 2020, la patiente présentait deux petits nodules rougeâtres infra-centimétriques sans induration en inféro-externe par rapport à la cicatrice. Un bilan échographique mettait en évidence, au niveau de la lésion la plus volumineuse, une formation hypoéchogène sous-cutanée de 4mm de grand axe (Figure 1). Le radiologue évoqua un nodule de Velpeau. La cytoponction était atypique avec des cellules fusiformes. Une biopsie chirurgicale démontrera l’angiosarcome post-radique confirmé par l’immunohistochimie positive à c-Myc.
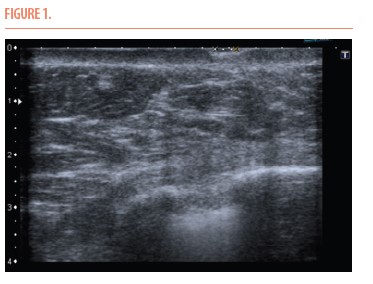
L’IRM réalisée pour le bilan d’extension était négative.
Le traitement de cette lésion d’angiosarcome post-radique du sein consista en une reprise de la mastectomie avec exérèse élargie des deux lésions suspectes associée à une greffe cutanée. Cette résection n’entreprenait pas l’ensemble de la zone irradiée.
Après l’analyse anatomopathologique complémentaire (Figure.2), le diagnostic d’angiosarcome cutané post-radique fut confirmé. Cette lésion était très infiltrante au niveau du derme et extrêmement mal délimitée. En effet, un doute existait concernant la marge de section inférieure. En juin 2021, lors d’une consultation de contrôle, une nouvelle lésion nodulaire au niveau de la partie inférieure de la cicatrice fut biopsiée. Malheureusement, l’analyse conclut à une récidive de l’angiosarcome. Dès lors, une reprise chirurgicale en marge saine fut organisée. La patiente, suivie tous les 6 mois, est en rémission depuis lors.
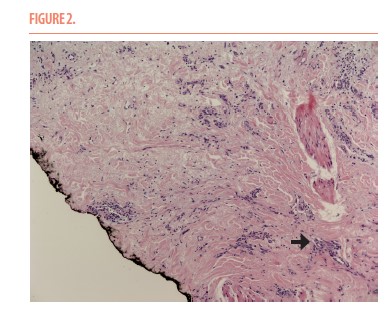
Cas clinique 2
Il s’agit d’une patiente de 75 ans qui ne présentait pas d’antécédent familial de cancer du sein. Ses antécédents personnels étaient marqués par une hypertension artérielle, une hypercholestérolémie, un diabète de type 2 et un épisode d’accident vasculaire cérébral.
En 2012, suite à un bilan sénologique par mammographie et échographie, une lésion de 3cm de grand axe fut biopsiée. L’analyse révéla un carcinome micropapillaire encapsulé avec la présence de plusieurs foyers microscopiques infiltrants triple négatifs (RP 0%, RO 0%, HER négatif) de stade cT2cN0cM0.
Une tumorectomie du quadrant supérieur du sein droit et un curage axillaire furent réalisés.
L’analyse anatomopathologique conclut à un adénocarcinome canalaire infiltrant triple négatif (RO 0%, RP 0% et HER2 -) avec un indice de prolifération élevé (70%) de stade pT2 pN0 cM0.
La patiente bénéficia également d’un traitement adjuvant par chimiothérapie FEC 75 (cyclophosphamide, épirubicine et 5-fluorouracil) à hauteur de 3 cures avec un intervalle de 3 semaines entre chaque cure. Celle-ci fut suivie de 9 cures de paclitaxel hebdomadaires.
Un traitement par radiothérapie fut entrepris au niveau de la glande mammaire droite à raison de 42.4 Grays sur le sein droit avec une surimpression de 16 Grays en 8 fractions au niveau de la cicatrice et du lit tumoral.
En octobre 2020, la patiente présenta une lésion hémorragique au niveau du sein droit. À l’examen clinique, on observait deux nodules semi-centimétriques ainsi qu’une lésion hémorragique ulcérée au niveau de la région inféro-médiane du sein droit (Figure 3).
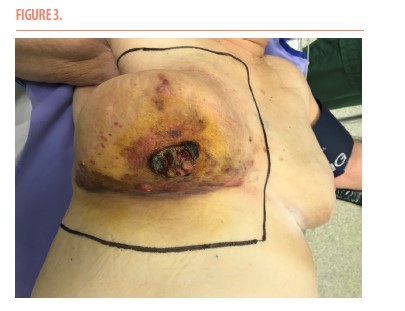
Celle-ci fit l’objet d’un bilan par mammographie qui ne révéla pas d’opacité suspecte ni de signe de récidive ou de microcalcification atypique.
Une échographie complémentaire mit en évidence des microcalcifications de stéatonécrose ainsi qu’un épaississement cutané du niveau inférieur du sein droit (Figure 4).
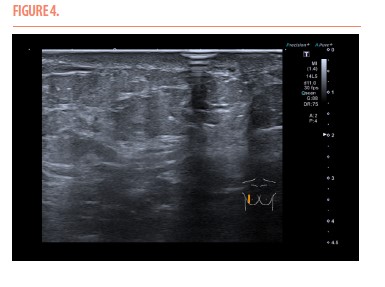
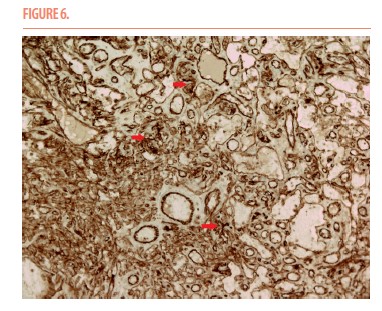
La biopsie cutanée démontra une histologie typique de l’angiosarcome (cellules endothéliales atypiques bordant des fentes vasculaires ramifiées anarchiques) confirmée grâce aux immunomarquages positifs au CD31 et CD34 (Figures 5, 6 et 7). Les anatomopathologistes avaient conclu à un angiosarcome post-radique mais les marqueurs c-Myc et FLT4 n’ont pas été testés.


La prise en charge chirurgicale de cette lésion consista en une mastectomie élargie à toute la zone irradiée du sein droit (Figure 8) avec une greffe cutanée.
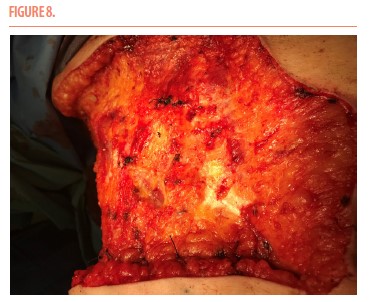
L’analyse anatomopathologique post-opératoire confirma l’angiosarcome. Cette lésion mesurait 17mm de grand axe s’ulcérant à la peau, s’étendant dans le derme et le tissu sous-cutané superficiel. Les marges de résection étaient saines.
Malheureusement en 2021, dans le cadre du suivi de la patiente, deux métastases furent découvertes au niveau pulmonaire droit et des ganglions lymphatiques médiastino-hilaires droits et axillaires gauches. La maladie étant multimétastatique, une prise en charge chirurgicale ne fut pas proposée.
Une chimiothérapie palliative par Taxol hebdomadaire fut proposée mais la patiente et sa famille refusèrent. La patiente fut institutionnalisée suite à un AVC et ne se présenta plus à la consultation d’oncologie malgré une proposition de suivi.
Discussion / Revue de la littérature
Dans le contexte de la chirurgie oncologique conservatrice du sein, la radiothérapie adjuvante (RT) permet de diminuer le taux de récidive locale à 5 ans de 26% à 7% et d’avoir le même taux de survie globale qu’après une mastectomie (8). La radiothérapie est donc toujours indiquée après une chirurgie conservatrice du sein. Après une mastectomie pour un cancer avancé, la RT permet une réduction de 5.4% de mortalité à quinze ans comparé à la mastectomie sans RT. Elle permet également une diminution du risque de rechute locale. La RT est aussi indiquée dans les cancers localement avancés (pT3-4), les cancers stadifiés N2 et les cas où les tranches de sections chirurgicales sont positives à l’analyse anatomopathologique (R1). (8)
Rombouts et al. décrivent en 2019 que 0.1% des patientes développent une complication rare de la radiothérapie : l’angiosarcome. Celle-ci survient avec un temps de latence médian de 8 ans après le traitement du cancer primitif.(5) Abdou Y. et al caractérisent l’angiosarcome de mauvais pronostic avec une survie globale à 5 ans de 51% et une survie sans récidive à 5 ans de 36%. (4)
L’angiosarcome secondaire est une tumeur maligne de l’endothélium à prolifération rapide. Ce type de tumeur se présente macroscopiquement et cliniquement sous forme d’une lésion cutanée indurée non douloureuse, ecchymotique pouvant s’ulcérer. (7)
L’angiosarcome est secondaire lorsque l’on identifie une cause à son développement. L’angiosarcome peut survenir suite à une radiothérapie, comme dans les cas présentés mais peut aussi survenir suite à un lymphœdème chronique, aussi connu sous le nom de syndrome de Stewart-Treves chez les patientes ayant subi un curage ganglionnaire axillaire. (9)
La mammographie n’est pas spécifique et donc peu utile dans le diagnostic des angiosarcomes. L’échographie permet de mettre en évidence des lésions hétérogènes et hypervasculaires, qui peuvent être soit hypoéchogènes soit hyperéchogènes. L’échographie n’est pas spécifique, même si elle permet d’attirer l’attention sur une structure cutanée anormale au niveau mammaire. L’IRM permet une meilleure caractérisation morphologique de la tumeur qui apparait en hypo-signal T1 et hyper-signal T2 signant l’origine vasculaire de la tumeur. La résonance magnétique est surtout utilisée pour le bilan d’extension mais également pour détecter les récidives de l’angiosarcome au niveau du site d’exérèse. (7)
L’élément clé du diagnostic reste la biopsie des lésions suspectes. L’angiosarcome est caractérisé par des travées vasculaires anarchiques bordées de cellules endothéliales porteuses d’atypies nucléaires (Figure 9) (7).
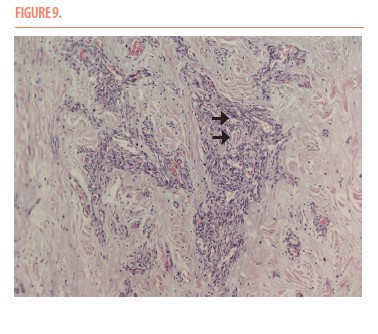
L’analyse histologique comprend la recherche de marqueurs tels que le CD31, le CD34, le facteur VIII, Fli-1 et ERG. Ceux-ci confirment l’origine vasculaire de la lésion. (7) Dans les deux cas cliniques présentés précédemment, CD31 et CD34 ont tous deux été mis en évidence. Le CD31 est spécifique de l’angiosarcome alors que le CD34 est plus sensible. (10)
e traitement préférentiel de l’angiosarcome secondaire est la résection chirurgicale élargie de la lésion en R0. (4)
La résection radicale de toute la zone cutanée précédemment irradiée permet une augmentation de la survie (86 % versus 46 % chez les patients ayant bénéficié d’une tumorectomie simple) et une diminution des récidives locales (3). Par contre, la dissection axillaire des ganglions n’est pas à effectuer d’emblée puisque l’angiosarcome présente rarement des métastases à ce niveau. (7)
L’utilisation de la chimiothérapie est très controversée. Certains auteurs comme Gutkin et al. démontrent un effet significatif sur la survie totale (3) mais ce n’est pas le cas dans d’autres méta-analyses (4). La chimiothérapie à base de taxane aurait une place en cas de tumeur de haut grade, ainsi que la doxorubicine qui peut être recommandée en cas de tumeur métastatique et/ou irrésécable. (4)(5)
Paradoxalement, la radiothérapie permet d’améliorer la survie sans rechute de l’angiosarcome secondaire. C’est une alternative thérapeutique lorsque les marges de résection chirurgicales sont positives. (4)
Dans les deux cas présentés précédemment, la chirurgie a effectivement été le traitement de première intention. Dans le premier cas, l’ensemble du lit de la radiothérapie ne fut pas totalement réséqué, seule la lésion d’angiosarcome fut retirée en marges saines. Par contre, pour la deuxième patiente, une attention particulière fut apportée à retirer tout le lit de la radiothérapie.
D’ailleurs, dans le premier cas, il y a eu une récidive locale. En effet dans ce cas, les marges de résection de la première exérèse de l’angiosarcome étaient positives au niveau inférieur. Une seconde intervention, plus large, a dès lors été nécessaire.
Pour le second cas, il n’y pas eu de récidive locale mais des métastases se sont manifestées à distance. Cela pourrait être dû à une dissémination micro métastatique déjà en cours au moment du diagnostic et non décelable par les différents examens complémentaires.
Un point d’approche intéressant est la comparaison entre les angiosarcomes primaires et les angiosarcomes secondaires à la radiothérapie.
L’angiosarcome primaire correspond à 0.04% des tumeurs mammaires. Ce type de néoplasie touche plus les femmes jeunes entre 30 et 40 ans. L’angiosarcome secondaire survient chez les femmes plus âgées. (1)
L’angiosarcome primaire se présente souvent comme une large masse du parenchyme mammaire. L’angiosarcome secondaire s’exprime, lui, comme une lésion cutanée ecchymotique plus ou moins ulcérée. (4)
Dans l’analyse par la technologie FISH, les angiosarcomes secondaires présentent une amplification de MYC et de FLT4 qui n’est pas retrouvée chez les patientes atteintes par un angiosarcome primaire. (3)
L’angiosarcome primaire a une survie à 5 ans plus longue que l’angiosarcome secondaire (73.7% versus 63.5%) et est moins enclin à développer des récidives locales ainsi que des métastases à distance. (3)
La prise en charge des deux types d’angiosarcomes repose sur le geste chirurgical en marge saine. La différence majeure étant que, dans le cas de l’angiosarcome secondaire à la radiothérapie, la résection doit concerner l’ensemble de la zone précédemment irradiée afin d’éviter la survenue d’autres lésions de type angiosarcome. L’angiosarcome primaire doit être réséqué avec une marge de 1cm à 2cm pour les tumeurs inférieures ou égales à 5cm de diamètre. (3)
Conclusions
L’angiosarcome post-radique est une complication rare de la radiothérapie qui est un traitement adjuvant essentiel du cancer du sein. Cette complication survient plusieurs années après l’irradiation.
Ce type de tumeur endothéliale se présente typiquement sous la forme d’une lésion cutanée qui peut être ulcéro-hémorragique. C’est l’immunohistologie qui permet le diagnostic par mise en évidence de marqueurs endothéliaux comme par exemple le CD31 qui est un marqueur vasculaire spécifique.
Les marqueurs tels que c-Myc et FLT4 permettent de confirmer la nature post-radique de l’angiosarcome.
Le traitement de première intention est la résection chirurgicale en marge saine emportant toute la zone irradiée, qui peut être le siège de nouvelle lésion d’angiosarcome.
Affiliations
1. Assistante en chirurgie, Clinique Saint-Luc, B-5004 Bouge
2. CHR de Verviers, Chirurgie Digestive, stanislas.laurent@chrverviers.be
Correspondance
Dr. Charlotte Charlier
Clinique Saint-Luc
Chirurgie
Rue Saint-Luc 8
B-5004 Namur
charlotte.charlier@student.uclouvain.be
Références
- Farran Y, Padilla O, Chambers K, Philipovskiy A, Nahleh Z. Atypical Presentation of Radiation-Associated Breast Angiosarcoma: A Case Report and Review of Literature. Am J Case Rep. 2017 Dec 18;18:1347–50.
- Torres KE, Ravi V, Kin K, Yi M, Guadagnolo BA, May CD, et al. Long-term outcomes in patients with radiation-associated angiosarcomas of the breast following surgery and radiotherapy for breast cancer. Ann Surg Oncol. 2013 Apr;20(4):1267–74.
- Gutkin PM, Ganjoo KN, Lohman M, von Eyben R, Charville GW, Nazerali RS, et al. Angiosarcoma of the Breast: Management and Outcomes. Am J Clin Oncol. 2020 Nov;43(11):820–5.
- Abdou Y, Elkhanany A, Attwood K, Ji W, Takabe K, Opyrchal M. Primary and secondary breast angiosarcoma: single center report and a meta-analysis. Breast Cancer Res Treat. 2019;178(3):523–33.
- Rombouts AJM, Huising J, Hugen N, Siesling S, Poortmans PM, Nagtegaal ID, et al. Assessment of Radiotherapy-Associated Angiosarcoma After Breast Cancer Treatment in a Dutch Population-Based Study. JAMA Oncol. 2019 Feb;5(2):267–9.
- Hamels J, Blondiau P, Mirgaux M. Cutaneous angiosarcoma arising in a mastectomy scar after therapeutic irradiation. Bull Cancer. 1981;68(4):353–6.
- Bonito FJP, de Almeida Cerejeira D, Dahlstedt-Ferreira C, Oliveira Coelho H, Rosas R. Radiation-induced angiosarcoma of the breast: A review. Breast J. 2020;26(3):458–63.
- Wendy Jeannerez Sozzi, René-Olivier Mirimanoff. Indications de la radiothérapie dans le cancer du sein non métastatique [Internet]. Revue Medicale Suisse. [cited 2022 Feb 21]. Available from: https://www.revmed.ch/revue-medicale-suisse/2007/revue-medicale-suisse-1...
- Esposito E, Avino F, di Giacomo R, Donzelli I, Marone U, Melucci MT, et al. Angiosarcoma of the breast, the unknown—a review of the current literature. Transl Cancer Res. 2019 Oct;8(S5):S510–7.
- Majdoubi A, Serji B, Harroudi TE. Angiosarcome mammaire radio-induit: à propos d’un cas. Pan Afr Med J. 2020 May 21;36:29.