Une problématique connue des la découverte des premiers antibiotiques
Au tournant du XXème siècle, les avancées en matière de maladies infectieuses connaissent une intensité fulgurante. Parmi les avancées majeures, l’usage thérapeutique des antibiotiques occupe une place prépondérante. Le microbiologiste écossais Alexandre Fleming découvre alors la pénicilline. Alertant sur la problématique de la résistance, il fera d’emblée la remarque suivante : « La personne irréfléchie qui joue avec un traitement à base de pénicilline est moralement responsable de la mort de l’homme qui succombe à une infection par l’organisme résistant à la pénicilline. » Ce pionnier de la découverte des antibiotiques mesure d’emblée la responsabilité collective autour de leur usage et la met en exergue. L’ABR est donc un phénomène connu, appréhendé et décrit dès la découverte des premiers antibiotiques. Pourtant, force est de constater que, jusqu’à l’aube du XXI ème siècle, cette problématique reste largement occultée et ignorée (Figure 1).
Chaque année, près de 33 000 personnes (1) meurent en Europe des suites d’une infection par un pathogène résistant. Le chiffre vertigineux de 700 000 morts par an dans le monde, dont la majorité dans les pays en développement, est avancé par l’Organisation mondiale de la santé (OMS). Les estimations pour les décennies à venir s’avèrent encore plus préoccupantes. En 2050, chaque année, 10 millions de personnes pourraient mourir des conséquences de l’ABR (2). Il ne nous est guère permis d’ignorer aujourd’hui les enjeux sanitaires qui en découlent. Dans un futur proche, il incomberait ainsi à l’ABR une surmortalité directe importante mais également la mise en péril de nombreuses avancées de la médecine moderne (chirurgies complexes, réanimation, oncologie, transplantation) ; autant d’avancées pour lesquelles l’antibiothérapie constitue une pierre angulaire.
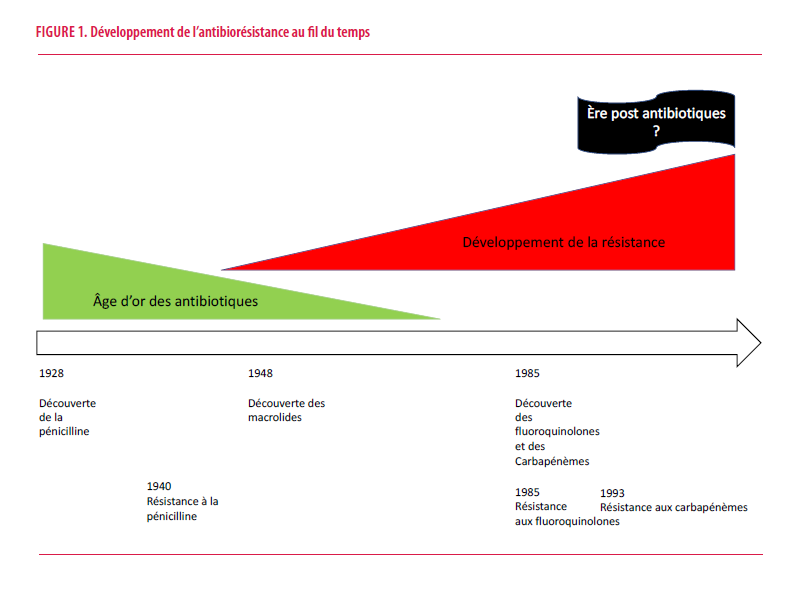
L’ABR, une problématique globale dans un monde interconnecté
L’histoire des antibiotiques s’inscrit pleinement dans le cadre de la globalisation, tant au niveau de leur production que dans leur consommation (3). La résistance ne fait pas exception à la règle et l’émergence de pathogènes résistants aux antibiotiques à un endroit de la planète est rapidement transposée à l’échelle du globe. L’ABR ne connait donc pas de frontières et se diffuse parfois indépendamment des mouvements humains. A titre d’exemple, une équipe de microbiologistes scandinaves (4) a montré que les oiseaux résidants en Arctique, dans des contrées parmi les plus désertiques de la planète, sont colonisés par des bactéries multirésistantes. Les espèces animales ne sont pas les seules à être contaminées. L’environnement l’est également partout sur la planète. A ce titre, une étude menée par Mc Cann et al (5) a mis en évidence 131 gènes de résistance dans des échantillons prélevés dans l’archipel désertique du Svalbard en Norvège. Ces gènes sont retrouvés dans le sol d’une terre lointaine, éloignée de toute civilisation ou activité humaine. Fait notable, on y a retrouvé notamment le gène blaNDM-1, gène de résistance aux carbapénèmes, qui en moins de dix ans, a colonisé les zones les plus désertiques de la planète.
Une problématique multifactorielle
La résistance aux antibiotiques se situe aux confins des problématiques géopolitiques contemporaines telles que les guerres, le climat, la migration, la gouvernance mondiale et les inégalités de développement. Prise en étau entre des guerres successives et pauvreté extrême, le Moyen-Orient est une région du monde déstabilisée de façon chronique depuis plusieurs décennies et une des contrées les plus vulnérables aujourd’hui. C’est aussi un exemple probant d’émergence et de diffusion de résistance. En Irak, en Syrie, au Yémen, le fardeau en vies humaines est immense, et le coût économique prohibitif. L’impact économique potentiel est estimé par Taylor et al dans la région entre 2 milliards et 159 milliards sur 40 ans (7).
Analysant l’exemple syrien, Jakovljevic et al (6) ont démontré que l'ABR est très peu mise en lumière bien que la corrélation avec la déstabilisation chronique de cette région du monde soit réelle. Dans un tel contexte géopolitique, une conjonction de facteurs intervient pour créer un modèle favorable où l’ABR explose : effondrement des systèmes de santé, vente libre des antibiotiques, contrebande de médicaments, nature des armes employées, type de traumatisme etc. Aussi faut-il ajouter à cela les difficultés d’approvisionnement et le climat quasi-anarchique et l’absence de règles des pays en guerre.
Exacerbée par les crises contemporaines, la résistance aux antibiotiques est aussi un enjeu de gouvernance car les pays les plus fragilisés sont aussi les plus vulnérables face à ce phénomène. Pierre Collignon et al. (8) ont étudié la résistance aux antibiotiques, en Europe, en fonction de la consommation humaine d’antibiotiques, des dépenses de santé dans le secteur privé, du niveau d’éducation supérieur, du niveau économique (revenu par habitant) et la qualité de la gouvernance. En tout, vingt-huit pays européens ont servi d’objet d’étude sur la période de 1998 et 2010. Étonnamment, seulement 28% de la variation de la résistance entre les pays est attribuable à la variation de l’usage des antibiotiques. Lorsque le facteur gouvernance est ajouté en tant que variable additionnelle, 63% de la variation totale est expliquée. La qualité de la gouvernance apparait comme le paramètre socioéconomique le plus important. L’hypothèse des auteurs est que le faible niveau de gouvernance est associé à une absence de contrôle de l’usage des antibiotiques. Ces défis particuliers sont particulièrement présents dans les contrées les plus pauvres du globe qui font face à de nombreux défis tels que la vente libre et non réglementée des antibiotiques ; souvent contrefaits ; l’absence de mise en place de réseaux de surveillance nationaux performants ; l’absence d’accès au diagnostic microbiologique.
Une prise de conscience lente et tardive
Un retard immense a été pris dans la lutte contre l’ABR et la prévention y afférent. Pourtant, dès 1945, les scientifiques alertent sur l’usage incontrôlé des antibiotiques. En 1988, Lederberg affirme déjà : « Dans la compétition naturelle entre bactéries et humains, il n’est aucune garantie que nous soyons les survivants ». Dans cette affirmation alarmiste transparait déjà la prise de conscience de la communauté scientifique. En 1998, Richard Wise (9) exprime également son inquiétude en commençant un article par la remarque suivante : « Les problèmes de résistance aux antimicrobiens suscitent de nouvelles inquiétudes ». En 2007, Richard James, va plus loin en proposant le terme d’« apocalypse post antibiotique ». A l’heure actuelle, la prise de conscience et l’engagement dans les problèmes entourant l’ABR est bas comparé à d’autres problématiques globales telles que le climat. La mesure de l’urgence à agir reste encore trop cloisonnée aux milieux académiques et d’expertises sans pour autant parvenir à amorcer une prise de conscience au niveau politique. Cette dissociation entre scientifiques et décideurs politiques est au cœur du retard pris dans la gestion de cette crise.
A l’échelle européenne, la prise de conscience se construit et s’étoffe depuis le début des années 2000. Depuis 2001 et à la suite de l’adoption de la recommandation du conseil de l’Union européenne sur l’utilisation des agents antimicrobiens en médecine humaine, les activités de lutte contre la résistance se sont développées à l ‘échelle de l’ECDC (European Center for Disease Prevention). Celles-ci s’étendent aux domaines de la surveillance, la surveillance épidémique, la formation, la mise en place d’un répertoire de ressources en ligne et le soutien aux états membres lors de l’élaboration de leurs plans nationaux. (10, 11) En Belgique, de façon relativement récente un plan d’action ambitieux s’étendant sur quatre années (2020-2024) (12) a été mis en place, reflétant une prise de conscience nette nourrie par l’ambition d’un leadership fort et d’une coordination efficace.
À l’échelle planétaire et notamment dans les pays à ressources limitées, c’est finalement le positionnement de l’OMS, en 2015, au travers d’un rapport qui montre l’urgence à intervenir, qui servira de réelle prise de conscience. Bien qu’insuffisantes, différentes initiatives se mettent progressivement en place pour tenter d’y apporter une réponse adéquate. Les initiatives sont nombreuses et structurées en 4 grands axes :
- mieux comprendre l’émergence, la transmission et la dissémination de l’ABR ;
- améliorer l’usage des antibiotiques, promouvoir un usage raisonné en médecine humaine et animale pour préserver le capital antibiotique restant ;
- développer des stratégies curatives et préventives innovantes, développer la recherche de nouveaux antibiotiques ;
- améliorer la gouvernance, lutter contre la corruption dans les zones les plus impactées.
La réponse structurée commence à se dessiner et la prise de conscience à se former petit à petit. Les plans nationaux se multiplient ainsi que les tentatives de limitation de la consommation des antibiotiques en santé humaine et animale, du moins dans les pays à haut revenus. Le concept « one health » se situe au cœur de cette réponse.
L’ABR, un champ d’application important du concept « One Health »
Dans la riposte face à l’ABR, le concept « one health » s’impose progressivement comme le prisme de lecture principal. Il se construit en puisant dans le paradigme selon lequel santé humaine, santé animale et environnement sont interconnectés. Ainsi, structurer la réponse à travers ce prisme permet d’augmenter la résilience de nos sociétés face à ce défi commun.
Il existe différentes définitions de ce concept. L’association des vétérinaires américains le définit comme un effort intégratif de multiples disciplines travaillant à l’échelle locale, nationale et globale pour atteindre une santé optimale pour les hommes, les animaux et l’environnement (AVMA 2008) (13). La FAO (Food and agricultural organisation) (2012) (14) quant à elle, définit l’approche one health comme un mécanisme multidisciplinaire, international et collaboratif pour aborder et réduire les risques infectieux à l’interface homme, animal, écosystèmes. Enfin, l’initiative one health évoque une stratégie mondiale pour développer les collaborations interdisciplinaires dans tous les aspects de la santé pour les hommes, les animaux et l’environnement. (15) Si elles se déclinent de façon sensiblement différente, toutes ces définitions ont en commun de mettre l’accent sur une approche intégrative de la santé, avec comme pierres angulaires la coordination entre les différents acteurs et la transversalité.
L’ABR (Figure 2) répond aisément au cadre d’application de ce concept car les bactéries résistantes présentes chez l’animal se transmettent à l’homme ou l’environnement et vice versa. En médecine vétérinaire, les antibiotiques sont largement employés de façon préventive et curative et étaient jusqu’à il y a peu employés comme facteurs de croissance pour les animaux d’élevage, pratique aujourd’hui interdite dans l’union européenne. Les bactéries résistantes sélectionnées par l’antibiothérapie en médecine humaine peuvent également se transmettre à l’animal. Par ailleurs, les eaux usées peuvent contaminer les sols et les végétaux. Les niveaux de transmission sont donc multiples et se font à différents niveaux, intégrant les trois composantes du concept « one health ».
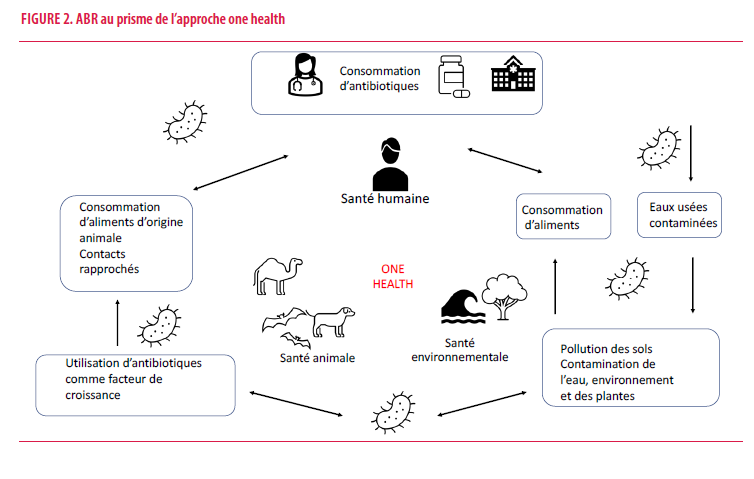
L’utilisation du « concept « one health » est particulièrement intéressante dans un monde globalisé car plastique et adaptable aux enjeux nationaux voir locaux, tout en maintenant une ligne directrice. Dans un monde interconnecté, avec des défis sanitaires souvent partagés, il est particulièrement pertinent d’avoir des grilles de lectures communes pour lutter contre les enjeux globaux tout en pouvant s’adapter aux problématiques locales.
Ainsi l’approche one health peut être appliquée en réponse à des contextes spécifiques comme celui de la peste pulmonaire à Madagascar ou la grippe aviaire en Afrique de l’ouest. Cette approche intersectorielle peut également être appliquée à des problèmes régionaux. C’est à titre d’exemple une des principales voies à explorer en réponse aux crises récurrentes d’insécurité alimentaire en Afrique subsaharienne. C’est également une grille de lecture qui peut être appliquée à des problématiques plus globales comme l’ABR ou le risque zoonotique. En Belgique, de nombreux projets de recherche ont été développés structurés par cette thématique (plus de 200 projets et activités de recherche) (17). Les efforts en ce sens sont concentrés sur trois thématiques principales : les zoonoses, la résistance aux antimicrobiens, environnement et santé.
D’après Leboeuf (17) et Cassidy (18), l’appropriation du concept « one health » par les différents acteurs et les succès de sa mise en application s’expliquent par le fait qu’il répond à la définition d’un objet frontière (19). Les objets frontières sont des objets qui sont suffisamment plastiques et flexibles pour s’adapter aux besoins locaux et aux contraintes des différentes parties impliquées mais dans le même temps suffisamment solide pour maintenir une identité commune à travers les différents sites de mise en application. La force inhérente d’un tel objet est ainsi qu’il amène aisément les différentes parties à collaborer.
La flexibilité offerte permet à ce concept d’être appliqué dans de multiples objectifs et à s’adapter aux différents contextes permettant ainsi à toutes les parties prenantes de s’y reconnaitre et de se l’approprier.
La pertinence d’une telle approche plastique et adaptable à différents contextes apparait assez incontestable dans le contexte de la gestion de l’ABR. De façon assez inédite, l’approche one health permet aux différentes institutions internationales comme WHO (World Health Organization), la FAO, l’OIE (World Organization for Animal Health) de collaborer de façon non concurrentielle, avec une légitimité des différentes parties renforcée dans un esprit de collaboration et une intégration aux défis géopolitiques du monde contemporain (20).
Conclusion
La construction de la réponse à l’ABR est un des nombreux défis collectifs en cours en santé globale. La réponse réside probablement dans une santé planétaire éthique ainsi qu’une écologie transversale, nourries d’une conscience aiguë des interdépendances et de l’impératif de coopération globale. Elle se doit également d’être intégrative, englober l’éthique animale et de l’environnement et prendre en compte la pluralité des déterminants anthropologiques.
Malgré son importance, encore aujourd’hui, le degré de reconnaissance publique de cette problématique essentielle demeure fâcheusement faible. L’émergence infectieuse c’est aussi et surtout l’émergence en devenir des consciences collectives. Pour l’heure, force est de constater que celle ayant trait à l’ABR fait encore cruellement défaut.
Correspondance
DR. Amel Filali, MD, MSc, MA
CHC Montlégia
Service de médecine interne et Maladies infectieuses
Boulevard Patience et Beaujonc 2
B-4020 Liège, Belgique
filali0amel@yahoo.fr
Références
- https://antibiotic.ecdc.europa.eu/en/get-informed/key-messages/health-bu...
- https://amr-review.org/sites/default/files/AMR%20Review%20Paper%20-%20Ta...
- Andremont A. « Antiobiotiques et antibiorésistance, un avatar singulier de l’histoire planétaire », Questions de communication. 2016 ;. 29 (1) : 15-27.
- Sjölund M, Bonnedahl J, Hernandez J, Bengtsson S, Cederbrant G, Pinhassi J, et al.. Dissemination of Multidrug-Resistant Bacteria into the Arctic. Emerg Infect Dis. 2008 Jan;14(1):70-2.doi: 10.3201/eid1401.070704.5.
- McCann CM , Christgen B , Roberts JA , Su JQ, Arnold KE , Gray ND , et al. Understanding drivers of antibiotic resistance genes in High Arctic soil ecosystems. Environ Int. 2019 Apr;125:497-504.doi: 10.1016/j.envint.2019.01.034.
- Jakovljevic M, Al Ahdab S, Jurisevic M, Mouselli S. Antibiotic Resistance in Syria: A Local Problem Turns Into a Global Threat. Front Public Health. 2018 Aug 2;6:212. doi: 10.3389/fpubh.2018.00212. eCollection 2018.
- Taylor J, Hafner M, Yerushalmi E, Smith R, Bellasio J, Vardavas R, et al. Estimating the Economic Costs of Antimicrobial Resistance. Model and Results. Rand Corporation. 2014.
- Collignon P, Beggs JJ, Walsh TR, Gandra S, Laxminarayan R. Anthropological and socioeconomic factors contributing to global antimicrobial resistance: a univariate and multivariable analysis. Lancet Planet Health. 2018 Sep;2(9):e398-e405. doi: 10.1016/S2542-5196(18)30186-4.
- Wise R, Hart T, Cars O, Streulens M, Helmuth R, Huovinen P, Sprenger M. Antimicrobial resistance. Is a major threat to public health. BMJ. 1998 Sep 5;317(7159):609-10.doi: 10.1136/bmj.317.7159.609.
- https://ec.europa.eu/health/system/files/2020-06/amr_projects_3rd-report...
- https://antibiotic.ecdc.europa.eu/en
- https://www.health.belgium.be/fr/lutte-contre-la-resistance-aux-antimicr...
- https://www.avma.org/one-health-what-one-health
- https://www.fao.org/one-health/fr
- One Health Initiative-One World One Medicine One Health: About the One Health initiative. Kahn, L. 2012.
- Leboeuf, A. Making sense of One Health: Cooperating at the human-animal- ecosystem health interface. Health and Environment Report. April 2011; 7.
- https://www.sciensano.be/nl/projecten
- Cassidy A. One Medicine? – Investigating interdisciplinary collaboration. Rutgers University Press, 2016.
- van Herten J, Bovenkerk B, Verweij M. One Health as a moral dilemma: Towards a socially responsible zoonotic disease control. Zoonoses Public Health. 2019 Feb;66(1):26-34. doi: 10.1111/zph.12536..
- Chien, YJ. How did international agencies perceive the avian influenza problem? The adoption and manufacture of the ‘One World, One Health’ framework Sociol Health Illn. 2013 Feb;35(2):213-26. doi: 10.1111/j.1467-9566.2012.01534.x.