Introduction
Depuis quelques mois, le monde fait face à une pandémie de syndromes respiratoires aigus sévères (ARDS) causés par un nouveau coronavirus dont le matériel génétique est similaire à plus de 80% avec celui de chauves-souris (bat-SL-CoVZC45, bat-SL-CoVZXC21) (1). Les coronavirus sont des virus à ARN connus depuis longtemps des scientifiques et du monde médical, en particulier pour leur capacité à causer des pneumonies chez l’humain, parfois à l’issue fatale. Ces virus ont par ailleurs un tropisme pour le système cardio-vasculaire (CV). Ils sont particulièrement nocifs chez des sujets présentant des comorbidités, comme en témoignent les précédentes épidémies virales telles que le MERS (middle east respiratory syndrome coronavirus) ou le SRAS-COV (acute respiratory syndrome coronavirus). Mieux comprendre les effets de COVID-19 sur le système CV est essentiel pour combattre efficacement ce nouvel agent pathogène. Cet article passe en revue ce qui est actuellement connu d’un point de vue cardiologique sur ce nouveau virus.
Facteurs de risque et maladies cardio-vasculaires préexistantes
Avec le recul actuel dont on dispose, on constate que l’infectiosité (ou nombre de reproduction d’un germe pathogène) et la virulence du COVID-19 (dénommé initialement 2019-nCoV puis ‘SARS-CoV-2’ par l’OMS) sont supérieures à la grippe saisonnière. Dans la province de Hubei où ce nouveau pathogène est soupçonné être apparu en décembre 2019, 81% des cas ont été classés comme légers, mais 14% étaient graves et 5% nécessitaient des soins intensifs (S.I.). Le taux de létalité global moyen était de 2,3 % mais variait considérablement selon les moyens mis en œuvre pour soigner les populations et également selon les classes d’âge. Faible chez les moins de 60 ans, la mortalité observée entre 70 et 79 ans était d’environ 8,0 %, mais dépassait les 14% chez les octogénaires (2). Force est donc de constater que le nombre de décès est beaucoup plus élevé que l’estimation initiale présentée par les autorités chinoises ou que les précédentes épidémies de SRAS-COV (Sarbecovirus, années 2002-2003 : 916 morts) ou du METS-CoV (Merbecovirus, années 2012-13 : 800 morts) au Moyen-Orient (3,4). Notons encore qu’une proportion faible (1.2% selon les chinois) des personnes atteintes reste mystérieusement asymptomatique (porteurs sains) (5). Face à l’ampleur d’un désastre humanitaire qui s’annonçait comme rapide, l’OMS a considéré le 11 mars 2020 (trop tardivement selon certains experts) que l’épidémie était devenue « pandémique » et que les moyens à mettre en œuvre pour la combattre devenaient une urgence mondiale (6). Aujourd’hui, on ne parle déjà presque plus de pandémie mais du risque d’endémie lié à un virus qui ne disparaîtrait plus jamais. Les taux les plus élevés de décès sont sans surprise enregistrés chez les patients les plus vulnérables, dont les cardiaques. Ceci a déjà été observé précédemment pour les virus respiratoires comme en 2013 lors de l’infection par l’influenza H7N9 où plus de 60% des patients sévèrement atteints présentaient au moins une comorbidité ou une maladie cardiaque chronique (7). L’infection par d’autres beta-coronavirus comme le MERS-COV était aussi plus susceptible de se produire chez les patients présentant une maladie CV préexistante (8). Une estimation précise du nombre de patients cardiaques atteints du COVID-19 reste toutefois, une entreprise périlleuse compte tenu de l’absence de dépistage à grande échelle au sein de la population générale, dans les hôpitaux ou les maisons de retraite et de soins. De nouveaux tests sérologiques seront probablement disponibles à plus grande échelle dans un avenir proche, mais il aurait été idéal de connaître ce chiffre dès le début de l’épidémie. Une première analyse réalisée rétrospectivement sur les premiers patients chinois indique que l’HTA, le diabète touchaient respectivement 15 et 20% d'entre eux. La prévalence des maladies CV était chez cette quarantaine de patients chinois d’environ 15% (9). Les données ISARIC (International Severe Acute Respiratory and Emerging Infection Consortium), vont dans le même sens (Figure 1). Selon une autre enquête chinoise portant sur les données de 1099 patients, l’hypertension était présente dans près de 15%, le diabète dans 7% environ, la maladie coronaire dans seulement 2.5% (10). Au sein des instituts de soins chroniques, les données épidémiologiques sont différentes de la population générale comme on pourrait s’y attendre. Ainsi, dans un registre américain réalisé au sein de maisons de soins, la grande majorité des résidents COVID-19 (+) étaient hypertendus (±67%), cardiaques (±60 %), ou souffraient d’une maladie rénale (±40 %), ou d’un diabète (±31%). Cancers, maladies pulmonaires étaient aussi des pathologies chroniques fréquentes (11).

Cela aura un impact sur les chiffres de mortalité du virus en Belgique qui a fortement touché les maisons de repos et soins (MRS) et déclenché une vaste réflexion sur l’absence de mesures prises par les autorités pour protéger les séniors. Comme dans les MRS, les patients admis aux S.I. présentent une maladie cardio-vasculaire dans plus de 50% des cas, et une fois sur trois, ces malades critiques présentent au moins 2 comorbidités (12). Comme déjà observé pour des infections respiratoires virales similaires, tous ces facteurs sont de mauvais pronostic et prédisent l’apparition de nouvelles atteintes cardiaques, et l’évolution du malade vers un état de choc, une défaillance multi systémique, une arythmie ventriculaire létale (4).
Complications cardiovasculaires du COVID-19
Les statistiques concernant les atteintes cardiaques liées au COVID-19 sont encore très limitées dans les pays occidentaux. Elles sont non seulement incomplètes mais on fait face à une absence de comparaison directe entre les patients « naïfs » qui développent des complications cardiologiques et ceux déjà cardiaques avant d’être infectés et qui suite au virus se déstabilisent.
Symptômes d’allure cardiologiques
Selon la data base ISARIC, environ 10% de patients se présentent avec des douleurs thoraciques suspectes. Toutefois, les symptômes « cardinaux » de l’infection sont la température (56%), puis la dyspnée et la toux (48%). La perte de l’odorat et du goût sonne également comme des symptômes très sensibles pour suspecter la maladie. Or, un SCA peut se présenter d’une manière similaire avec de la dyspnée, et un diagnostic correct n’est pas forcément établi d’emblée. S’il est difficile de lier toutes les douleurs thoraciques d’apparence ‘cardiaques’ à des atteintes myocardiques plutôt que pulmonaires, il est certain que le virus peut causer des dommages sévères hors des voies respiratoires dont le cœur. Les atteintes cardiaques diverses comme des arythmies, des syndromes coronaires, des états de choc hémodynamiques sont d’ores et déjà rapportées par les équipes de terrain. D’autres organes sont aussi le lieu de complications comme des lésions dermato, oculaires, hépatiques (et cholestase) ou rénales (glomérulonéphrites, nécroses tubulaires). Par ailleurs, les taux d’embolies pulmonaires semblent être également élevés. Dans une étude portant sur 214 patients COVID-19, plus de 36% présentaient des manifestations neurologiques (13). Sous l’impulsion de l’ISARIC et l’OMS, un questionnaire européen dénommé CAPACITY-COVID va servir dans le futur de registre de référence. Mis en place depuis fin mars (www.capacity-COVID.eu) il permettra un meilleur cadastre des présentations cliniques des patients COVID-19 (14). L’espoir de cette initiative est également d’aider à identifier l’incidence réelle des complications CV des patients atteints de COVID-19, et de suivre l’évolution clinique des patients cardiaques.
Patients hypertendus, et rôle du système rénine-angiotensine dans l’infection COVID-19
Des inquiétudes ont été relayées dans la presse médicale et grand public concernant l’usage dans l’HTA d’inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA), et d’antagonistes des récepteurs de l’angiotensine (ARA) vis-à-vis du COVID-19. Ces inquiétudes sont basées sur la forte prévalence de l’HTA des patients malades (traités par IECA) et sur les mécanismes développés par le virus pour infester les cellules de l’organisme hôte. L’infection des voies respiratoires par COVID-19 est déclenchée par la liaison du virus à l’enzyme de conversion de l’angiotensine 2 (ou ACE2 pour Angiotensin-Converting Enzyme-2) située à la surface de l’épithélium des voies respiratoires, mais aussi des vaisseaux, et du cœur. L’ ACE2 est l'homologue de l’ACE1, qui convertit l’angiotensine I en angiotensine II. Pour rappel, l’ACE-I joue un rôle néfaste dans l’organisme en majorant e.a. la tension artérielle. Cette enzyme est très impliquée dans l’insuffisance cardiaque par le biais du système rénine-angiotensine. Si la liaison de l’ACE2 au virus permet à ce dernier de pénétrer les cellules épithéliales pulmonaires, elle est également largement exprimée dans les cellules endothéliales vasculaires cardiaques, mais aussi des reins, du foie, de l’intestin, etc. En d’autres termes, le coronavirus peut probablement pénétrer dans n’importe quel tissu ou organe tant que le nombre nécessaire d’ACE2 est disponible. Une fois exposés au coronavirus, ces organes peuvent également être profondément affectés et déclencher secondairement une réponse immunitaire intense liée à l’activation de diverses cellules immunitaires (lymphocytes T6, T8, etc…). Dans une cascade immunitaire que l’on pense incontrôlée (« cytokine storm »), ces cellules libèrent de nombreuses interleukines (IL6, 17, …) et autres cytokines qui provoquent l’atteinte multi-systémique irréversible qui emporte nombre de patients. Compte tenu de l’importance de l’ACE2 dans la pénétration des COVID-19, il a été suggéré que les médicaments agissant sur l’ACE-I et 2 pourraient contribuer à majorer la sévérité de la maladie. Les données sont expérimentales et conflictuelles. En l’absence d’évidence clinique que les inhibiteurs de l’enzyme de conversion aggravent réellement la maladie, la Société Européenne d’Hypertension recommande chez les patients stables (infectés ou suspects de l’être) de ne pas stopper ces traitements à l’heure actuelle.
Atteinte systémique vasculaire
Les présentations cliniques très variées et multi-systémiques observées chez les patients laissent à penser que les formes les plus graves de l’affection s’apparentent plus à une maladie inflammatoire sévère qu’une infection virale. Les résultats d’analyses histo-pathologiques de patients sévèrement atteints indiquent en effet qu’il existe une sur-activation des cellules T CD8 e. a. chargées de granules cytotoxiques ( lymphocytes Th17 sécréteurs de diverses IL). Une des hypothèses est que le recrutement de cellules immunitaires, soit par l’infection virale elle-même de l’endothélium ou médiée par des processus immunitaires pourrait entrainer un dysfonctionnement endothélial « généralisé » associé à de l’apoptose. Ceci explique les atteintes ischémiques multiples : SCA, AVC, embolies, ischémie intestinale, gangrènes) telles qu’observés de par le monde. Ces craintes viennent d’être étayées par un groupe suisse qui dans une correspondance avec le Lancet a démontré que l’infection virale touchait préférentiellement les cellules endothéliales humaines qui tapissent les différents lits vasculaires de nos organes (poumons, rein, cœur, …). Rapportées chez 3 patients, ces inflammations vasculaires conduisent à de l’occlusion vasculaire, et à la mort cellulaire. Parmi les patients rapportés, citons celui d’une femme de 58 ans qui a succombé brutalement d’un SCA de type STEMI. Son autopsie a prouvé la présence d’une cicatrice d’infarctus comme attendu mais aussi de lésions inflammatoires vasculaires sévères sans signes typiques de myocardite (15). Sur un autre patient dont la présentation clinique était totalement différente (ischémie mésentérique), l’analyse histologique de l’intestin réséqué a également confirmé la présence massive de processus inflammatoires vasculaires occlusifs. Ces phénomènes jouent un rôle important dans l’évolution clinique des patients et pourraient conduire à changer les stratégies thérapeutiques poursuivies actuellement.
Atteintes cardiaques aiguës
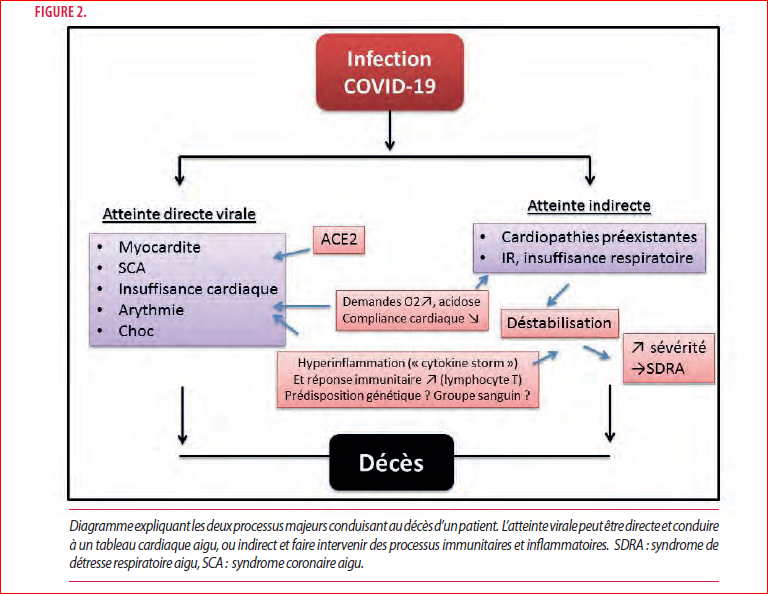
Dans le contexte du syndrome de détresse respiratoire aigu tel que vécu par 20% des patients, il est logique qu’un certain nombre développe des lésions cardiaques. Les atteintes cardiaques au décours de la maladie sont diverses et prennent parfois la forme d’une élévation isolée des marqueurs biologiques du dommage myocardique (troponine, CPK, CKMB), ou d’atteintes structurelles bien identifiables par les examens complémentaires. Au début de l’épidémie à Wuhan, sur les 41 premiers patients COVID + souffrant de pneumonie virale, les médecins ont relevé dans 12% des cas des probables lésions cardiaques aiguës (niveaux de troponine-HS>28pg/ml). Les complications les plus courantes de ces patients n’étaient toutefois pas cardiologiques. L’ARDS (29%), une virémie (15 %) étaient à l’avant plan. Sans être exclusif d’une atteinte cardiaque aigue, la troponine s’élève aussi dans l’insuffisance rénale. Or une baisse significative de la perfusion rénale est observée dans plus de 70% des patients admis aux S.I (16). Dans cette cohorte chinoise, un patient sur trois est admis aux S.I. Un taux de décès moyen de 15% est observé, en grande partie suites à des complications hémodynamiques, multi-organiques chez ceux qui avaient développé au départ une atteinte cardiaque (17). Ces observations ont également été rapportées lors de précédentes épidémies virales pulmonaires. L’origine de ces atteintes cardiaques est multifactorielle : inflammation généralisée et « vascularite », infection et conséquences hémodynamiques sévères qui s’en suivent comme le choc ou l’ARDS (Figure 2). Tant l’inflammation que ses conséquences peuvent causer une rupture de plaque d’athérome préexistante (-> thrombose coronaire aigue -> STEMI), ou une forte réduction de la perfusion coronaire en oxygène (-> ischémie sévère -> infarctus de type 2). Dans plusieurs rapports, dont une méta-analyse ne portant toutefois que sur 341 patients, le niveau de troponine I cardiaque était significativement plus élevé chez ceux qui présentaient une atteinte virale sévère et suggérait que ces patients se compliquaient d’un infarctus (en majorité de type 2) (18).
La recommandation principale est de garder à l’esprit qu’un bilan cardiologique doit être poussé le plus loin possible en présence de douleurs thoraciques évocatrices, d’altérations de l’ECG, ou échographiques. À l’inverse une élévation isolée des marqueurs biologiques du dommage cardiaque ne doit pas nécessairement conduire à des tests invasifs. Le tout est à interpréter dans le contexte clinique.
Myocardite
La myocardite est par définition une maladie inflammatoire du muscle cardiaque causée par l’infiltration au sein des myocytes de cellules « immunocompétentes ». Des autopsies de patients du COVID-19 ont révélé des infiltrations pulmonaires et myocardiques par des cellules inflammatoires mononucléaires, traduisant une attaque virale ou une intense réaction immunitaire déclenchée (19). La présence des récepteurs ACE- 2 au niveau cardiaque profitent au COVID-19 pour infester les cellules. Biologiquement, la myocardite se reflète par une augmentation des niveaux de biomarqueurs cardiaques comme déjà rappelé. Ce processus inflammatoire peut faire suite à tout type de lésion cardiaque. L’affection est de nature complexe et présente de multiples visages et étiologies dont des maladies infectieuses de tout bord (virales, bactériennes, mais aussi protozoaires, ou parfois fongiques…).
La myocardite aiguë est souvent le résultat non seulement d’une infection virale qui nécrose directement le myocarde mais aussi la conséquence comme décrit précédemment d’une réponse immunitaire excessive qui est à l’origine déclenchée par l’organisme pour éliminer l’agent infectieux. Actuellement pour le COVID-19 on ne connait pas le(s) mécanisme(s) qui conduisent à l’inflammation du cœur. Les entérovirus ont un tropisme direct pour les cardiomyocytes qu’ils « lysent » et sont impliqués par ce mécanisme dans des cas de myocardites fulminantes (20). Le COVID-19 pourrait infecter les cellules cardiaques de la même manière et les lyser secondairement après réplication de leur ARN. La découverte du virus dans les cardiomyocytes étaye cette hypothèse. D’autres virus comme le parvovirus B19 ciblent les cellules endothéliales vasculaires cardiaques. Le corona aurait des propriétés similaires comme expliqué précédemment. Les mécanismes pathogènes par lequel le B19 exerce son action sont multiples et peuvent impliquer une cytotoxicité directe sur les protéines cellulaires, une activation de l’interleukine-6 (IL-6), la production de facteurs de nécrose tumorale, ainsi que la stimulation d’un processus d’apoptose et d’autolyse. L’infection des cellules endothéliales est également associée à la chronicisation de la maladie, et plus tard au développement d’une cardiopathie dilatée, avec altération de fonction du ventricule gauche (VG). Les conséquences à long terme du COVID-19 ne sont évidemment pas encore évaluables mais on peut penser par les similitudes entre les 2 infections que certains patients ne sortiront pas indemne de leur myocardite. Des COVID-19 ont en effet présenté des formes de myocardites sévères avec altération aigue de la fonction du VG. Le diagnostic d’une myocardite quant à lui n’est pas aisé. L’aspect ECG le plus typique de la myocardite est généralement l’apparition de changements non spécifiques de l’onde T (ondes T négatives) comme on pourrait le voir dans le SCA ou l’hypertrophie ventriculaire gauche. D’autre part, des ECG de patients avec myocardite étaient similaires à ceux d’un STEMI, ou des patients développant un syndrome de Takotsubo. Les examens complémentaires aident à faire la différence. Dans la myocardite, des niveaux de troponine très élevés (>10.000ng/L), signent une atteinte cardiaque parfois fulminante. En ce qui concerne le pronostic, quelques décès de patients COVID-19 liés à ces myocardites sont rapportés, toutefois l’incidence semble heureusement faible voire anecdotique. Les implications thérapeutiques qui découlent de ces observations sont importantes. Sous support inotrope, des réanimateurs ont pu observer que certaines myocardites qui au départ prenaient une tournure foudroyante ont finalement vu une fin heureuse. Il a par ailleurs été rapporté des normalisations des paramètres hémodynamiques, de l’oxygénation, de la fonction cardiaque lors de l’administration de traitements modulants l’inflammation comme la méthylprednisolone (hautes doses jusque 200mg/jour), ou des immunoglobulines (20 g/jour) (21).
Syndrome coronaires aigu (SCA)
Une hypoxémie profonde associée à une tachycardie peut entraîner des douleurs thoraciques et des modifications électrocardiographiques évoquant une ischémie myocardique. Lorsque les biomarqueurs sont altérés, un infarctus du myocarde de type 2 peut être suggéré, et cette situation est fréquente aux S.I. En particulier, des données récentes en provenance de Chine suggèrent que les lésions myocardiques au cours d’une infection par COVID-19 - comme l’indiquent les taux élevés de troponine - représentent un indicateur puissant prédisant un risque plus élevé de complications et de décès. Les SCA de type STEMI déclenchés par le corona ne sont pas aussi fréquents qu’il n’y paraît. Nous n’avons connu qu’un cas isolé de STEMI co-associé à du COVID-19. Il s’agissait d’un homme de 68 ans hypertendu et diabétique de type 2, qui a été conduit aux urgences par sa famille pour altération de l’état général depuis une semaine avec dyspnée, toux sèche, frissons et confusion. La famille signale une notion de douleur thoracique droite il y a plusieurs jours. Le bilan d’admission diagnostique une pneumonie interstitielle bilatérale hypoxièmiante typique de l’origine virale à SARS-CoV2. L’ECG d’amission met en évidence un rythme sinusal régulier, toutefois tachycarde à 102 /min et un sus-décalage ST V2-V4 avec présence d’ondes Q, y compris dans le territoire inférieur signant un syndrome coronarien STEMI subaigu antérieur (Figure 3).
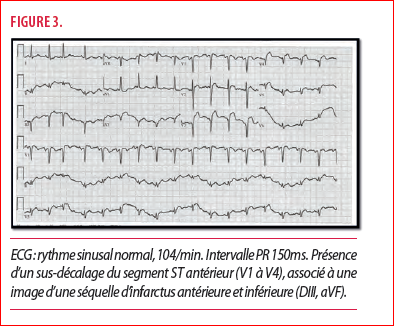
Le bilan angiographique de ce patient a montré une lésion subocclusive de l’IVA ayant bénéficié avec succès de l’implantation d’un stent (Figure 4).

L’échographie cardiaque transthoracique a montré une akinésie apicale et antérieure avec altération modérée de la fonction globale du ventricule gauche. Le patient nécessitera dans un premier temps un support ventilatoire non invasif et puis une intubation orotrachéale sera nécessaire quelques jours plus tard. Le pic de troponine était de 1571ng/m, celui des CK à 4.26μg/l. Même s’il est impossible rétrospectivement d’incriminer dans ce cas précis ce SCA à l’atteinte virale qui fut détectée peu de temps après, le lien entre le SCA et les patients COVID-19 est établi. Un SCA dans ce contexte s’explique par l’âge, les comorbidités, l’état respiratoire et hémodynamique, l’ARDS, et l’état de choc. Le processus inflammatoire est facteur déstabilisant des plaques d’athérome, et le tropisme du virus pour les cellules endothéliales vasculaires peut expliquer des thromboses aigues (Figure 5).

Plusieurs publications ont tenté de faire un cadastre des SCA. Sur 138 patients en majorité des hommes d’âge moyen de 56 ans (42-68 ans) hospitalisés à l’hôpital universitaire Zhongnan de Wuhan en Chine, 7% ont présenté un syndrome coronaire aigu (22). 26 % des patients ont dû être rapidement (dans un délai moyen d’un jour après admission) admis aux S.I. suite à l’apparition de complications, en majorité un ARDS (61.1%).
Plus de 70% parmi eux avaient des comorbidités et 1 sur 4 une maladie cardio-vasculaire préexistante. Une fois aux S.I., 22.2% de ces patients critiques ont présenté un SCA. Le niveau de troponine I était en moyenne de 11.0 pg/ml (5.6-26.4) comparé à la valeur de 6.4 pg/ml (2.8-18.5) pour les autres patients sans nécessité de soins aigus. Une telle observation rejoint une publication du Lancet de janvier 2020 où 12% des patients COVID hospitalisés étaient considérés comme compliqués d’une atteinte cardiaque comme en témoignait des niveaux de Troponine I élevés. Il n’y a pas de détails concernant la nature de cette atteinte. Dans cette même publication, il faut notifier également qu’aucun des patients n’a présenté de douleurs thoraciques à l’admission et que le symptôme cardinal était la dyspnée. Enfin, les médecins ont notifié ces atteintes myocardiques chez 1 patient sur 3 lorsqu’ils étaient admis aux S.I. (23).
D’autre part, cette pandémie a un impact négatif sur la prise en charge des SCA. En chine, comme en Italie il a été observé un délai ‘anormalement long’ dans la prise en charge tant de patients COVID-19 (+) ou (-) et présentant un tableau d’infarctus. Ce délai est parfois la conséquence d’une mauvaise perception par le patient de ses symptômes (délai allongé entre le début des symptômes et l’appel des secours) ou la crainte d’être hospitalisé dans un service où indubitablement il pourrait contracter le COVID-19. On constate également dans la majorité des centres une diminution des admissions pour SCA. La revascularisation rapide reste le traitement de choix du STEMI, même en présence d’une infection COVID-19 prouvée. Le recours à la fibrinolyse doit être réservé aux patients n’ayant pas accès à ce traitement de premier choix. Afin de permettre de poursuivre une telle activité, il a été recommandé aux services de réorganiser les salles d’urgence et de cathétérisme cardiaque. Le but étant d’adapter les procédures pour permettre aux patients COVID (+) ou suspects de l’être de bénéficier d’une revascularisation tout en garantissant à ceux qui sont testés négatifs pour le virus la sécurité de ne pas contracter le virus durant leur séjour hospitalier. Quant aux positifs, ces recommandations visent bien entendu à protéger le personnel soignant.
ECG et Troubles du rythme
L’infection du COVID-19 ne s’accompagne pas de modifications ECG typiques que l’on pourrait facilement détecter. Il n’existe pas d’arythmies cardiaques spécifiques de la maladie non plus, toutefois une certaine discordance entre la fréquence cardiaque et la température a été observée chez les patients atteints de COVID-19. La fréquence cardiaque semble chez certains être plus lente qu’attendu au vu des niveaux de température. Ce phénomène a également été observé dans d’autres maladies infectieuses telles que la fièvre typhoïde. Par ailleurs, une aggravation d’un trouble de conduction préexistant (nœud sinusal, bloc AV) peut se produire chez les patients atteints d’une infection COVID-19, en particulier en cas d’atteinte myocardique et de SCA. Chez les patients gravement malades dans l’unité de S.I., une bradycardie voire des asystolies transitoires par arrêt sinusal peuvent se produire lorsque le patient est placé en décubitus ventral. Ceci s’expliquerait par une augmentation transitoire du tonus vagal. Toutefois, l’hypoxémie peut jouer un rôle également. Il est reconnu que la « simple » grippe saisonnière (Influenza) est un important déclencheur de maladies cardiaques, d’hospitalisation, syndrome coronarien aigu, et en particulier d’arythmies ventriculaires sévères comme cela a été démontré e.a. chez des sujets appareillés de défibrillateurs (24). ARDS, choc et arythmies sont les trois principales complications des patients avec une pneumonie sévère due au COVID-19. Par arythmie, on entend toutes anomalies du rythme cardiaque, depuis la tachycardie sinusale du patient fiévreux ou choqué aux arythmies les plus sévères. Le risque rythmique du COVID ne diffère pas beaucoup des patients généralement admis dans des contextes de maladies sévères, en particulier pour la FA. Notre expérience le confirme. Nous vivons actuellement l’histoire d’un jeune patient qui fut admis en urgence en raison d’un syndrome grippal avec fièvre à 40°C, frissons et toux sèche et majoration progressive d’une dyspnée. Un CT thoracique réalisé d’emblée montre des opacités en verre dépoli prédominant dans le lobe inférieur gauche. L’évolution de ce patient a nécessité au départ une oxygénothérapie par Optiflow, par la suite une ventilation mécanique invasive (associé à un procubitus), un traitement par NO inhalé et finalement mise en place d’une ECMO. L’état hémodynamique du patient a nécessité l’usage de Noradrenaline. Durant son évolution, il a présenté plusieurs épisodes de FA, somme toute banales qui ont été facilement jugulés (Figure 6).

Mais l’expérience d’autres sur le terrain ont parfois été diamétralement opposée, avec des cas d’arythmies sévères et de morts subites. Les causes sont évidemment multiples : SCA, myocardite, troubles ioniques, troubles de l’oxygénation, etc. Ainsi, dans une étude du JAMA, une forte prévalence d’arythmies cardiaque a été observée (16.7%) chez des patients chinois atteints d’une pneumonie. L’état clinique précaire du patient est à nouveau un facteur de risque, en particulier lorsque son état nécessite un séjour aux S.I. (22.2% vs 6.9% non S.I.) (25). Comme déjà exposé, ces patients sont plus âgés, présentent plus co-morbidités et mais ont généralement des taux de D-dimères, CKMB et troponines majorés. Ceci n’est donc pas vraiment une surprise. Le détail des arythmies observées n’est pas spécifié, mais en se basant sur les précédentes épidémies virales, la fibrillation auriculaire et les arythmies ventriculaires sont les principales arythmies auxquelles on se trouve généralement confronté. Ces données indiquent aussi que les patients les plus sévèrement atteints par la pneumonie devraient précocement être mis sous monitoring. Par ailleurs, pour les patients les plus gravement touchés et présentant une instabilité hémodynamique due à une TV ou à une FA/flutter rapides, l’amiodarone par voie intraveineuse est le médicament antiarythmique de choix. Toutefois, il est préférable d’éviter sa combinaison avec l’hydroxychloroquine et l’azithromycine lorsque ces dernières sont utilisées.
Choc cardiogénique
Un SCA, une myocardite fulminante, une arythmie rapide non contrôlée comme une FA, une TV peuvent s’accompagner d’un choc cardiogénique (CC). Dans le contexte infectieux, l’origine du choc n’est pas toujours clairement définie. ECG, échographie cardiaques, monitoring hémodynamique invasifs sont des éléments qui seront apprécier à leur juste valeur pour aider au diagnostic. Le pronostic du CC reste dans la majorité des cas sombre.
Quelles considérations cardiaques lors de traitements pharmacologiques du COVID-19
Certains médecins privilégient les traitements « supportifs » (oxygénothérapie, traitements antibiotiques si doute sur une surinfection bactérienne) car en l’absence de vaccin, les traitements « curatifs » du COVID-19 sont actuellement tous expérimentaux, parfois donnés à titre compassionnel comme le remdesivir (inhibiteur viral) de Gilead Sciences (CA, USA) ou en off-label comme l’hydroxychloroquine. Cette dernière a vu son usage dans le COVID acceptée depuis le 28 mars par l’Emergency Use Autorisation. À l’heure d’aujourd’hui l’efficacité de la plupart de ceux-ci n’est pas toujours connue, il y a urgence sanitaire mais cela ne doit pas enlever la rigueur avec laquelle les investigations sont menées. Annonces et contre-annonces dans la presse sur l’effet ou non de ces molécules en dit long sur les batailles commerciales qui se jouent en coulisse. Pour exemple, le jeudi 23 avril fera date. « Par erreur » une déléguée de l’OMS a laissé entendre sur le site web de l’agence que le remdesivir ne serait pas efficace. L’information reprise par le Financial Times conduit en quelques secondes l’action de GILIEAD cotée au Nasdaq dans une chute sans précédent, et affole le reste des marchés. Car le monde économique n’est pas prêt à poursuivre un long confinement et avait mis beaucoup d’espoir dans la molécule pour en sortir. En dehors de ces considérations, l’évidence est que certaines substances peuvent avoir des conséquences cardiaques sévères et qu’il est important de connaître car même des sujets indemnes de tous commémoratifs cardio-vasculaires peuvent en souffrir.
Usage de l’hydroxychloroquine et l’Azithromycine
À l’heure actuelle, il est supposé que certains médicaments utilisés dans la prophylaxie du paludisme comme l’hydroxychloroquine, soient efficaces dans le traitement de l’infection par le SRAS-CoV-2. Selon le baromètre publié par SERMO (société de sondage), l’utilisation de l’hydroxychloroquine fait partie des médicaments les plus prescrit (analgésiques, azithromycine) dans la maladie, par exemple elle serait donnée dans 72% des cas COVID en Espagne, 49% en Italie, 23% des cas en France (26). Prouvé in vitro, l’hydroxychloroquine serait efficace sur le COVID-19 via des effets sur le pH endosomal et la glycosylation des récepteurs de l’enzyme de conversion de l’angiotensine 2 qui sont nécessaires à l’entrée du virus dans la cellule. Le traitement est administré avant même d’avoir les preuves cliniques de son efficacité. La revue Prescrire quant à elle soulève le scepticisme grandissant qui entoure ce traitement et les effets secondaires potentiellement sévères causés par ces molécules. La substance possède des propriétés d’inhibition des canaux sodiques, potassiques repolarisants et est inotrope négative. Un traitement chronique peut provoquer des cardiopathies, avec altération des fonctions du VG, des troubles de la conduction avec bradycardie. En aigu, la molécule peut également allonger l’espace QT et être la cause de Torsades de Pointes. Le seuil de 500ms pour l’espace QT serait atteint dans 11% des cas et 12% des patients présenteraient un allongement du QT de plus de 60ms selon une étude non « peer reviewed » portant sur 84 patients du NYU Longone medical center. Selon l’ANSM en France, le centre de pharmacovigilance de l’hexagone a déjà rapporté depuis mars une centaine de cas avec effets secondaires variés. Une deuxième enquête a été mise sur pied, et a rapporté 43 cas graves sous hydroxychloroquine seule ou en association, dont 7 décès par mort subite sans parler des syncopes, rythmiques causées par un allongement excessif du QT (27). L’azithromycine, antibiotique largement utilisé, est aussi utilisé dans le COVID-19 mais est aussi reconnue comme une cause pharmacologique d’allongement de l’intervalle QT, d’arythmies graves et de risque accru de mort subite. La substance pourrait être utilisée seule sans monitoring ECG. Associée à l’hydroxychloroquine, comme prôné en France par le Prof. Didier Raoult, la bi-thérapie a été utilisée chez des patients avec semble-t-il plus de succès. Manipuler ces substances en minimisant les dangers est possible, mais une mesure adéquate du QT est nécessaire en utilisant la tangente (Figure 7). LE QT doit par ailleurs être corrigé pour la fréquence selon la formule de Bazett.

Il est utile de rappeler que l’âge, le sexe féminin, des troubles ioniques, de l’insuffisance rénale mais aussi la combinaison de divers produits majorant le QT sont des facteurs de risque pour les torsades de pointes. La prudence est donc de mise comme rappelé par la majorité des sociétés savantes de cardiologie qui ont édités des règles concernant la sécurité du traitement par hydroxychloroquine et la surveillance à mettre en œuvre pour réduire les risques de complications cardiaques (Figure 8).

Lopinavir/Ritonavir
Le lopinavir est un inhibiteur de protéase développé initialement pour traiter le VIH. Il est souvent associé au ritonavir, qui prolonge sa demi-vie plasmatique. Pour lutter contre le COVID-19, la molécule a été évaluée dans le cadre de petits essais dont un contrôlé randomisé sur 199 patients qui s’est révélé être négatif. Les effets indésirables gastro-intestinaux, notamment les nausées, les vomissements et la diarrhée, étaient fréquents (environ 50%) dans le groupe lopinavir-ritonavir, toutefois les auteurs ne mentionnaient ni d’allongement du QT ni d’autre toxicité cardiaque particulière (28).
Le Redemsivir
Un essai sur 61 patients répartis dans divers centres dans le monde avec cette molécule donnée à titre compassionnel a été récemment publié (29). Non randomisée, sans groupe contrôle, le traitement a permis une amélioration clinique significative dans 68% des cas. La molécule se veut prometteuse, mais son innocuité cardiaque n’est pas connue. Sur cette première série de patients, aucun événement majeur n’a été rapporté, toutefois 60% des patients (essentiellement les intubés) présentaient des effets secondaires dont de l’hypotension.
Autres substances
De nombreuses substances sont à l’étude à travers le monde. Les principaux médicaments disposant d’un potentiel attrait thérapeutique dans le COVID-19 sont les suivants : le favipiravir, la ribavirine, le sarilumab et le baricitinib. Les données actuelles sont trop limitées pour établir des recommandations sur d’éventuels risques cardiaques et en particulier rythmiques.
Conclusion
Apparue en décembre 2019, les infections COVID 19 se sont rapidement répandues dans le monde créant une nouvelle pandémie. Si les complications respiratoires dominent souvent le tableau clinique et sont liées à une mortalité non négligeable, ce virus a des implications cardio-vasculaires (CV) importantes à connaître. Les patients présentant des facteurs de risque CV, notamment le sexe masculin, l’âge avancé, le diabète, l’hypertension et l’obésité, ainsi que les patients souffrant de maladies CV et cérébrovasculaires avérées, ont été identifiés comme des populations particulièrement vulnérables avec une morbidité et une mortalité accrues lorsqu’ils souffrent du COVID-19. Les infections par COVID-19 sont associées à une augmentation des niveaux de biomarqueurs cardiaques due à des atteintes myocardiques. Des autopsies de patients atteints de l’infection ont révélé une infiltration du myocarde par des cellules inflammatoires mononucléaires interstitielles. Même s’il n’existe pas à l’heure actuelle de traitement ayant prouvé son efficacité pour combattre le virus, plusieurs substances comme l’hydroxychloroquine sont utilisées et peuvent aussi avoir des répercussions sur le rythme cardiaque et être responsable d’arythmies létales.
Affiliations
Service de cardiologie, Cliniques universitaires Saint-Luc, B-1200 Woluwe-Saint-Lambert.
Correspondance
Pr. Christophe Scavée
Cliniques Universitaires Saint-Luc
Service de cardiologie
Avenue Hippocrate 10
B-1200 Woluwe-Saint-Lambert.
christophe.scavee@uclouvain.be
Références
- Lu R, Zhao X, Li J et al. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. Lancet. 2020; doi:10.1016/S0140-6736(20)30251-8.
- Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72314 Cases From the Chinese Center for Disease Control and Prevention. JAMA. 2020.
- Drosten C, Günther S, Preiser W, et al. Identification of a novel coronavirus in patients with severe acute respiratory syndrome. N Engl J Med. 2003;348:1967-1976
- http://www.who.int/emergencies/mers-cov/en/.
- Novel Coronavirus Pneumonia Emergency Response Epidemiology T. [The epidemiological characteristics of an outbreak of 2019 novel coronavirus diseases (COVID-19) in China]. Zhonghua Liu Xing Bing Xue Za Zhi. 2020;41(2):145-151.
- https://www.who.int/docs/default-source/coronaviruse/situation-reports/2....
- Gao H-N, Lu H-Z, Cao B, Shang H et al. Clinical Findings in 111 Cases of Influenza A (H7N9) Virus Infection. N Engl J Med. 2013; 368:2277-2285. DOI: 10.1056/NEJMoa1305584.
- Badawi A, Ryoo S et al. Prevalence of comorbidities in the Middle East respiratory syndrome coronavirus (MERS-CoV): a systematic review and meta-analysis. Int J Infect.Dis. 2016 ; 49, 129–133.
- Huang C, Li X, Zhao J et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020; 395: 497–506.
- Guan WJ, Ni ZY, Hu Y, et al; China Medical Treatment Expert Group for COVID-19. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020. doi:10.1056/NEJMoa2002032.
- McMichael M, Currie D, Clark S, Pogosjans S, Kay M; et al. Epidemiology of COVID-19 in a Long-Term Care Facility in King County, Washington. N Engl J Med. 2020. DOI: 10.1056/NEJMoa2005412.
- Bhatraju P, Ghassemieh B, Michelle Nichols M, Kim R et al. COVID-19 in Critically Ill Patients in the Seattle Region. N Engl J Med. 2020. DOI: 10.1056/NEJMoa2004500.
- Mao L, Wang M, Chen S, He Q, Chang J, Hong C, et al. Neurological Manifestations of Hospitalized Patients with COVID-19 in Wuhan, China: a retrospective case series study. 2020:2020.02.22.20026500.
- CAPACITY-COVID : a European registry to determine the role of cardiovascular disease in the COVID-19 pandemic. Eur Heart J. 2020; 0, 1–2 doi:10.1093/eurheartj/ehaa280
- Varga Z, Flammer A, Steiger P et al. Endothelial cell infection and endotheliitis in COVID-19. Lancet 2020. doi.org/10.1016/S0140-6736(20)30937-5.
- Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020;395(10223):497-506. doi:10.1016/S0140-6736(20)30183-5.
- Huang, C. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020; 395, 497–506.
- Lippi G, Lavie CJ, Sanchis-Gomar F. Cardiac troponin I in patients with coronavirus disease 2019 (COVID-19): Evidence from a meta-analysis. Prog Cardiovasc Dis. 2020.
- Xu Z, Shi L, Wang Y, Zhang J, Huang L, Zhang C et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020.
- Chow LH, Beisel KW, McManus BM. Enteroviral infection of mice with severe combined immunodeficiency. Evidence for direct viral pathogenesis of myocardial injury. Lab Invest. 1992;66:24–31.
- Hongde Hu, Fenglian Ma, XinWei, Yuan Fang. Coronavirus fulminant myocarditis treated with glucocorticoid and human immunoglobulin. doi:10.1093/eurheartj/ehaa190
- Wang D, Hu B, Hu C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirusinfected pneumonia in Wuhan, China. JAMA. February 2020. DOI: 10.1001/jama.2020.1585.
- Huang, C. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 395, 497–506 (2020).
- Madjid M, Connolly AT, Nabutovsky Y, et al. Effect of high influenza activity on risk of ventricular arrhythmias requiring therapy in patients with implantable cardiac defibrillators and cardiac resynchronization therapy defibrillators. Am J Cardiol. 2019;124(1):44-50. doi:10.1016/j.amjcard.2019.04.011.
- Wang D, Hu B, Hu C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020. doi:10.1001/jama.2020.1585
- Consulté le 21/04/20 sur le site https://www.businesswire.com/news/home/20200402005460/en
- https://ansm.sante.fr/afssaps/S-informer/Actualite/Medicaments-utilises-....
- Cao B, Wang Y, Wen D, Liu W et al. A Trial of Lopinavir-Ritonavir in Adults Hospitalized with Severe COVID-19. N Engl J Med. 2020. DOI: 10.1056/NEJMoa2001282.
- Grein J, Shin D, Diaz E et al. Compassionate Use of Remdesivir for Patients with Severe COVID-19 DOI: 10.1056/NEJMoa2007016.