Prothèse Totale de Hanche : modifications de nos habitudes ancestrales grâce à la chirurgie mini-invasive
Pierre Pirlot, Gautier Beckers, Jean-Emile Dubuc, Olivier Cornu, Maïte Van Cauter
Actuellement, en Belgique, environ 30.000 prothèses totales de hanche (PTH) sont implantées par an (1).
Suite au vieillissement de la population et l’accroissement de la population, les coûts liés à la santé publique sont de plus en plus élevés. Aujourd’hui, 80 % des interventions chirurgicales peuvent suivre un « parcours standardisé », ce qui a induit l’établissement de forfaitisation (durée d’hospitalisation, coût forfaitaire, …). Depuis 2019, les implants utilisés en arthroplastie de hanche sont également soumis à un plafond de remboursement. L’impact financier fait donc partie de notre quotidien et doit être pris en compte par le chirurgien.
L’essor de la chirurgie mini-invasive pour les PTH ainsi que l’établissement d’un protocole « Optimal Recovery » aux seins des Cliniques Universitaires Saint Luc a permis de réduire les complications post-opératoires ainsi que la durée de séjour hospitalier (2-3). Historiquement, le post-opératoire comprenait un contrôle biologique systématique à J2 et J5. Actuellement, la plupart des patients ayant regagné le domicile avant le J5, ce contrôle ne se réalise plus. Il est à noter que 8% de nos patients quittent l’hôpital le lendemain de l’intervention chirurgical.
Grâce à la chirurgie mini-invasive et dans ce contexte toujours plus présent de forfaitisation, il est donc judicieux de se poser la question si le contrôle sanguin post-opératoire doit rester systématique (Figure 1) ?
Le coût de l’analyse sanguine post-opératoire est d’environ 40 euros. Entre 2015 et 2020, nous avons revu plus de 1000 dossiers de patients opérés d’une PTH dans un contexte de coxarthrose primaire. Nos résultats montrent que moins de 3 % des patients nécessitent une transfusion en post-opératoire. Cette étude a permis d’identifier les différents facteurs de risque pouvant amener à une perte sanguine accrue et par conséquent, la nécessité d’une transfusion. : il s’agit d’un âge avancé, d’un score ASA supérieur ou égal à 2, de la préexistence d’une hypertension artérielle, de l’ostéonécrose fémorale proximale comme indication de l’arthroplastie, du sexe féminin et d’une hémoglobine préopératoire basse.
Un score (THABUS pour Total Hip Arthroplasty Blood test Usefulness Score) a été établi pour identifier les patients nécessitant ou pas un suivi biologique en post-opératoire immédiat. Il est accessible à l’adresse suivante : www.thabus.com.Ce score nécessitera une validation clinique prospective avant d’être utilisé largement dans la pratique quotidienne. Une mesure simple pour tenter de prévenir ce risque transfusionnel serait de corriger préalablement à la chirurgie les anémies (supplémentation martiale et acide folique, traitement à l’érythropoïétine).
Références
- INAMI. Belgian Hip and Knee Arthroplasty Registry. Annual Report 2018 https://www.ehealth.fgov.be/file/view/AXDOTDE0mTlaOSp4Nmeq?filename=Orth...
- Moerenhout KG , Cherix S, Rudiger HA (2012). ‘Prothèse totale de la hanche par voie antérieure «mini-invasive». Rev Med Suisse. 2012; Vol. 2. no.367, p. 2429 – 2432.
- Van Cauter M, Dubuc JE, Yombi JC, Cornu O. « Optimal Recovery » et prothèse totale de hanche bilatérale. Louvain Med. 2018 ; 137 (2) : 74-75 .
Prothèse totale de genou idéale, la quête se poursuit !
Loïc Thoreau, Daniel Morcillo Marfil, Emmanuël Thienpont
La prise en charge de la gonarthrose par prothèse totale de genou (PTG) reste controversée dans l’opinion publique avec des scores cliniques rapportant jusqu’à 20 pc de patient insatisfaits. Comparativement aux bénéfices obtenus après une prothèse totale de hanche (PTH), ces résultats sont insuffisants (1). La réduction de cette proportion constitue un objectif majeur pour la communauté orthopédique moderne.
De plus en plus, la réflexion s’oriente vers des stratégies de resurfaçage respectant l’anatomie individuelle du patient (2). Ce changement de paradigme est soutenu par la technologie moderne qui a permis le développement de robots (3) et d’implants sur mesures (4-5). Notre équipe a rapidement embrassé cette philosophie de resurfaçage et s’est montrée pionnière en la matière avec l’utilisation du robot (ROSA) et d’implants custom made dès l’apparition, en Belgique, de ces technologies.
Présents aux prémices de cette (r-)évolution, nous sommes en mesure de dégager les premiers résultats de ces techniques qui s’annoncent particulièrement encourageante avec des scores cliniques d’ores et déjà améliorés à court terme.
La quête de la prothèse idéale se poursuit avec l’espoir de la confirmation de ces résultats prometteurs à l’avenir. Par ailleurs l’enthousiasme de la communauté orthopédique autour de cette problématique et la volonté constante des chirurgiens d’améliorer la fonction de leurs patients restent les marqueurs tangibles d’une avancée déterminante à venir.
Références
- Thienpont E, Vanden Berghe A, Schwab PE, Forthomme JP, Cornu O. Joint awareness in osteoarthritis of the hip and knee evaluated with the ‘Forgotten Joint’ Score before and after joint replacement. Knee Surg Sports Traumatol Arthrosc. 2016;24(10):3346-3351.
- Thienpont E, Klasan A. The dissatisfied total knee arthroplasty patient. New technologies-the white knight in shining armor coming to their rescue? Arch Orthop Trauma Surg. 2021;141(12):2021-2025.
- Batailler C, Hannouche D, Benazzo F, Parratte S. Concepts and techniques of a new robotically assisted technique for total knee arthroplasty: the ROSA knee system. Arch Orthop Trauma Surg. 2021;141(12):2049-2058.
- Beckmann J, Meier MK, Benignus C, Hecker A, Thienpont E. Contemporary knee arthroplasty: one fits all or time for diversity? Arch Orthop Trauma Surg. 2021;141(12):2185-2194.
- Brinkmann EJ, Fitz W. Custom total knee: understanding the indication and process. Arch Orthop Trauma Surg. 2021 Dec;141(12):2205-2216.
Place de la chirurgie en 1 temps et de l’antibiothérapie suppressive dans la prise en charge des infections d’implants orthopédiques
Pierre-Philippe Guilmot, Hervé Poilvache, Maïte Van Cauter, Jean-Cyr Yombi, Olivier Cornu
Un nombre important d’implants articulaires sont posés chaque année en Belgique (plus de 60.000 rien que pour la hanche et le genou) (1). De l’ordre de 2% des implantations (environ 1200/an) vont malheureusement s’accompagner d’une infection bactérienne. La maitrise de cette complication requière une approche multidisciplinaire, combinant un traitement chirurgical de débridement et un traitement antibiotique. L’approche thérapeutique se décline selon le délai entre le moment de la contamination et l’expression clinique de l’infection, du profil de la bactérie responsable de cette infection et de sa susceptibilité aux antibiotiques (l’identification préalable du microorganisme par ponction articulaire ou biopsie chirurgicale constitue dès lors encore et toujours une pierre angulaire de la prise de décision), des co-morbidités générales et locales que présente le patient, de l’état des tissus mous environnants, et particulièrement de la présence d’abcès ou de fistules productives, compliquant l’approche chirurgicale, et, enfin, de la complexité à extraire l’implant en place et à assurer une reconstruction fonctionnelle.
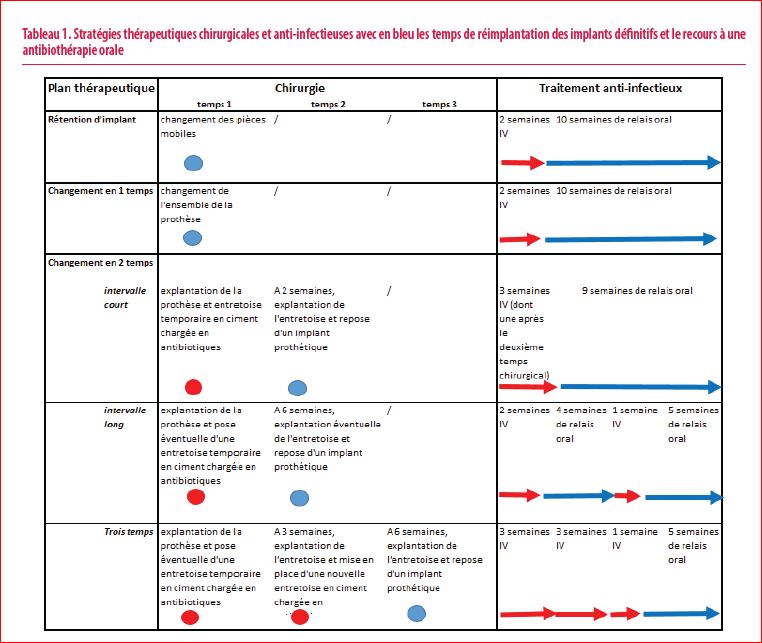
Traditionnellement, le plan thérapeutique identifiait 3 approches, avec trois variantes pour la troisième (Tableau 1) (2). La stratégie avec rétention d’implant était habituellement appliquée dans les infections postopératoires précoces (moins de 3 semaines) et dans les infections hématogènes, prises en charge rapidement, la chirurgie de révision en 1 temps préférée chez des patients peu susceptibles de supporter des chirurgies répétées et la chirurgie en 2 temps privilégiée dans tous les autres cas avec pour objectif d’assainir le foyer infectieux avant de remettre un implant prothétique de manière durable.
La qualité de l’identification microbiologique et l’amélioration des prises en charge dans un contexte multidisciplinaire avec des chirurgiens entraînés au débridement permet d’entrevoir une extension des indications de la chirurgie en 1 temps. Le dogme du deux temps est d’avoir éradiqué l’infection en l’absence de tout corps étranger mais implique pourtant l’implantation d’un corps étranger sous la forme d’une entretoise en ciment chargée d’antibiotiques pour faciliter le deuxième temps de reprise. L’idée a dès lors germé de réaliser une reprise complète en un temps en y associant le principe du deux temps : deux chirurgies séparées le même jour, permettant le recours à un champ opératoire non contaminé pour le temps de reconstruction mais également l’utilisation de systèmes de libération d’antibiotiques, comme des allogreffes, dans la zone opératoire (3).
Cette approche, si elle dispose, à priori, d’un résultat légèrement inférieur à une stratégie traditionnelle en 2 temps sur le plan du contrôle de l’infection, offre un meilleur résultat fonctionnel (4). Il semble aussi qu’elle expose moins aux super-infections avec des germes multi-résistants, sélectionnés par la pression antibiotique.
Toute stratégie comporte un taux d’échec, particulièrement quand l’implant est maintenu en place (stratégie avec rétention d’implant), que le débridement ne peut être conduit de manière optimale et complète, ou que l’antibiothérapie est sub-optimale par résistance microbienne, intolérance ou faible pénétration du biofilm bactérien de la molécule antibiotique choisie. Certains facteurs peuvent également aisément justifier de ces échecs : le délai entre la contamination et la prise en charge peut être plus long que celui idéalement recommandé, le patient présenté une moins bonne défense immunitaire. La stratégie envisagée peut également être remise en question par le patient, pour des raisons qui lui sont propres, ou par l’anesthésiste car le patient présente un risque chirurgical disproportionné, ou encore par le chirurgien fac à une difficulté technique.
Face à ces risques accrus d’échec, dans les cas où les approches classiques ont paru dépassées ou dans ces situations où la stratégie thérapeutique ne peut être conduite en adéquation avec les recommandations scientifiques, des approches non conformes ont été dérivées, comme l’instauration d’une antibiothérapie suppressive jusqu’au terme de la vie de l’implant. Il s’agit d’une stratégie non curative avec pour objectif de réduire les symptômes de l’infection et/ou de retarder et/ou prévenir la progression de l’infection et le descellement de l’implant. La décision d’introduire un tel traitement ne doit pas être prise à la légère. Ce traitement antibiotique au long cours est susceptible d’induire de la résistance bactérienne mais aussi de conduire à une toxicité pour le patient. La décision doit donc être soigneusement pesée et prise collégialement de manière multidisciplinaire. Cers situations peu fréquentes sont observées dans 5 à 14% des cas (5-7) et jusqu’à 36% des patients âgés de plus de 80 ans (8). Elle n’est possible que si l’infection est microbiologiquement documentée et si le traitement anti-infectieux par voie orale prolongée est envisageable, moyennant un suivi de la tolérance. Le taux d’échec de cette approche initialement extrêmement élevé (5) s’est amélioré avec l’approche multidisciplinaire et l’application stricte des critères précités (8) avec un maintien d’un implant fonctionnel dans 83% des cas. La tolérance au long cours reste un point d’attention important (9) et semble plus favorable si un traitement par cyclines est envisageable (10). L’arrêt du traitement suppressif est malheureusement associé de manière régulière à la récidive de l’infection et il convient de ne l’interrompre que si l’implant vient à être changé.
Références
- Orthopride report 2018, https://www.ehealth.fgov.be/file/view/AXDOTDE0mTlaOSp4Nmeq?filename=Orth...
- Izakovicova P, Borens O, Trampuz A. Periprosthetic joint infection: current concepts and outlook. EFORT Open Rev. 2019 Jul 29;4(7):482-494. doi: 10.1302/2058-5241.4.180092. PMID: 31423332; PMCID: PMC6667982.
- Winkler H, Stoiber A, Kaudela K, Winter F, Menschik F. One stage uncemented revision of infected total hip replacement using cancellous allograft bone impregnated with antibiotics. J Bone Joint Surg Br. 2008 Dec;90(12):1580-4. doi: 10.1302/0301-620X.90B12.20742. PMID: 19043128.
- Jenny JY, Barbe B, Gaudias J, Boeri C, Argenson JN. High infection control rate and function after routine one-stage exchange for chronically infected TKA. Clin Orthop Relat Res. 2013 Jan;471(1):238-43. doi: 10.1007/s11999-012-2480-7. PMID: 22798139; PMCID: PMC3528934.
- Goulet JA, Pellicci PM, Brause BD, Salvati EM. Prolonged suppression of infection in total hip arthroplasty. J Arthroplasty. 1988;3(2):109-16. doi: 10.1016/s0883-5403(88)80075-5. PMID: 3397740.
- Segreti J, Nelson JA, Trenholme GM. Prolonged suppressive antibiotic therapy for infected orthopedic prostheses. Clin Infect Dis. 1998 Oct;27(4):711-3. doi: 10.1086/514951. PMID: 9798021.
- Sandiford NA, Hutt JR, Kendoff DO, Mitchell PA, Citak M, Granger L. Prolonged suppressive antibiotic therapy is successful in the management of prosthetic joint infection. Eur J Orthop Surg Traumatol. 2020 Feb;30(2):313-321. doi: 10.1007/s00590-019-02559-4. Epub 2019 Oct 1. PMID: 31578679.
- Prendki V, Zeller V, Passeron D, Desplaces N, Mamoudy P, Stirnemann J, Marmor S, Ziza JM. Outcome of patients over 80 years of age on prolonged suppressive antibiotic therapy for at least 6 months for prosthetic joint infection. Int J Infect Dis. 2014 Dec;29:184-9. doi: 10.1016/j.ijid.2014.09.012. Epub 2014 Oct 30. PMID: 25447723.
- Wouthuyzen-Bakker M, Nijman JM, Kampinga GA, van Assen S, Jutte PC. Efficacy Antibiotic Suppressive Therapy in Patients with a Prosthetic Joint Infection. J Bone Jt Infect. 2017 Jan 15;2(2):77-83. doi: 10.7150/jbji.17353. PMID: 28529867; PMCID: PMC5423578.
- Pradier M, Robineau O, Boucher A, Titecat M, Blondiaux N, Valette M, Loïez C, Beltrand E, Nguyen S, Dézeque H, Migaud H, Senneville E. Suppressive antibiotic therapy with oral tetracyclines for prosthetic joint infections: a retrospective study of 78 patients. Infection. 2018 Feb;46(1):39-47. doi: 10.1007/s15010-017-1077-1. Epub 2017 Oct 20. PMID: 29052797.
Les arthroscopies d’épaule en décubitus dorsal
Maxime Bonnelance, Xavier Libouton, Olivier Barbier
La position optimale des patients qui bénéficient d’arthroscopies de l’épaule reste controversée. En effet, les deux méthodes les plus couramment utilisées sont la position semi-assise et le décubitus latéral, ayant toutes les deux leurs avantages et inconvénients (1). L’installation en décubitus dorsal est une 3e alternative plus récente que nous détaillerons pour en souligner l’intérêt.
La position en décubitus latéral permet une traction statique en flexion abduction du membre, permettant une bonne exposition des structures articulaires (labrum, longue portion du biceps (LHPB), …). Elle présente toutefois un risque accru de lésion du plexus brachial ainsi qu’un inconfort pour le patient lors des procédures pratiquées uniquement en anesthésie loco-régionale (2). La conversion vers la voie ouverte reste aussi une étape compliquée dans cette installation.
La position semi-assise, largement la plus utilisée, permet un positionnement dynamique du membre supérieur, ainsi qu’une conversion en voie ouverte aisée. Mais son inconvénient reste le risque cérébral accru lié aux hypotensions prolongées afin de mieux contrôler les saignements per procéduraux, pouvant occasionner des lésions allant de l’ophtalmoplégie à des atteintes cérébrales étendues sur ischémie (3,4). Malgré son utilisation majoritaire, cette position semi-assisse reste peu appréciée des anesthésistes surtout pour les interventions se prolongeant. Un nouveau positionnement chirurgical minimisant ces risques de perfusion cérébrale est donc d’un intérêt certain
Le choix de la position chirurgicale est le plus souvent dépendant de l’expérience du chirurgien. En effet, de nombreux chirurgiens pratiquent leur réparation de coiffe en position semi-assise, et leur réparation labrale en décubitus latéral.
Récemment, une 3ième position chirurgicale en décubitus dorsal a été décrite par Iamsumang and Chernchujit en 2016 (5). Elle permet de réaliser toutes les procédures arthroscopiques dans cette position en combinant les avantages et minimisant les inconvénients liés aux autres positions.
L’objectif de cet article est donc de décrire de manière pratique cette nouvelle position que nous avons dorénavant adopté.
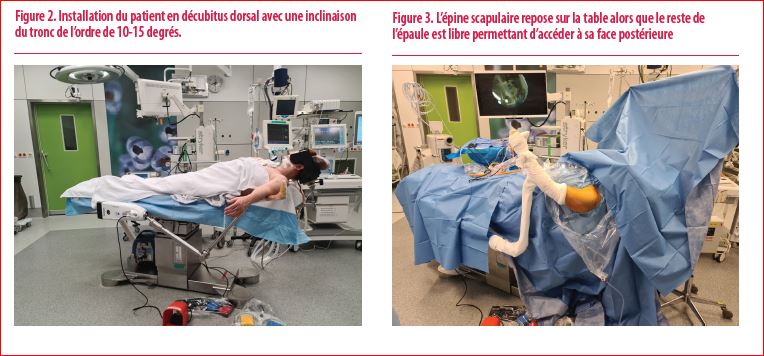
Le patient est positionné sur une table classique « épaule », équipée d’une têtière en « U ». Si elle se pratique sous anesthésie générale, la mise en place d’un masque laryngé est possible. La partie supérieure de la table est légèrement relevée, de l’ordre de 10 -15° (Figure 2), elle peut être inclinée d’avantage durant les procédures de Bankart, rendant la porte postérieure plus accessible.
Afin de permettre un maximum d’amplitude avec les instruments, l’accès à la face postérieure de l’épaule est très important : il faudra veiller à ce que, médialement, l’épine scapulaire repose sur la table et que le reste de l’épaule soit libre (Figure 3), appui postérieur de la table épaule ôté.
Le membre supérieur est champé stérilement dans sa totalité et fixé à un positionneur articulé (Spider 2, Smith&Nephew). Il permettra de maintenir le membre dans la position désirée durant toute l’intervention : Abduction, flexion et rotations sont contrôlées.
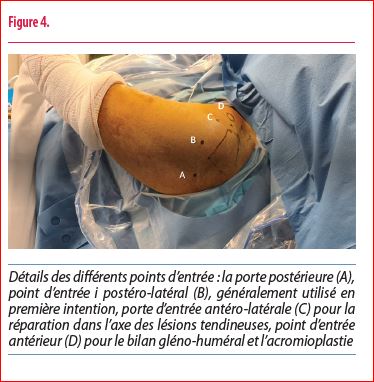
Lors d’une réparation de coiffe arthroscopique, le point d’entrée initial est postéro-latéral (Figure 4, B), l’arthroscope est inséré dans l’espace sous-acromial, une légère anté-élévation et traction sur le membre est appliqué avec le positionneur, afin d’ouvrir cet espace. Cette position permettra de visualiser directement la lésion de coiffe. Il faudra maintenir l’arthroscope positionné à 90° par rapport au bras opéré (les images ainsi que les gestes réalisés seront donc différents de 90°).
Le bilan gléno-huméral (glène, LHBP...) est réalisé directement par la lésion de coiffe, il a l’avantage de ne pas traumatiser la coiffe postérieure lors d’un bilan classique intra-articulaire via la porte postérieure (Figure 4, A).
La voie instrumentale est alors réalisée antérieurement (Figure 4, D), dans l’espace classique de l’intervalle des rotateurs. Une bursectomie classique, ainsi qu’une libération du tendon supra-épineux et du ligament coraco-acromial, sont réalisées.
Si nécessaire, une ténotomie/ténodèse du LHBP est pratiquée.
Après visualisation et nettoyage de la lésion tendineuse, une porte d’entrée antéro-latérale (Figure 4, C) est réalisée afin de manipuler les implants transosseux dans l’axe de la lésion tendineuse. Une acromioplastie est réalisée en fin d’intervention, ainsi qu’une résection acromio-claviculaire si nécessaire, via la porte initiale antérieure (Figure 4, D).
Des portes supplémentaires peuvent être réalisées en fonction du type de suture utilisé.
Dans notre institution, toutes les arthroscopies d’épaule sont dorénavant réalisées en décubitus dorsal. Les deux compartiments sont accessibles aisément, mais nous essayons dans cette intervention de suture de coiffe de travailler exclusivement dans le compartiment sous-acromiale, afin de minimiser les dommages à la coiffe postérieure. De plus, cette position permet une conversion en voie ouverte aisée.
Les avantages principaux sont un gain de temps dans l’installation du patient, et une position plus confortable pour le patient si une anesthésie loco-régionale est réalisée exclusivement.
Du point de vue anesthésique, les avantages résident dans des risques cérébraux minimisés, un maintien tensionnel plus stable, ainsi qu’un accès aux voies respiratoires supérieures rapide et aisé.
Du point de vue de l’opérateur, l’étape principale est l’apprentissage des techniques arthroscopiques classiques avec une orientation de caméra différente. L’utilisation d’un positionneur dynamique facilite les procédures, une traction statique plus conventionnelle peut être utilisée aussi.
Les principales astuces sont résumées dans le tableau 2.

Références
Jorge R, Familiari F, Bitzer A, Srikumaran U, Papalia R, et McFarland EG. « Patient Positioning in Shoulder Arthroscopy: Which Is Best? » Joints. 2019;7, (no 2): 46-55. https://doi.org/10.1055/s-0039-1697606.
Peruto CM, Ciccotti MG et Cohen SB. « Shoulder Arthroscopy Positioning: Lateral Decubitus versus Beach Chair ». Arthroscopy : The Journal of Arthroscopic & Related Surgery : Official Publication of the Arthroscopy Association of North America and the International Arthroscopy Association. 2009; 25, no 8. https://doi.org/10.1016/j.arthro.2008.10.003.
Murphy GS, Greenberg SB, et Szokol JW. « Safety of Beach Chair Position Shoulder Surgery: A Review of the Current Literature ». Anesthesia & Analgesia. 2019; 129, no 1: 101-18. https://doi.org/10.1213/ANE.0000000000004133.
Dane S, Sears BW, Aghdasi B, Only A, Francois A, Tonino P, et Marra G. « Cerebral Desaturation Events during Shoulder Arthroscopy in the Beach Chair Position: Patient Risk Factors and Neurocognitive Effects ». Journal of Shoulder and Elbow Surgery. 2013; 22, no 9: 1228-35. https://doi.org/10.1016/j.jse.2012.12.036.
Chonlathan I, et Chernchujit B. « The Supine Position for Shoulder Arthroscopy ». Arthroscopy Techniques. 2016; 5, no 5: e1117-20. https://doi.org/10.1016/j.eats.2016.06.002.
Affiliations
Cliniques universitaires Saint-Luc, Université catholique de Louvain, Service de Chirurgie Orthopédique et Traumatologie, Bruxelles, Belgique.
1. Contributeurs équivalents
Correspondance
Pr. Olivier Cornu
Cliniques universitaires Saint-Luc UCL
Service de Chirurgie Orthopédique et Traumatologie
Avenue Hippocrate 10
B-1200 Bruxelles