INTRODUCTION
La pseudo-obstruction intestinale chronique (POIC) est une maladie rare et méconnue de la motilité gastro-intestinale, responsable d’une morbidité et mortalité importantes (1). Sa prévalence est inconnue mais semble rare en gériatrie, étant décrite principalement en pédiatrie et chez les jeunes adultes. Obtenir des données épidémiologiques à propos de la POIC au sein de la population gériatrique permettrait d’optimiser et de standardiser la prise en charge diagnostique et thérapeutique des patients gériatriques.
CAS CLINIQUES
Le premier cas est un homme de 77 ans admis aux urgences suite à deux malaises consécutifs avec perte de connaissance dans un contexte d’hypotension et de déshydratation avec hyponatrémie et hypokaliémie secondaires à la prise de diurétiques et de diarrhée modérée les jours précédents. Par ailleurs, on note une perte de dix kilos en un an.
Parmi ses antécédents, retenons une hémorragie fronto-pariéto-temporale droite à l’âge de 31 ans, responsable d’une hémiparésie gauche séquellaire, un épisode de fécalome et globe vésical, une hypertrophie prostatique, une hyponatrémie et une décompensation cardiaque. Dans un contexte de constipation chronique, un abdomen à blanc avec lavement baryté de 2010 objective un dolichocôlon et méga-sigmoïde. Une colonoscopie en 2014 confirme un dolichocôlon majeur.
Son traitement médicamenteux consiste en valproate, acide acetylsalicilique, bisoprolol, losartan, furosémide, spironolactone, tamsulosine, esoméprazole, lorazépam, calcium et vitamine D, ibuprofene si douleur et macrogol.
L’évaluation gériatrique ne met pas en évidence de troubles cognitifs majeurs (score MMSE -Mini Mental State Examination- à 29/30). Sur le plan socio-familial, il est célibataire sans enfant. Son parent le plus proche est sa sœur et il vit en maison de repos et de soins depuis deux ans. Au niveau fonctionnel, l’échelle des activités de la vie journalière (AVJ) est de 14/24, décrivant une indépendance altérée. Il présente une dénutrition protéique sévère, avec un score nutritionnel (Mini Nutritional Assessment) de 19.5/30 malgré un Indice de Masse Corporelle de 25.9 kg/m².
Peu après son arrivée, il se plaint de constipation et développe cinq jours plus tard de la diarrhée avec nausées. L’abdomen à blanc et le scanner objectivent une coprostase colique droite sans fécalome et une importante dilatation colique notamment du transverse (environ 12 cm) et du côlon gauche, puis deux semaines plus tard du sigmoïde (14 cm), dans un contexte de dolichocôlon chronique (figure 1).
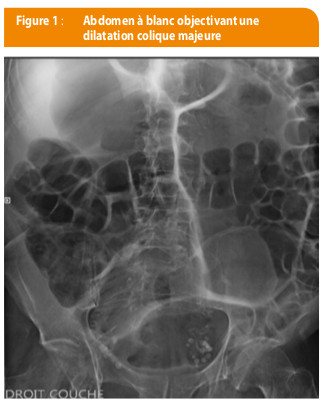
Ce cas a été discuté conjointement avec les gastro-entérologues, réticents à effectuer une endoscopie pour exsufflation vu le risque de perforation important, et les chirurgiens avec lesquels nous décidons de rester conservateurs. Une sonde nasogastrique de décharge est placée et le patient est laissé à jeun avec instauration d’une alimentation parentérale (figure 2). Une sonde rectale et des laxatifs (Macrogol oraux) sont prescrits. Une sonde urinaire à demeure est mise en place suite à plusieurs récidives de rétention vésicale. L’hypokaliémie secondaire au syndrome diarrhéique est sévère (2.66 mEq/l) et entraînera une fibrillation auriculaire paroxystique. Par deux fois, une endoscopie avec exsufflation limitée au rectum sera réalisée. Du prucalopride et de l’erythromycine en intraveineux seront débutés une fois l’hypokaliémie normalisée (nécessité d’apports quotidiens d’environ 100 mEq KCL et de diurétique d’épargne potassique). Il sera alité suite à un épisode infectieux sans identification bactériologique, sur probable translocation bactérienne digestive et une pneumonie d’inhalation. Des massages abdominaux en présence d’une canule rectale s’avèrent efficaces. Le patient retrouvera progressivement un transit spontané, reprendra un régime alimentaire normal et sera sevré de la parentérale et des canules rectales plus d’un mois après le début des symptômes, ceci correspondant également à la reprise de la marche. La supplémentation potassique et les prokinétiques seront progressivement stoppés, en maintenant une dose titrée en prucalopride en chronique (2mg par jour).

Le deuxième cas est une femme de 86 ans admise aux urgences pour hypoxie sur pneumonie. Elle est institutionnalisée en maison de repos et de soins et présente un profil gériatrique avec une dépendance totale pour les activités de base et instrumentales. De nombreuses chutes sont rapportées, la patiente ne se déplaçant que très peu et avec une aide mécanique. Elle est somnolente avec agitation nocturne gérée par psychotropes et ne tient plus de conversation depuis plusieurs mois. Une démence vasculaire avancée est probable vu l’hétéro-anamnèse, le score MMSE à 11/30, et le scanner cérébral objectivant une atrophie cortico-sous-corticale et une leuco-araïose avérées. Elle présente une amyotrophie sévère malgré son obésité.
On traite la pneumonie attribuée à des fausses déglutitions. Elle présente une insuffisance rénale aiguë post-rénale sur globe vésical, de résolution rapide après sondage, et une hypernatrémie sévère sur déshydratation. Une sonde nasogastrique pour administration d’eau libre puis d’alimentation entérale est placée. Une pseudo-obstruction colique est diagnostiquée suite aux douleurs abdominales, aux bruits métalliques à l’auscultation et à une distension majeure à l’imagerie. Le scanner objective en effet une importante dilatation aérique colique notamment du côlon transverse et du côlon gauche avec présence de liquide au niveau du recto-sigmoïde. Vu l’expérience du premier cas récemment vécu, des massages abdominaux en présence d’une canule rectale de décompression sont rapidement débutés. Du prucalopride est ensuite essayé mais vite arrêté devant le peu d’amélioration et la mauvaise tolérance (douleurs abdominales). L’hypokaliémie secondaire est substituée. La question de la chronicité de cette pseudo-obstruction se pose. Selon la famille, elle présente des symptômes abdominaux principalement de la constipation depuis une quarantaine d’années, attribués à une origine psychosomatique. Une colonoscopie en 2009 s’avère non contributive. Un scanner en 2013 dans ce contexte de constipation chronique avait déjà objectivé une importante distension gazeuse des anses grêles et coliques (diamètre de 7 cm) et une stase liquidienne au niveau du rectum et du sigmoïde.
DISCUSSION
La POIC est un trouble de la motilité intestinale rare et hautement morbide. Le syndrome occlusif abdominal peut être chronique ou évoluer par accès paroxystiques itératifs, sans qu’il y ait d’obstacle mécanique (2,5). L’aspect chronique la différencie donc de la pseudo-obstruction intestinale aiguë (POIA) ou syndrome d’Ogilvie, mais les critères de temporalité restent malheureusement souvent flous, aucune donnée n’étant à ce jour disponible pour la POIC.
Des critères diagnostiques ont été établis en 2009 par le ministère de la santé du Japon (1) (Tableau 1). Les quatre conditions suivantes, retrouvées chez nos deux patients, pour déclarer la présence d’une POIC doivent être remplies : au moins un épisode d’obstruction intestinale dans les six mois précédents, ballonnement et/ou douleur abdominale endéans les douze dernières semaines, dilatation et/ou niveaux hydro-aériques intestinaux objectivés sur l’imagerie et l’absence de maladie organique potentiellement responsable.

La prévalence de la POIC est inconnue. Une étude nationale au Japon a estimé la prévalence à 1/100 000 hommes et 0,8/100 000 femmes (1). Il s’agit souvent d’enfants ou de jeunes adultes (3), quoique cette même étude citait un âge moyen de diagnostic de 63,1 ans pour les hommes et 59,2 ans pour les femmes (1).
Les symptômes dépendent du segment intestinal atteint, avec plusieurs atteintes simultanées possibles. L’atteinte du grêle prédomine souvent (4). Chez le premier patient, l’ensemble de l’intestin était concerné mais principalement le cadre colique et le sigmoïde, entraînant alors une distension abdominale et de la constipation. D’autres atteintes étaient présentes, telle une gastroparésie transitoire et des symptômes urinaires de type rétention. Ces derniers peuvent parfois entraîner une urétéro-hydronéphrose (3). Les symptômes débutent souvent de manière insidieuse. Dans les deux cas rapportés, la situation existait depuis plusieurs années. Cela représente un challenge pour le diagnostic et entraîne sans doute un retard de prise en charge.
Il est important de distinguer la POIC du volvulus. Les occlusions sont soit fonctionnelles, c’est le cas de la POIC, soit mécaniques comme le volvulus (10). Les occlusions fonctionnelles ont pour définition l’absence d’obstacle mécanique. Il s’agit d’un diagnostic d’exclusion et le traitement est uniquement étiologique et symptomatique. Le volvulus est une occlusion mécanique par un facteur extrinsèque. Il s’agit d’une strangulation ou torsion d’un segment intestinal mobile et de ses vaisseaux attenants souvent engendrée par une bride post-opératoire. L’obstacle est identifié par l’imagerie (image typique “en bec d’oiseau”, formée par le lavement radio-opaque en amont d’un volvulus) ou par la chirurgie. Les symptômes débutent brutalement, avec des douleurs permanentes et un péristaltisme absent. Sans traitement chirurgical d’urgence, l’ischémie peut survenir. Chez les hommes de plus de 60 ans, le volvulus siège le plus fréquemment au niveau du sigmoïde et l’évolution est plutôt subaiguë. Le traitement de premier choix chez ces patients plus âgés est une réduction par lavement ou endoscopie (10). L’autre mécanisme des occlusions mécaniques se fait par obstruction, c’est le cas des corps étrangers intrinsèques (fécalome par exemple), des maladies inflammatoires ou encore des tumeurs. Les symptômes dans ce cas apparaissent progressivement, avec des douleurs intermittentes et un météorisme diffus et le traitement est chirurgical.
La mise au point étiologique, comme toujours en gériatrie et en médecine en général, doit tenir compte de la balance risques-bénéfices de toute intervention à visée diagnostique et de la sanction thérapeutique qui en découle. Le consentement du patient doit bien entendu toujours être obtenu. L’âge des patients permet déjà d’exclure une origine primitive, qui représente 40% des POIC. Elles sont classées en trois groupes selon les anomalies physiopathologiques : myopathies, neuropathies viscérales (atteinte du système nerveux extrinsèque ortho- et para-sympathique ou du système nerveux intrinsèque appelé encore système nerveux entérique) et mésenchymopathies (atteinte des cellules interstitielles de Cajal) responsables de manifestations neurologiques supplémentaires (2, 3, 5).
Après avoir exclu un obstacle organique par scanner ou un volvulus colique, la recherche d’une étiologie secondaire commence par l’anamnèse. On s’enquiert des antécédents, des médicaments (l’izoniazide, les inhibiteurs calciques, les antidépresseurs tricycliques, les anti-parkinsoniens, les anti-cholinergiques et les opiacés étant les pourvoyeurs les plus fréquents), de l’existence d’une néoplasie (le cancer pulmonaire à petites cellules étant le plus fréquent), d’une radiothérapie récente, d’un diabète avec neuropathie, d’un déficit immunitaire, d’une lésion médullaire ou encore d’une maladie inflammatoire.
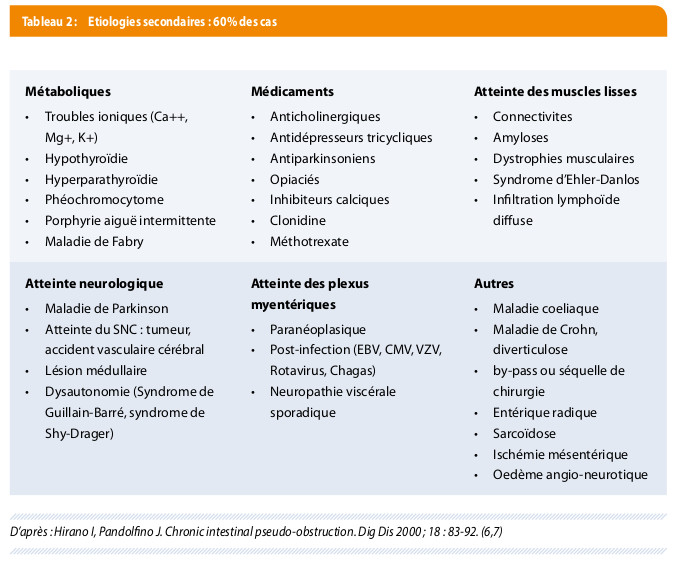
Les causes métaboliques sont les plus fréquentes des atteintes secondaires (5). Une biologie plus complète peut ainsi rechercher une hypothyroïdie, hyperparathyroïdie ou des troubles ioniques du calcium, potassium ou magnésium. La mise au point des deux patients s’est donc pratiquement arrêtée là. En effet, des biopsies sont nécessaires pour exclure les autres étiologies secondaires (Tableau 2 ). Elles sont toutefois souvent négatives car ne comprennent pas les couches profondes, souvent atteintes dans la POIC (5).
Les autres tests parfois proposés restent limités dans la mise au point des patients gériatriques très fragiles. Il s’agit de la scintigraphie, de la manométrie antro-duodénale ou grêle, du test respiratoire à l’hydrogène, de l’électromyographie des membres inférieurs, du bilan urodynamique ou de la chirurgie en dernier recours pour obtenir des biopsies (2,5,8).
Sans autre élément probant, l’hypothèse étiologique du premier cas clinique est une atteinte neurologique, avec des séquelles d’une hémorragie cérébrale et une dysautonomie. De nouveau sans preuve formelle pour la deuxième patiente, une cause médicamenteuse dans le chef de l’olanzapine par ses effets anticholinergiques a été retenue. Une cause neurologique centrale est envisagée également devant le diabète sucré bien équilibré sans traitement que présentait la patiente, avec une possible atteinte dysautonomique, et une potentielle atteinte centrale mal expliquée due à sa démence vasculaire avancée.
Une attention particulière est portée au problème de l’hypokaliémie, pouvant à la fois être une cause et une conséquence. En effet, on sait qu’une hypokaliémie sévère peut engendrer des symptômes au niveau des muscles lisses, causant ainsi de la constipation, pouvant aller jusqu’à l’iléus paralytique. L’hypokaliémie est également une conséquence des diarrhées par pertes digestives. Le mécanisme classique des diarrhées sécrétoires consiste en une sécrétion active de chlore et/ou une sécrétion passive de sodium ou une inhibition de la réabsorption intestinale de sodium, s’accompagnant d’eau par effet isotonique. Le mécanisme agissant dans les pseudo-obstructions coliques responsables d’hypokaliémies sévères semble tout autre. Le taux de potassium dans les selles de ces patients serait beaucoup plus élevé que dans n’importe quelle autre cause de diarrhée, taux d’ailleurs proportionnel à la quantité de selles émises (11,12). Cela s’accompagne d’une hypernatrémie, secondaire aux faibles pertes intestinales de sodium et aux pertes d’eau importantes. Cette hypersécrétion potassique serait due à une stimulation adrénergique excessive du système nerveux entérique et à la distension colique elle-même qui stimule la sécrétion de potassium via les neurotransmetteurs VIP et acétylcholine (11,12). Cette dernière donnée encourage à agir rapidement sur la distension colique dans les POIC, de manière endoscopique ou pharmacologique, pour limiter les pertes potassiques et l’hypokaliémie en résultant (12).
Aucun traitement curatif n’existe actuellement. Il convient de gérer les symptômes et lutter contre la dénutrition fréquente. La revue de la littérature révèle cependant qu’une alimentation entérale par sonde naso-jéjunale à court terme ou par gastrostomie - ou jéjunostomie si existence d’une gastroparésie- à long terme est à préférer à la nutrition parentérale. De fait, cette dernière est souvent définitive et peut causer des atrophies intestinales, translocations bactériennes et complications biliaires (4). Si la parentérale est néanmoins administrée en cas d’échec de l’entérale, des apports par voie naturelle doivent être maintenus en parallèle pour éviter ces mêmes complications (4). On préconise alors un régime fractionné, sans graisse et sans lactose, ainsi qu’une éventuelle substitution en cas de malabsorption. Dans les cas de myopathie où les troubles de la motilité sont généralisés, la nutrition parentérale est parfois indiquée.
Le traitement médicamenteux comporte plusieurs options qui sont malheureusement rarement efficaces en cas de dilatation majeure chronique. Les prokinétiques sont recommandés conjointement aux laxatifs. Le prucalopride est un agoniste des récepteurs sérotoninergiques bien toléré, sûr et efficace pour accélérer le transit et soulager les symptômes de ballonnement et douleurs abdominales (7) chez les personnes âgées (8) (la dose recommandée est alors de 1mg par jour plutôt que de 2mg). Il existe un risque d’allongement du QT et de torsade de pointes, mais nettement moindre qu’avec le cisapride. L’Erythromycine (recommandé à la dose de 3mg/kg/8h en intraveineux pendant 5 à 7 jours), un antibiotique macrolide agoniste motiline like qui augmente la fréquence et l’amplitude des contractions intestinales peut aussi être utilisé. Il est plus efficace pour le traitement des poussées qu’en entretien (9). Comme pour le prucalopride, la kaliémie doit être normalisée avant son administration pour éviter les troubles du rythme. D’autres prokinétiques sont disponibles pour le traitement des poussées mais sont plus à risque, comme le métoclopramide et la domperidone. La prostigmine/ néostigmine, un inhibiteur réversible de l’acétylcholinestérase, n’a pas été testée dans la POIC (5). Elle doit se faire en perfusion intraveineuse (0,5mg) et sous surveillance cardiaque et tensionnelle (5). Enfin, les antibiotiques sont recommandés en cas de pullulation bactérienne (4).
La colo-exsufflation est plus à risque que la recto-exsufflation en terme de perforation colique (de 0 à 5% des cas). Elle n’a pas été validée dans la POIC. La mortalité est inférieure à 5%. Les récidives surviennent dans 0 à 50% des cas, la procédure étant alors moins efficace (entre 25 et 80%) (5).
La chirurgie – par décompression intestinale, gastrostomie d’aspiration et jéjunostomie d’alimentation – n’est pas un premier choix. Elle entraîne, outre des complications per- et post-opératoires classiques, un risque de péjoration de la POIC (5). L’entérectomie sub-totale peut être responsable d’un syndrome de grêle court et de dépendance à la nutrition parentérale. L’efficacité et la sécurité à long terme de la caecostomie ne sont pas connues. Enfin, la transplantation intestinale est réservée aux patients (jeunes) ayant des complications majeures de la nutrition parentérale (4).
CONCLUSIONS
La pseudo-obstruction intestinale chronique est un diagnostic rare, surtout en gériatrie. Cette entité doit pourtant être connue des gériatres car elle est probablement parfois présente chez les patients âgés souffrant de constipation chronique. Des études de prévalence devraient être réalisées au sein de cette population âgée et fragile afin de développer et optimiser une prise en charge spécifique.
La gestion, tant dans ses aspects diagnostiques que thérapeutiques, devrait être mesurée eu égard à l’importante morbidité de la pathologie, des examens et des traitements, le tout survenant chez des patients âgés déjà fragiles.
Le contrôle des symptômes et des troubles ioniques (l’hypokaliémie pouvant être à la fois une cause et une conséquence), la nutrition – de préférence entérale – et le maintien d’une mobilité minimale sont primordiaux. La temporisation permet de mener une réflexion pluridisciplinaire – en accord avec le patient – privilégiant une attitude conservatrice.
Recommandations pratiques
- La recherche étiologique restera souvent limitée en gériatrie (antécédents, anamnèse, examen clinique, biologie et imagerie) au vu de la balance risque/bénéfice négative de certains examens.
- Non curatif, le traitement veillera à contrôler les symptômes et les troubles ioniques, maintenir une nutrition de préférence entérale et une mobilité minimale
Affiliations
(1) Service de Gériatrie, Grand Hôpital de Charleroi, 6061 Montignies-sur-Sambre, Belgique
Correspondance
Dr. Henrianne Levie
Grand Hôpital de Charleroi
Service de Gériatrie
Grand'Rue, 3
B-6000 Charleroi
Références
- Iida H, Ohkubo H, Inamori M, Nakajima A, Sato H. Epidemiology and Clinical Experience of Chronic Intestinal Pseudo-Obstruction in Japan: A Nationwide Epidemiologic Survey. J Epidemiol 2013; 23(4): 288–294.
ouvrir dans Pubmed - De Giorgio R, Sarnelli G, Corinaldesi R, Stanghellini V. Advances in our understanding of the pathology of chronic intestinal pseudo-obstruction. Gut 2004;53:1549–1552.
ouvrir dans Pubmed - Mann S D, Debinski H S, Kamm M A. Clinical characteristics of chronic idiopathic intestinal pseudo-obstruction in adults. Gut 1997 Nov; 41(5):675-81.
ouvrir dans Pubmed - Joly F, Amiot A, Coffin B, Lavergne-Slove A, Messing B, Bouhnik Y. Pseudo-obstruction intestinale chronique. Gastroentérologie Clinique et Biologique 2006 ; 30 (8-9) : 975-985.
ouvrir dans Pubmed - Ben Ameur H, Boujelbene S, Issam Beyrouti M. Traitement de la Pseudo-Obstruction Colique aiguë (syndrome d’Ogilvie) revue systématique de la Littérature. La Tunisie Médicale 2013 ; 91 (010 ) : 565-572.
ouvrir dans Pubmed - Hirano I, Pandolfino J. Chronic intestinal pseudo-obstruction. Dig Dis 2000;18(2):83-92.
ouvrir dans Pubmed - Emmanuel AV, Kamm MA, Roy AJ, Kerstens R, Vandeplassche L.. Randomised clinical trial: the efficacy of prucalopride in patients with chronic intestinal pseudo-obstruction - a double-blind, placebo-controlled, cross-over, multiple n = 1 study. Aliment Pharmacol Ther 2012; 35(1): 48–55.
ouvrir dans Pubmed - Müller-Lissner S., Rykx A., Kerstens R., Vandeplassche L. A double-blind, placebo-controlled study of prucalopride in elderly patients with chronic constipation. Neurogastroenterol Motil 2010;22(9):991-8.
ouvrir dans Pubmed - Emmanuel AV, Shand AG, Kamm MA. Erythromycin for the treatment of chronic intestinal pseudo-obstruction : description of six cases with a positive response. Aliment Pharmacol Ther 2004;19(6):687-94.
ouvrir dans Pubmed - CDU-HGE. Occlusions intestinales. In: Les fondamentaux de la pathologie digestive. Elsevier-Masson, France, 2014.
- Van Dinter TG, Fuerst FC, Richardson CT, Santa Ana CA, Polter DE, Fordtran JS, Binder HJ. Stimulated Active Potassium Secretion in a Patient With Colonic Pseudo-Obstruction: A New Mechanism of Secretory Diarrhea. Gastroenterology 2005; 129: 1268–1273.
ouvrir dans Pubmed - Blondon H, Béchade D, Desramé J, Algayres J-P. Secretory diarrhoea with high faecal potassium concentrations: A new mechanism of diarrhoea associated with colonic pseudo-obstruction? Report of five patients. Gastroentérologie Clinique et Biologique 2008; 32(4):401-404.
ouvrir dans Pubmed