La neurologie : nouveautés diagnostiques et thérapeutiques 2019
Adrian Ivanoiu
En cette époque d’explosion des connaissances dans tous les domaines de la médecine il n’est pas chose aisé que de résumer les principales avancées de l’année écoulée. Parmi les domaines de la neurologie, la prise en charge des maladies cérébrovasculaires a connu des avancées considérables ces dernières années, avec l’introduction à large échelle des thérapies efficaces que sont la thrombolyse et la thrombectomie. L’heure est maintenant au raffinement des techniques et à leur extension aux situations cliniques « non-standard », avec un accent important mis sur les aspects organisationnels pour amener ces patients dans les meilleurs délais dans un service médical approprié.
Un autre domaine phare de la neurologie, la sclérose en plaques, a connu aussi l’introduction de nouveaux traitements immunomodulateurs innovants depuis plusieurs années. Une attention particulière est actuellement portée aux âges extrêmes de la vie, de l’adolescence quand les premiers symptômes peuvent apparaître à l’âge mature avec tous les problèmes qui s’ajoutent au handicap déjà présent du fait de la maladie. La sclérose en plaques est de plus en plus vue comme un dérèglement immunitaire chronique qui commence tôt et qui perdure pendant le restant de la vie du patient. Un point particulier concerne les efforts pour trouver une thérapeutique efficace pour combattre la phase progressive, dégénérative, de la sclérose en plaques qui suit la phase inflammatoire. En termes diagnostiques une découverte importante concernant les nouveaux marqueurs d’imagerie par résonance magnétique nucléaire de la sclérose en plaques est associée aux travaux d’un jeune neurologue, le Docteur Maggi, qui vient de rejoindre l’équipe du service de neurologie des Cliniques Saint Luc (voir Maggi ds. cette édition).
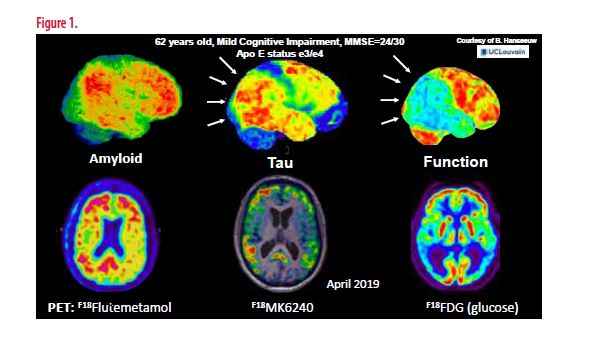
Alors que les maladies cérébrovasculaires et neuroinflammatoires ont enregistré des avancées spectaculaires dans le domaine du traitement cela n’est pas encore le cas pour les maladies neurodégénératives qui restent « l’ultime frontière » de la neurologie au niveau thérapeutique. Toutefois, de plus en plus de recherches dans ce domaine sont entreprises et les avancées semblent prometteuses dans des affections comme les maladies d’Alzheimer ou de Parkinson. Des nouvelles technologies permettent actuellement un diagnostic plus précoce de la maladie d’Alzheimer en utilisant des traceurs pour les protéines pathologiques qui caractérisent cette maladie (amyloïde β42 et protéine tau). La Figure 1 montre le premier examen de ce type en Belgique francophone utilisant un traceur pour la protéine tau (F18-MK6240) qui a été réalisé aux Cliniques universitaires Saint Luc le 25 avril 2019 dans le cadre d’un protocole de recherche. Par ailleurs, à côté des développements technologiques, d’autres méthodes originales permettant un diagnostic plus précoce de la maladie d’Alzheimer sont testées, partant de l’utilisation de « big data ». Une telle étude de notre équipe est expliquée par Olga Seminck et le Professeur Hanseeuw (cette édition) qui exploitent les données écrites dans les messages SMS ou les emails afin de déceler des modifications subtiles de l’utilisation de mots ou de la syntaxe qui seraient prédictives d’un futur déclin cognitif.
L’épilepsie fait partie du quatuor de tête des affections neurologiques les plus fréquentes. Un aspect souvent méconnu de cette pathologie est l’augmentation du risque de mort subite, chez des patients encore jeunes et, en apparence, en bonne santé. Le Professeur Ferrao-Santos, neurologue et épileptologue des Cliniques universitaires Saint Luc fait le point sur cette complication redoutée de l’épilepsie dans cette édition (Ferrao-Santos, cette édition).
Le domaine neuromusculaire, qui inclut des pathologies fréquentes comme les neuropathies inflammatoires ou d’une autre étiologie ou encore les myopathies, n’est pas en reste. Dans cette édition, le Professeur Van den Bergh, neurologue responsable du Centre neuromusculaire Saint Luc, fait le point sur les neuropathies paranodales/nodales chroniques à anticorps IgG4 ressemblantes mais différentes de la polyradiculoneuropathie inflammatoire démyélinisante chronique (CIDP – chronic inflammatory demyelinating polyradiculoneuropathy) qui est une pathologie peu connue en dehors du domaine de la neurologie et de diagnostic difficile, alors que des traitements sont disponibles. Toujours dans ce domaine, le Docteur Dubuisson, neurologue aux cliniques universitaires Saint Luc, présente une nouvelle méthode de diagnostic des neuropathies utilisant des techniques échographiques (Dubuisson, dans cette édition).
Enfin, « last but not least », de nouveaux traitements antimigraineux ont fait leur apparition sur le marché (ex. les antagonistes des récepteurs du CGRP) qui pourraient changer fondamentalement la prise en charge. Notre collègue, le Docteur de Tourtchaninoff, neurologue des cliniques universitaires Saint Luc, présente dans cette édition une mise au point de l’année dernière par le Professeur Goadsby, une des figures de proue internationales dans le domaine de la migraine et des céphalées. On peut rétorquer qu’il s’agit d’une affection bénigne mais, en réalité, la maladie migraineuse est une source majeure de souffrance pour ceux qui en sont atteints et d’absentéisme au travail. La neurologie s’est donc très bien porté en 2019 et les pistes de recherche en cours sont prometteuses pour encore plus de résultats demain avec, on l’espère, des meilleures capacités de prise en charge pour les patients qui sont atteints de troubles neurologiques.
Références
- Maggi, P. Nouveaux biomarqueurs IRM pour le diagnostic et le pronostic de la sclérose en plaques. louvain med 2020 ; 139 (02) : 126
- Bernard Hanseeuw, Louise-Amélie Cougnon, Olga Seminck. Les messages électroniques pour dépister la maladie d’Alzheimer. louvain med 2020 ; 139 (02) : 127
- Ferrao-Santos S. Comment la mort subite liée à l’épilepsie (SUDEP) façonne la recherche et développement dans le domaine de l’épilepsie. louvain med 2020 ; 139 (02) : 122
- Van den Bergh P.Y. K.. Les neuropathies paranodales/nodales chroniques à anticorps IgG4 et CIDP. louvain med 2020 ; 139 (02) : 124
- Dubuisson N. Utilisation de l’échographie dans les polyneuropathies. louvain med 2020 ; 139 (02) : 128
- de Tourtchaninoff M. Céphalées : nouveautés thérapeutiques en 2019. louvain med 2020 ; 139 (02) : 121
Céphalées : nouveautés thérapeutiques en 2019
Marianne de Tourtchaninoff
Dans un récent article de revue, Peter Goadsby, une des figures de proue internationales dans le domaine de la migraine et des céphalées, nous livre les dernières avancées en la matière.
Les céphalées primaires, comme la migraine et le cluster headache, sont les raisons les plus fréquentes pour lesquelles les patients consultent en neurologie. Ces céphalées touchent chaque année près de 3 milliards de personnes. Toute nouvelle thérapie dans le domaine est donc d’un intérêt majeur.
L’avènement des triptans il y a 30 ans a constitué une révolution. Depuis lors, les progrès réalisés dans la compréhension des mécanismes de la migraine et du cluster headache, surtout au cours des 5 dernières années, ont permis le développement de nouvelles pistes thérapeutiques. Un des champs les plus importants dans ce domaine est probablement celui du rôle du CGRP (calcitonine gene related peptide) dans les mécanismes physiopathogéniques de la migraine.
Au chapitre de la migraine proprement dite, Peter Goadsby retient en termes de nouveautés thérapeutiques :
1) dans le domaine du traitement des crises, les gépants, antagonistes des récepteurs du CGRP (rimegepant et ubrogepant) et les ditans, agonistes des récepteurs de la sérotonine de type 5-HT1F (lamiditan) ont terminé les études de phase 3 et seront bientôt proposés comme option de traitement de crise dans la migraine, avec un profil de sécurité majoré. En effet ces produits n’ont pas d’effet vasoconstricteur, effet qui limite actuellement l’usage des triptans;
2) dans le domaine du traitement prophylactique, le développement des anticorps monoclonaux anti-CGRP constitue une révolution en soi. Trois produits sont actuellement approuvés : l’erenumab, le fremanezumab et le galcanezumab. Un quatrième doit suivre, l’eptinezumab. Ces produits, spécialement développés pour le traitement de la migraine sont efficaces et bien tolérés;
3) des options non médicamenteuses existent également dans le traitement de la migraine grâce aux techniques de neuromodulation : stimulation magnétique transcrânienne (single pulse), stimulation non invasive du nerf vague, stimulation externe du nerf trijumeau. Ces traitements sont également bien tolérés;
4) Peter Goadsby voit également dans l’étude des phases non douloureuses de la migraine - phase prodromale (fatigue, bâillements, troubles de concentration et d’attention, fringales, …) et postdromale) - et dans la compréhension de leurs mécanismes un vaste champ de développement pour une meilleure prise en charge de la migraine notamment en terme d’auto-gestion par le patient;
5) plus anecdotiquement, Peter Goadsby nous parle de la reformulation galénique des triptans avec le développement de systèmes d’administration plus efficaces, comme un activateur de perméabilité pour le sumatriptan intra-nasal ou une application par voie transcutanée pour le zolmitriptan.
Au chapitre du cluster headache, entité quelque peu orpheline au vu du nombre de patients concernés, les avancées ne sont pas négligeables, peut-être grâce aux points communs entre mécanismes physiopathologiques de la migraine et du cluster headache. Peter Goadsby relève ce qui suit :
1) la stimulation non invasive du nerf vague, représente un traitement efficace et bien toléré dans les crises de cluster headache épisodique;
2 ) la stimulation non invasive du nerf vague, est également un traitement efficace et bien toléré dans le traitement prophylactique du cluster headache;
3) l’anticorps anti-CGRP galcanezumab s’est montré efficace et bien toléré dans un essai clinique contrôlé par placebo en tant que traitement prophylactique du cluster headache épisodique;
4) la stimulation du ganglion sphéno-palatin s’est aussi montrée efficace et bien tolérée lors de 2 études randomisées et contrôlées (sham-control) dans le cluster headache chronique.
Conclusion
L’auteur conclut que malgré certains points négatifs (limites épistémiologiques de la classification, financement insuffisant de la recherche dans le domaine, absence de nouveaux traitements pour les céphalées de tension, …), le neurologue est en mesure aujourd’hui de proposer aux patients céphalalgiques des traitements préventifs “sur mesure”, ce qui prouve que la recherche dans le domaine est efficace ; il peut, ou pourra bientôt, recourir aux nouvelles thérapies aigues et préventives de même qu’aux techniques de neuro-modulation. L’éducation du patient est également primordiale et l’explication des mécanismes physiopathogéniques doit lui permettre de mieux gérer la pathologie.
NB : les anticorps monoclonaux ne sont actuellement pas commercialisés en Belgique pour cause de refus de remboursement par l’INAMI ; ils sont donc inaccessibles aux patients belges.
Référence
Peter J. Goadsby. Primary headache disorders. Five new things. Neurology: Clinical Practice June 2019 vol. 9 no. 3 233-240 doi:10.1212/CPJ.0000000000000654
Comment la mort subite liée à l’épilepsie (SUDEP) façonne la recherche et développement dans le domaine de l’épilepsie
Susana Ferrao-Santos
La mort subite liée à l’épilepsie, ou SUDEP (Sudden unexpected death in epilepsy), est une problématique extrêmement redoutée mais également difficile à appréhender. Durant des années, les causes étaient mystérieuses, les possibilités d’action semblaient inexistantes et, dès lors, la communication autour de ce sujet particulier apparaissait si difficile que peu de médecins en parlaient.
Les patients, lorsque interrogés, sont pourtant assez unanimes : ils veulent être informés du risque de SUDEP, dès que possible, et par leur médecin de préférence (1). Aux Etats-Unis, les organisations de patients sont à la source d’une impulsion extrêmement dynamique, permettant de subventionner la recherche, la communication, les registres, etc. Il est fascinant d’observer qu’effectivement, en une décennie, nous sommes passés de la méconnaissance quasi-totale, à la dissection élégante de mécanismes physiopathologiques mais aussi au développement de technologies innovantes visant à protéger le patient du SUDEP.
Physiopathologie du SUDEP
L’incidence annuelle du SUDEP est de 1 cas/1000 patients chez les adultes et de 1 cas/4500 patients chez les enfants (2). L’étude Mortemus a permis de dévoiler les caractéristiques communes des cas de SUDEP enregistrés sous surveillance (EEG, ECG, SpO2, EMG), dans le cadre de bilans d’épilepsie. La physiopathologie proposée est celle d’une apnée d’origine centrale, durant et après la crise (3), bien que d’autres mécanismes probablement complémentaires (cardiaque, génétique) soient également à l’étude.
Le plus grand facteur de risque de SUDEP est la persistance de crises tonico-cloniques généralisées, en particulier si la fréquence dépasse 2 fois par an. Le caractère pharmaco-résistant de l’épilepsie, et le fait de ne pas ajouter d’antiépileptique en cas de persistance de crises sont également des facteurs de risque, plus modérés (2). Enfin, le SUDEP frappe plus souvent les jeunes adultes (4).
Impact de la surveillance et des interventions
Il semble clair que la surveillance nocturne permet de réduire l’incidence de SUDEP. Par exemple, une étude centrée sur les centres de résidence de patients souffrant de formes sévères d’épilepsie montre que les plus hauts taux de SUDEP surviennent dans les centres où la supervision nocturne est moindre (5). Il y a donc un effet bénéfique de l’intervention des proches ou des soignants, liés en premier lieu à une simple stimulation du patient. Par ailleurs, l’administration d’oxygène en milieu hospitalier réduit également l’importance de l’hypoxémie liée à la crise (6). Il y a donc une importante demande de développer des moyens efficaces de détecter les crises, pour permettre une intervention à temps. Il faut noter cependant que même lorsque la crise a été détectée, l’intervention ne permet pas toujours d’empêcher le décès.
Détection de crises
L’EEG est le meilleur biomarqueur d’une crise d’épilepsie, mais les appareils de mesure actuels ne permettent pas un usage quotidien à domicile. D’autres biomarqueurs de crises, en particulier des crises tonico-cloniques généralisées, sont la mesure de contraction musculaire, la variabilité de la fréquence cardiaque, la mesure de conductance dermique et la mesure de mouvement dans l’espace. Ces biomarqueurs font déjà l’objet de mesures, seuls ou en combinaison, par des appareils destinés à l’usage du grand public. Les fausses alertes, qui à l’heure actuelle sont souvent quotidiennes, sont un frein à l’usage chronique. La combinaison de plusieurs biomarqueurs devrait permettre de résoudre ce problème. Plusieurs technologies sont en développement et l’offre ne cesse d’augmenter. Le choix doit se porter en premier lieu sur les appareils ayant fait leurs preuves en milieu contrôlé, c’est-à-dire en unité de monitoring d’épilepsie. Un appareil de détection basé sur la contraction musculaire montre des résultats encourageants, validés comparativement à l’EEG (SeizureLink®). Un appareil mesurant le mouvement et la fréquence cardiaque est également validé et commercialisé (Nightwatch®). Le bracelet EMBRACE®, doté d’un accéléromètre et d’une mesure de conductance dermique est utilisé depuis plusieurs années. Le taux de fausses alertes est assez haut, mais la facilité d’usage et le prix le rendent attrayant.
Impact des technologies sur le SUDEP et conseils pour la pratique clinique
Il n’y a pas encore d’évidence clinique pour affirmer qu’un appareil, qu’il soit voué à la détection ou au traitement des crises (comme le stimulateur du nerf vague), ait un impact sur l’incidence du SUDEP (7). Par contre, les taux de SUDEP sont en réduction. Les raisons sont probablement multiples, mais notre meilleure connaissance des mécanismes en jeu et les recommandations en vigueur pour cibler un meilleur contrôle des crises tonico-cloniques généralisées sont probablement liés aux moindres taux de SUDEP (8). Les registres de cas de SUDEP sont extrêmement importants pour notre connaissance de cette complication dévastatrice de l’épilepsie. Tous les cliniciens en contact régulier avec l’épilepsie devraient être encouragés à rapporter les cas de SUDEP. En Belgique, aucun registre national n’existe, mais il est possible de rapporter les cas sur des registres supra-nationaux.
Références
- Xu Z, Ayyappan S, Seneviratne U. Sudden unexpected death in epilepsy (SUDEP): What do patients think? Epilepsy & Behavior. 2015; 42: 29–34. https://doi.org/10.1016/j.yebeh.2014.11.007
- Harden C, Tomson T, Gloss D, Buchhalter J, Cross JH, Donner E, et al. Practice guideline summary: Sudden unexpected death in epilepsy incidence rates and risk factors. Neurology, 2017; 88(17): 1674 LP – 1680. https://doi.org/10.1212/WNL.0000000000003685
- Ryvlin P, Nashef L, Lhatoo SD, Bateman LM, Bird J, Bleasel A, et al. Incidence and mechanisms of cardiorespiratory arrests in epilepsy monitoring units (MORTEMUS): A retrospective study. Lancet Neurol. 2013; 12(10): 966–977. https://doi.org/10.1016/S1474-4422(13)70214-X
- Sveinsson O, Andersson T, Torbj SC. Circumstances of SUDEP : A nationwide population-based case series. Epilepsia. 2018 May;59(5):1074-1082. https://doi.org/10.1111/epi.14079
- van der Lende M, Hesdorffer DC, Sander JW, Thijs RD. Nocturnal supervision and SUDEP risk at different epilepsy care settings. Neurology, 2018; 91(16): e1508–e1518. https://doi.org/10.1212/WNL.0000000000006356
- Rheims S, Alvarez BM, Alexandre V, Curot J, Maillard L, Bartolomei F, et al. Hypoxemia following generalized convulsive seizures: Risk factors and effect of oxygen therapy. Neurology. (2019); 92(3): E183–E193. https://doi.org/10.1212/WNL.0000000000006777
- Ryvlin P, So EL, Gordon CM, Hesdorffer DC, Orrin RS, Mark D, et al. Long-term surveillance of SUDEP in drug-resistant epilepsy patients treated with VNS therapy. Epilepsia. 2018 Mar;59(3):562-572. https://doi.org/10.1111/epi.14002
- Tomson T, Sveinsson O, Carlsson S, Andersson T. Evolution over time of SUDEP incidence: A nationwide population-based cohort study. Epilepsia, 2018; 59(8): e120–e124. https://doi.org/10.1111/epi.14460
Les neuropathies paranodales/nodales chroniques à anticorps IgG4 et CIDP
Peter Y. K. Van den Bergh
La polyradiculoneuropathie inflammatoire démyélinisante chronique (CIDP) dans sa forme typique a été définie dans un article séminal de Dyck et al. en 1975 (1). Le tableau clinique comprend une faiblesse musculaire proximale et distale symétrique associée à une atteinte de la sensibilité et des réflexes ostéotendineux diminués ou absents. L'évolution de la maladie est progressive sur au moins 2 mois. Nous savons maintenant que la présentation clinique de la CIDP est beaucoup plus large. Il existe des formes atypiques incluant une forme avec déficit sensitivo-moteur distal seul, des formes motrice ou sensitive pure, ainsi que des présentations multifocales ou focales (2,3). Même si certaines caractéristiques cliniques diffèrent de la CIDP typique, les différentes présentations de CIDP atypique partagent les caractéristiques communes de démyélinisation inflammatoire et d’une réponse favorable à l'immunothérapie. Étant donné que la CIDP telle que définie par son nom doit se caractériser par une démyélinisation inflammatoire, la position nosologique de plusieurs neuropathies chroniques auto-immunes par rapport à la CIDP n'est pas claire.
Au cours des dernières années, des anticorps contre des molécules d'adhésion cellulaire paranodales et/ou nodales ont été découverts chez des patients répondant aux critères cliniques et électrophysiologiques EFNS/PNS pour la CIDP (2). Or, le phénotype clinique associé à ces anticorps semble avoir des caractéristiques différentes et les biopsies nerveuses ne montrent pas d'inflammation manifeste ou de démyélinisation classique mais plutôt une attente axonale (4,5).
Des anticorps contre la contactine-1 (CNTN1) ont été rapportés chez 2 à 7% des patients étiquetés CIDP avec un phénotype clinique distinct. Ces patients étaient plus âgés, présentaient un début de maladie aigu ou subaigu, et une évolution agressive. Des anticorps contre la neurofascine-155 (NF155) ont été observés chez 7 à 18% des patients étiquetés CIDP avec un phénotype encore un peu différent, caractérisé par un âge plus jeune, une faiblesse musculaire distale, une ataxie, des tremblements. Des anticorps contre la protéine 1 associée à la contactine (Caspr1) ont été décrits chez 2 patients, l'un avec un syndrome de Guillain-Barré et l'autre avec un phénotype CIDP. Ils présentaient une douleur intense et une faiblesse musculaire distale. Tous ces patients avaient en commun une réponse faible ou absente au traitement par IgIV. Des anticorps contre les isoformes de la neurofascine nodale, NF140/186, ont été observés chez 5 patients par Delmont et al. (6). Ces patients présentaient un début de maladie subaigu et une ataxie sensitive. Une bonne réponse aux IgIV ou aux corticostéroïdes a été observée chez 3 d'entre eux. NF155, Caspr1 et CNTN1 sont des molécules d'adhésion cellulaire fixant la jonction axo-gliale au niveau de la zone paranodale, ce qui est essentiel pour la conduction nerveuse saltatoire. Le complexe CNTN1-Caspr1 au niveau de l'axolemme paranodal s'associe à la NF155 aux boucles de myéline terminales pour former des jonctions cloisonnées (“septate-like junctions”) agissant comme une barrière membranaire pour limiter la diffusion latérale des canaux ioniques, assurant que le sodium est concentré au nœuds de Ranvier et le potassium aux zones juxtaparanodales. Ceci conduit aux blocs de conduction et au ralentissement de la vitesse de conduction sans qu’il y ait démyélinisation.
Presque toujours, ces anticorps contre des protéines paranodales/nodales sont de l'isotype IgG4, une sous-classe d'anticorps aux propriétés fonctionnelles et structurelles uniques (7,8). Les anticorps IgG4 présentent un « échange de demi-corps », ce qui signifie qu'ils sont fonctionnellement bispécifiques et monovalents et, par conséquent, ne peuvent pas se fixer sur des antigènes identiques. Ils ont une activité anti-inflammatoire, y compris une faible capacité à induire le complément et l'activation cellulaire en raison de la faible affinité pour les récepteurs C1q et Fc. Ils provoquent une pathologie par interférence directe avec l'antigène, bloquant ainsi mécaniquement les interactions protéine-protéine. Toutes ces caractéristiques peuvent expliquer pourquoi il n'y a pas d'inflammation ni de démyélinisation médiée par les cellules immunitaires, comme dans la CIDP typique et atypique et pourquoi la réponse aux traitements habituels, les IgIV en particulier, font souvent défaut. Il est intéressant de noter que la réponse au traitement par rituximab a été jugée bonne.
Même si pas inflammatoire et pas démyélinisant, ces neuropathies partagent de nombreuses caractéristiques avec la CIDP et, par conséquent, nous pensons qu'ils devraient faire partie pas de CIDP mais comme nous le proposons du syndrome CIDP. La dénomination syndrome CIDP (CIDPS) permettrait d'élargir le spectre actuel de la CIDP en analogie avec le syndrome de Guillain-Barré (GBS) qui est devenu un parapluie couvrant un grand nombre de variantes, notamment le syndrome de Fisher et l'encéphalite de Bickerstaff, les formes non généralisées (régionales), les sous-types électrophysiologiques axonaux et démyélinisants. En introduisant le syndrome CIDP, la CIDP serait « pars pro toto », comprenant non seulement les variantes typiques et atypiques de la CIDP, non seulement les neuropathies paranodales/nodales chroniques à anticorps IgG4 mais également la neuropathie anti-MAG, la polyradiculopathie sensitive immune chronique (CISP) et la neuropathie motrice multifocale (MMN) (9).
Références
- Dyck PJ, Lais AC, Ohta M, Bastron JA, Okazaki H, Groover RV. Chronic inflammatory polyradiculoneuropathy. Mayo Clin Proc. 1975;50:621-637.
- Van den Bergh PYK, Hadden RDM, Bouche P, Cornblath DR, Hahn A, Illa I et al. European Federation of Neurological Societies/Peripheral Nerve Society Guideline on management of chronic inflammatory demyelinating polyradiculoneuropathy: report of a joint task force of the European Federation of Neurological Societies and the Peripheral Nerve Society – First revision. Eur J Neurol. 2010;17:356-363.
- Bunschoten C, Jacobs BC, Van den Bergh PYK, Cornblath DR, van Doorn PA. Progress in diagnosis and treatment of chronic inflammatory demyelinating polyradiculoneuropathy. Lancet Neurol. 2019; 18: 784–794.
- Querol L, Devaux J, RojasGarcia R, Illa I. Autoantibodies in chronic inflammatory neuropathies: Diagnostic and therapeutic implications. Nat Rev Neurol. 2017; 13: 533–547.
- Koike H, Nishi R, Ikeda S, Kawagashira Y, Iijima M, Katsuno M, et al. Ultrastructural mechanisms of macrophage-induced demyelination in CIDP. Neurology. 2018 4;91:1051-1060.
- Delmont E, Manso C, Querol L, Cortese A, Berardinelli A, Lozza A, et al. Autoantibodies to nodal isoforms of neurofascin in chronic inflammatory demyelinating polyneuropathy. Brain. 2017; 140: 1851–1858.
- van der Neut Kolfschoten M, Schuurman J, Losen M, Bleeker WK, Martínez-Martínez P, Vermeulen E, et al. Anti-inflammatory activity of human IgG4 antibodies by dynamic Fab arm exchange. Science. 2007;317:1554-1557.
- Huijbers MG, Querol LA, Niks EH, Plomp JJ, van der Maarel SM, Graus F, et al. The expanding field of IgG4-mediated neurological autoimmune disorders. Eur J Neurol. 2015; 22: 1151–1161.
- Van den Bergh PYK, van Doorn PA, Jacobs BC, Querol L, Bunschoten C, Cornblath DR. Boundaries of chronic inflammatory demyelinating polyradiculoneuropathy. Peripher Nerv Syst. 2020 Jan 24. doi: 10.1111/jns.12364.
Nouveaux biomarqueurs IRM pour le diagnostic et le pronostic de la sclérose en plaques
Pietro Maggi, MD, PhD
La sclérose en plaque (SEP) est une maladie immuno-médiée caractérisée au niveau histopathologique par des lésions inflammatoires démyélinisantes du cerveau et de la moëlle épinière. L’imagerie par résonance magnétique (IRM) permet quant à elle de visualiser ces plaques in vivo et représente un outil fondamental pour le diagnostic et le pronostic de la maladie. Toutefois, la SEP représente aujourd’hui un défi diagnostique en raison de la spécificité limitée des critères diagnostiques radiologiques de la maladie. En effet, d’autres pathologies remplissent ces critères également, ce qui augmente le risque d’erreurs diagnostiques (« misdiagnosis ») (1).
Un autre « unmet clinical need » fondamental de la SEP est le manque de biomarqueurs pronostiques et prédictifs, surtout en ce qui concerne les phases progressives de la maladie. Dans les formes progressives, la mise en évidence par IRM d’une inflammation active (c’est-à-dire des plaques se rehaussant après injection de contraste) est plutôt rare. Pourtant, la majorité des traitements immunomodulateurs/suppresseurs de la SEP agissent justement contre l’inflammation. Il est dès lors difficile pour le clinicien neurologue de prescrire un traitement immunomodulateur/suppresseur à un patient ne montrant pas de signes d’inflammation active à l’IRM. Récemment l’IRM en écho de gradient a permis de mettre en évidence deux nouveaux biomarqueurs capables 1) d’augmenter la spécificité diagnostique pour la SEP (grâce au signe de la veine centrale ou, en anglais, « central vein sign ») et 2) d’améliorer le pronostic de la maladie (en détectant des lésions avec inflammation chronique, en anglais « chronic active lesions » ; Figure).
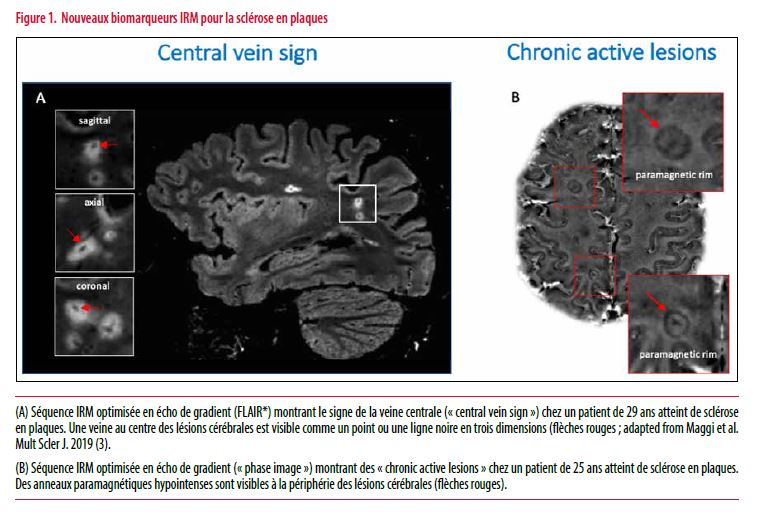
Du point de vue diagnostique, la présence d’une veine au centre des lésions de la substance blanche est une caractéristique histopathologique spécifique de la SEP, connue depuis Charcot. Aujourd’hui, la nature périveinulaire des lésions cérébrales peut être appréciée grâce à des nouvelles techniques d’IRM en écho de gradient. Une large étude multicentrique, a confirmé l’utilité du «central vein sign » dans le diagnostic différentiel de la SEP et a également montré que la performance diagnostique de ce biomarqueur varie en fonction de la séquence en écho de gradient utilisée (2). Une autre étude récente, utilisant une séquence optimisée en écho de gradient à 3 Tesla, a démontré que le « central vein sign » possède une haute valeur prédictive diagnostique chez des patients ayant des caractéristiques atypiques, ou « red flags », de la SEP(3).
En ce qui concerne l’aspect pronostique, la présence d’une inflammation chronique persistante au pourtour des lésions cérébrales, correspond à des anneaux paramagnétiques hypointenses visibles à la périphérie de ces lésions sur les images IRM en écho de gradient. Une large étude récemment publiée par Absinta et al. (4) a montré que la présence de ces « chronic active lesions » est corrélée à l’agressivité de la maladie en termes d’évolution clinique et radiologique. Dans ce contexte, une récente étude multicentrique suggère que ce biomarqueur radiologique (« chronic active lesions ») est corrélé positivement avec le niveau sérique des neurofilaments chez les patients atteints de SEP progressive (5). La possibilité de trouver un marqueur combiné sérologique-radiologique d’inflammation chronique pourrait guider la sélection des patients candidats aux traitements immunomodulateurs/suppresseurs.
Références
- Solomon AJ, Naismith RT, Cross AH. Misdiagnosis of multiple sclerosis: Impact of the 2017 McDonald criteria on clinical practice. Neurology. 2019;92(1):26-33. doi:10.1212/WNL.0000000000006583
- Sinnecker T, Clarke MA, Meier D, et al. Evaluation of the Central Vein Sign as a Diagnostic Imaging Biomarker in Multiple Sclerosis. JAMA Neurology. August 2019. doi:10.1001/jamaneurol.2019.2478
- Maggi P, Absinta M, Sati P, et al. The “central vein sign” in patients with diagnostic “red flags” for multiple sclerosis: A prospective multicenter 3T study. Multiple Sclerosis Journal. September 2019:135245851987603. doi:10.1177/1352458519876031
- Absinta M, Sati P, Masuzzo F, et al. Association of Chronic Active Multiple Sclerosis Lesions With Disability In Vivo. JAMA Neurology. August 2019. doi:10.1001/jamaneurol.2019.2399
- Maggi P, Kuhle J, Weigel M, et al. Paramagnetic phase rims and serum neurofilaments in relapsing-remitting and progressive multiple sclerosis patients: a combined laboratory-imaging marker of chronic inflammation. ECTRIMS 2019 – Oral Presentation. Multiple Sclerosis Journal. 2019;25(2_suppl):3-130. doi:10.1177/1352458519868070
Les messages électroniques pour dépister la maladie d’Alzheimer
Bernard Hanseeuw, Louise-Amélie Cougnon, Olga Seminck
La maladie d’Alzheimer touche une personne sur dix dans la population belge âgée de plus de 65 ans. Le risque de développer cette maladie augmente exponentiellement avec l’âge. Suite à la croissance de l’espérance de vie, le nombre de patients ne cesse donc d’augmenter ; et aujourd’hui, il n’existe pas de traitement qui permette d’arrêter la progression de la maladie (1). Il est donc urgent d’investir dans la recherche.
La recherche récente montre qu’une lutte efficace n’est sans doute possible que sous forme de prévention, par l’application de traitement avant l’apparition des symptômes de la maladie (tels les pertes de mémoire, la désorientation spatio-temporelle, le changement de personnalité (1). Cependant, aujourd’hui encore, c’est l’apparition de ces symptômes qui conduit au diagnostic.
L’analyse de la présence des protéines β-amyloïde et tau, caractéristiques de la maladie d’Alzheimer, dans le liquide céphalo-rachidien (2) ou en tomographie par émission de positron (3) permet désormais de poser ce diagnostic au stade des troubles cognitifs légers, avant la démence et la perte d’autonomie. Ces protéines anormales s’accumulent en effet dans le cerveau 15 à 20 ans avant la démence, et 10 à 15 ans avant les troubles cognitifs légers.
Bien que ces techniques permettent d’établir un diagnostic précoce, elles ne permettent tout de même pas à faire un dépistage systématique de la population âgée belge : la ponction lombaire et le PET-scan sont respectivement trop invasive et trop onéreux pour être proposés à tout un chacun. Vu la promesse des médicaments en phase d’essais cliniques d’être efficaces dans le cadre d’un traitement préventif, il devient primordial de développer des méthodes permettant de dépister les personnes à risque le plus tôt possible, avant que la cognition ne soit atteinte significativement. La méthode la plus sensible consisterait à mesurer la cognition de toute la personne âgée sur base régulière, de manière à dépister un déclin sur base individuelle le plus tôt possible ; mais cela est difficile pour des raisons pratiques évidentes (manque de personnels qualifiés pour tester la cognition, coût prohibitif…).
C’est dans ce cadre-là que le projet MIND-IT (https://www.uclouvain-mindit.be) a vu le jour au courant de l’année 2019. L’ambition de ce projet est d’exploiter la vaste quantité des messages électroniques échangée dans la vie quotidienne, comme les e-mails ou la messagerie WhatsApp, afin de voir si dans l’historique d’une personne on puisse voir une évolution dans la façon dont elle s’exprime. En effet, la maladie d’Alzheimer a une influence sur les capacités langagières : la richesse du vocabulaire diminue, ainsi que celle des structures grammaticaux employées (4). De plus, des études menées sur l’œuvre entière d’auteurs qui ont développé la maladie ont montré que leur style d’écriture avait déjà changé plusieurs années avant qu’ils ne soient diagnostiqués (5,6). Le projet MIND-IT étudie si l’historique des messages électroniques permet de voir une telle évolution pour tout un chacun, en mettant à profit les données acquises rétrospectivement dans la vie de tous les jours.
Pour réaliser cette étude, une équipe interdisciplinaire s’est formée impliquant plusieurs unités de recherche de l’UCLouvain : des chercheurs de l’Institut des Neurosciences, spécialistes de la maladie d’Alzheimer, et neurologues aux Cliniques universitaires Saint-Luc ; et des linguistes, spécialisés dans la communication électronique et le traitement automatique des langues.
Dans un premier temps, des personnes âgées de plus de 50 ans ayant la maladie d’Alzheimer, ainsi que des volontaires cliniquement normaux du même âge, sont recrutés pour faire don de l’historique de leurs messages électroniques.1 Ensuite, ces messages sont utilisés pour apprendre, grâce à l’intelligence artificielle, quelles sont les manifestations linguistiques d’une maladie d’Alzheimer qui se développe par rapport à une population de contrôle. L’objectif de cette étape est de développer un outil de détection qui fasse la différence entre ces deux groupes. Le défi est de détecter automatiquement les signes de la maladie d’Alzheimer et de déterminer quels paramètres linguistiques se modifient le plus tôt avant le diagnostic ; afin que dans un second temps, il puisse dépister des individus à risque, avant le diagnostic. Si cet outil s’avère efficace, il pourrait être utilisé pour proposer des examens médicaux aux personnes à risque, comme la ponction lombaire ou le PET-scanner, et éventuellement entrer dans des essais cliniques préventifs. Le but de MIND-IT est ainsi de permettre le dépistage préclinique, en évitant de faire subir des interventions à des personnes ne présentant aucune pathologie.
Références
- Meldolesi, J. Alzheimer’s disease: Key developments support promising perspectives for therapy. Pharm Res. 2019; 104316.
- Bayart JL, Hanseeuw B, Ivanoiu A, Van Pesch V. Analytical and clinical performances of the automated Lumipulse cerebrospinal fluid Aβ42 and T-Tau assays for Alzheimer’s disease diagnosis. J Neurol. 2019; 1–8.
- Hanseeuw BJ, Betensky RA, Jacobs HI, Schultz AP, Sepulcre J, Becker JA, et al. Association of amyloid and tau with cognition in preclinical Alzheimer disease: A longitudinal study. JAMA Neurology. 2019.
- Fraser KC, Meltzer JA, Rudzicz F. Linguistic features identify Alzheimer’s disease in narrative speech. J Alzheimers Dis. (2016). 49(2), 407–422.
- Kernot D, Bossomaier T, Bradbury R. The stylometric impacts of ageing and life events on identity. J Quantitative Linguistics. 2019; 26(1), 1-21.
- Marckx S, Verhoeven B, Daelemans W. The Claus case: exploring the use of propositional idea density for Alzheimer detection. Computational Linguistics in the Netherlands Journal. 2018; 8, 66–82.
1 La phase de recrutement est toujours en cours, pour participer, contactez louise-amélie.cougnon@uclouvain.be
Utilisation de l’échographie dans les polyneuropathies
Nicolas Dubuisson
Ces dernières années, suite à l’apparition sur le marché de nouvelles sondes électroniques à haute résolution et large bande de fréquence, permettant de visualiser le nerf de façon très précise, l’utilisation de l’échographie nerveuse a pris une nouvelle dimension.
Alors qu’au départ, son usage était essentiellement limité à l’évaluation des syndromes canalaires (syndrome du canal carpien, ...), des neuropathies traumatiques, des tumeurs nerveuses, et à l’aide aux interventions (infiltrations ou anesthésies locales). L’échographie est maintenant démontrée comme étant très utile dans la mise au point des polyneuropathies.
Les polyneuropathies sont des pathologies fréquentes, atteignant de 5,5 à 13.1% de la population générale (1) et leur diagnostic repose essentiellement sur l’examen clinique associé à une biologie sanguine et à une électromyographie (2).
Elles peuvent être séparée en deux catégories principales, celles d’origine héréditaires et les polyneuropathies inflammatoire (3).
Dans le domaine échographique, la polyneuropathie héréditaire la plus étudiée est la maladie de Charcot-Marie Tooth de type 1a (CMT1a) causée par une duplication du gène PMP 22, pour laquelle l’échographie nerveuse montre un pattern tout à fait spécifique avec un élargissement homogène et diffus de l’ensemble des nerfs étudiés.
Il existe également un élargissement nerveux, mais beaucoup moins marqué, pour d’autres types de neuropathies héréditaires comme CMTX, CMT2, CMT1b et CMT1c. La neuropathie héréditaire avec hypersensibilité à la pression (HNPP) montre un élargissement typique aux sites de compression habituels (coude, tête de la fibula, canal carpien) (4).
Pour ce qui est des polyneuropathies inflammatoires, la plus étudiée est la Chronic inflammatory demyelinating polyneuropathy (CIDP) qui est caractérisée par une atteinte sensitivo-motrice progressive proximale et distale affectant les 4 membres (forme typique). Un patient souffrant de CIDP présente typiquement un élargissement de la partie partie proximale des nerfs des membres supérieurs et du plexus brachial.
L’échographie nerveuse a deux rôles très important dans cette pathologie car elle permet d’une part, de renforcer le diagnostic (en association avec l’EMG) et d’autre part d’effectuer un monitoring thérapeutique. Le diamètre des nerfs diminuant si le traitement immunomodulateur est efficace (5). Ce même pattern est également retrouvé dans deux autres types de neuropathies inflammatoires, les neuropathies associées à une gammapathies monoclonales à IgM et les neuropathies motrices multifocales (MMN) (6). Les MMN sont des neuropathies purement motrices typiquement asymétriques, d’évolution progressive et pouvant être difficilement différentiable de certaines formes de sclérose latérale amyotrophique focales (SLA). Finalement les neuropathies vasculitiques présentent également des images caractéristiques à l’échographie nerveuse avec une atteinte proximale des nerfs des membres supérieurs mais une préservation du plexus brachial (7).
En conclusion, l’échographie nerveuse, lorsqu’elle est combinée avec l’EMG et un bon examen clinique, a pris une place importante dans la mise au point des neuropathies héréditaires et inflammatoires. En effet, l’association de l’échographie à l’EMG renforce la sensibilité et la spécificité des deux tests pris séparément, permettant avec plus de certitude d’établir un diagnostic. Ensuite elle permet de réaliser des screening rapide et non douloureux dans les suspicions de neuropathies héréditaires. Finalement, elle facilite le diagnostic différentiel entre les neuropathies traitables (MMN, CIDP) et non traitables (SLA, polyneuropathie axonale chroniques).
Il s’agit donc d’une technique prometteuse, mais pour laquelle des études à plus large échelle et étudiant d’autres types de neuropathies sont recommandées.
Références
- Hanewinckel R, Drenthen J, van Oijen M, et al.Prevalence of polyneuropathy in the general middle-aged and elderly population. Neurology. 2016; 87(18):1892–1898.
- England JD, Gronseth GS, Franklin G, et al. Practice parameter: the evaluation of distal symmetric polyneuropathy: the role of laboratory and genetic testing (an evidence-based review).Report of the American Academy of Neurology, the American Association of Neuromuscular and Electrodiagnostic Medicine, and the American Academy of Physical Medicine and Rehabilitation.PM R. 2009; 1(1):5–13.
- Telleman JA, Grimm A, Goedee S, Visser LH, Zaidman CM. Nerve ultrasound in polyneuropathies. Muscle Nerve. 2018; 57(5):716–728.
- Padua L, Coraci D, Lucchetta M, et al. Different nerve ultrasound patterns in charcot-marie-tooth types and hereditary neuropathy with liability to pressure palsies. Muscle Nerve. 2018; 57(1):E18–E23.
- Goedee HS, van der Pol WL, van Asseldonk J-TH, et al. Diagnostic value of sonography in treatment naive chronic inflammatory neuropathies. Neurology. 2017; 88(2):143–151.
- Breiner A, Ebadi H, Bril V, Barnett C, Katzberg HD. Ultrasound in Multifocal Motor Neuropathy: Clinical and Electrophysiological Correlations. J.Clin. Neuromuscul. Dis. 2019; 20(4):165–172.
- Goedee HS, Stephan Goedee H, van der Pol WL, et al. Nerve sonography to detect peripheral nerve involvement in vasculitis syndromes. Neurology: Clinical Practice. 2016; 6(4):293–303. Available at: http://dx.doi.org/10.1212/cpj.0000000000000258.
Affiliations
- Cliniques universitaires Saint Luc, service de neurologie, B-1200 Bruxelles
- Centre de référence neuromusculaire
- Institut des Neurosciences, Pôle clinique (NEUR)
- Institut Langage et Communication (CENTAL et MiiL) de l’UCLouvain
Correspondance
Pr. Adrian Ivanoiu
Cliniques universitaires Saint Luc
Service de neurologie
Avenue Hippocrate 10
B-1200 Bruxelles