Lancement du dosage sanguin de la p-tau217 en Belgique : une avancée majeure dans le diagnostic de la maladie d’Alzheimer
Jean-Louis Bayart1-4, Lise Colmant2,5, Emilien Boyer2, Lara Huyghe2, Lisa Quenon2,5, Thomas Gerard2,6, Pascal Kienlen-Campard2, Renaud Lhommel2,6, Adrian Ivaniou2,5, Jonathan Douxfils3, Bernard Hanseeuw2
La maladie d’Alzheimer est une maladie neurodégénérative caractérisée par l’accumulation de plaques amyloïdes (amyloïdopathie) et la formation d’enchevêtrements neurofibrillaires constitués de protéine tau (tauopathie) (1). Ces deux dernières décennies, l’émergence de biomarqueurs, notamment via la tomographie par émission de positons (PET) ou l’analyse du liquide céphalorachidien, a permis d’affiner ce diagnostic, mais ces méthodes restent coûteuses et/ou invasives.
Récemment, des avancées considérables ont été réalisées quant à la mise au point de biomarqueurs sanguins reflétant le processus physiopathologique sous-jacent, justifiant même depuis peu leur intégration dans les critères diagnostiques du groupe de travail de l’« Alzheimer’s Association » (2). Parmi les biomarqueurs sanguins, la protéine tau phosphorylé en position 217 (p-tau217) fait l’objet d’un intérêt croissant au cours des dernières années en raison de sa capacité à refléter précocement les dépôts amyloïdes et tau, caractéristiques de la maladie (3-4).
Une étude menée par l’Institute of NeuroScience (IoNS) de l’UCLouvain a validé l’utilisation clinique du dosage plasmatique de la p-tau217 sur une cohorte de plus de 200 patients présentant divers stades de la maladie. Les résultats montrent que les concentrations de p-tau217 sont en moyenne 450% plus élevées chez les patients atteints par la maladie. Un seuil de 0,193 pg/mL offre une sensibilité de 95% et une spécificité de 94% (Figure 1), avec une corrélation forte entre les concentrations sanguines et la sévérité de la tauopathie, telle qu’objectivée au PET.
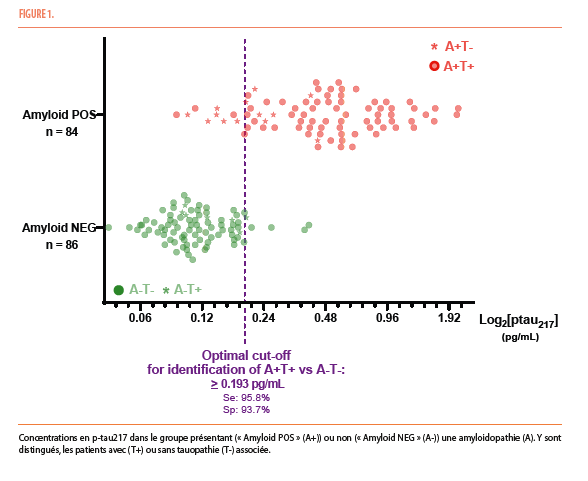
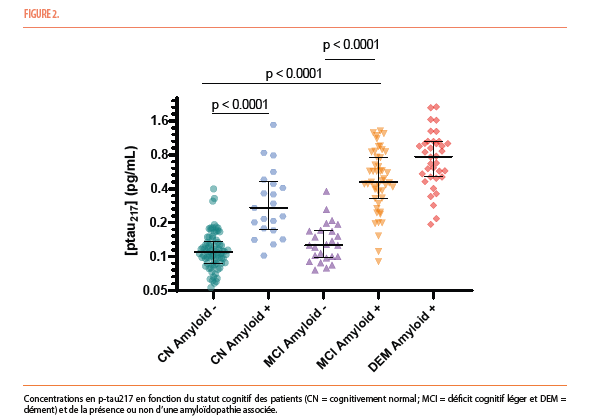
La p-tau217 augmentant même déjà avant l’apparition du déclin cognitif chez les patients présentant déjà une amyloidopathie au PET (Figure 2). Ceci s’aligne à d’autres données récentes rapportées dans la littérature ; la protéine p-tau217 sanguine démontrant même des performances comparables à la ponction lombaire dans plusieurs études (5-6).
Fort de ces résultats, le réseau H.UNI est désormais le premier réseau à proposer ce test sanguin dans le paysage Belge. « La question n’est en effet pas de savoir si les biomarqueurs sanguins vont arriver en routine clinique mais bien « quand ? ». Les données de la littérature et les guidances vont toutes en ce sens et il est dès lors important de cadrer l’utilisation de ce test pour éviter toute dérive future. Ce biomarqueur n’est donc pas destiné à être utilisé dans le cadre d’un dépistage de masse auprès d’individus cognitivement normaux. Il s’adresse exclusivement aux patients présentant des troubles cognitifs objectivés par un médecin et confirmés par un examen neuropsychologique si le MMSE est supérieur ou égal à 24/30. En effet, l’objectif du test est de confirmer le processus physiopathologique sous-jacent, pas de dépister une pathologie asymptomatique pour laquelle aucun traitement préventif n’existe actuellement. La caractérisation de certains facteurs confondants potentiels sera également importante (fonction rénale, antécédents d’AVC ou de trauma crânien, etc.) ; en effet, parmi les quelques cas faussement positifs, un patient souffrait d’insuffisance rénale chronique (eGFR = 20 Ml/min/1.73 m2) et un avait subi un trauma crânien récent. » déclarent le Professeur Bernard Hanseeuw (Neurologue aux Cliniques Universitaires Saint-Luc et chercheur à l’IoNS) et Jean-Louis Bayart (Pharmacien Biologiste à la Clinique Saint-Pierre d’Ottignies et aux Cliniques Universitaires Saint-Luc, doctorant à l’IoNS et à l’UNamur), principaux investigateurs de cette étude.
Enfin, les biomarqueurs sanguins, dont la p-tau217, devraient également à termes jouer un rôle crucial dans l’identification des patients éligibles aux futurs traitements ciblant la maladie d’Alzheimer. En effet, le Lecanemab, un anticorps monoclonal dirigé contre les agrégats amyloïdes, a récemment été approuvé par l’Agence européenne des médicaments (EMA). L’utilisation de la p-tau217 pourrait faciliter la sélection des patients avec troubles cognitifs susceptibles de bénéficier de ces nouvelles thérapies.
Références
- Dubois B, Villain N, Frisoni GB et al. Clinical diagnosis of Alzheimer’s disease: Recommendations of the International Working Group. Lancet Neurol. 2021;20(6):484-96.
- Jack CR Jr, Andrews JS, Beach TG et al. Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup. Alzheimers Dement. 2024;20(1):11-26.
- Ashton N, Brum W, Di Molfetta G et al. Diagnostic Accuracy of a Plasma Phosphorylated Tau 217 Immunoassay for Alzheimer Disease Pathology. JAMA Neurol. 2024 ; 81(3) :255-263.
- Milà-Alomà, M, Ashton, NJ, Shekari, M et al. Plasma p-tau231 and p-tau217 as state markers of amyloid-β pathology in preclinical Alzheimer’s disease. Nat Med. 2022 ; 28, 1797–1801.
- Therriault J, Servaes S, Tissot C, et al. Equivalence of plasma p-tau217 with cerebrospinal fluid in the diagnosis of Alzheimer’s disease. Alzheimer’s Dement. 2023; 19: 4967–4977.
- Ashton NJ, Puig-Pijoan A, Milà-Alomà M, et al. Plasma and CSF biomarkers in a memory clinic: Head-to-head comparison of phosphorylated tau immunoassays. Alzheimer’s Dement. 2023; 19: 1913–1924.
Affiliations
1. Department of Laboratory Medicine, Clinique Saint-Pierre, Ottignies
2. Institute of NeuroScience (IoNS), Université Catholique de Louvain, Bruxelles
3. Unité de Recherche en Pharmacologie et Toxicologie Clinique, Université de Namur
4. Department of Laboratory Medicine, Cliniques universitaires Saint-Luc, Bruxelles
5. Department of Neurology, Cliniques universitaires Saint-Luc, Bruxelles
6. Department of Nuclear Medicine, Cliniques universitaires Saint-Luc, Bruxelles
Correspondance
Dr Jean-Louis Bayart
Cliniques Saint-Pierre
Department of Laboratory Medicine
Avenue Reine Fabiola 9
B-1348 Ottignies Louvain-la-Neuve
jean-louis.bayart@cspo.be