Les nouveaux inhibiteurs de JAK2 dans la myélofibrose
Violaine Havelange, Stefan N. Constantinescu
Introduction
La myélofibrose (primitive ou post-polycythemia vera/thrombocytémie essentielle) est la néoplasie myéloproliférative la plus agressive. La myélofibrose se caractérise par l’accumulation de fibres collagène qui désorganisent l’environnement de la moelle osseuse et entravent l’hématopoïèse. Cette néoplasie myéloproliférative est induite le plus souvent par une des 3 mutations drivers (JAK2V617F, CALR, MPL) qui vont activer constitutivement la tyrosine kinase JAK2 et les voies de signalisation en aval (STAT, PI3K/AKT/mTOR and the RAS/MAPK). Les mégacaryocytes (et les monocytes) activés par JAK2, vont sécréter entre autres du TGF-β1 et des cytokines pro-inflammatoires responsables de l’activation de différents types cellulaires dans la matrice extracellulaire et du développement de la fibrose. La fibrose est responsable d’une érythropoïèse inefficace (anémie), d’expression cytokinique aberrante (symptômes constitutionnels et cachexie) et d’une hématopoïèse extra médullaire (hépatosplénomégalie). Ces patients ont une survie médiane médiocre de 5 à 7 ans et une pauvre qualité de vie due aux complications de la maladie. Les patients deviennent rapidement transfusion dépendants. Ils peuvent développer une hépatosplénomégalie avec une hypertension portale. Enfin, les risques de transformation en phase blastique sont élevés (9-12% à 10-17 ans).
Les inhibiteurs de JAK2
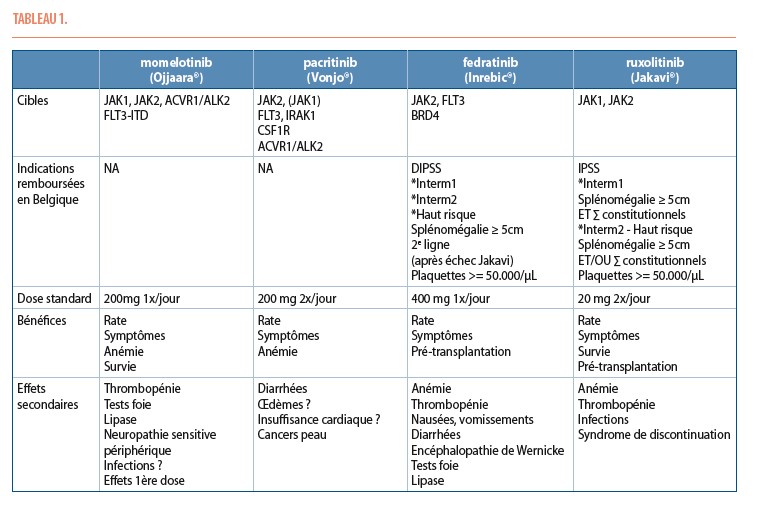
Actuellement, 4 inhibiteurs de JAK2 ont été approuvés par la FDA dans le traitement de la myélofibrose dont 2 plus récemment : momelotinib (15/09/2023) – pacritinib (28/02/2022) – fedratinib (16/08/2019) et ruxolitinib (16/11/2011). Ce sont des petites molécules inhibiteurs ATP compétitifs de la kinase mais non sélectifs de JAK2. Leur spectre d’inhibition est différent et est repris dans la table 1 (1,2).
Le ruxolitinib (Jakavi®) est le 1er inhibiteur de JAK approuvé en Belgique dans le traitement de la myélofibrose (3). Il est remboursé pour des patients avec un score pronostique IPSS intermédiaire 1 ayant une splénomégalie ≥ 5cm sous le rebord costal ET des symptômes constitutionnels ou -un IPSS intermédiaire 2 - haut risque avec une splénomégalie ≥ 5cm sous le rebord costal ET/OU des symptômes. Le ruxolitinib n’est pas sélectif de la forme mutée. Il inhibe JAK2 et donc l’érythropoïèse et la thrombopoïèse mais également JAK1 et la surveillance immunitaire. Le ruxolitinib permet de réduire la taille de la rate de > 35% et les symptômes constitutionnels chez 30-40% des patients (études COMFORT-I/II). Les effets secondaires principaux sont l’anémie (dans les 3 premiers mois de traitement) et la thrombopénie (Table 1). On observe également un gain pondéral avec une majoration des taux de cholestérol et triglycérides. Ces patients peuvent présenter des infections urinaires et une réactivation d’herpès zoster (zona 6%), d’hépatite B ou de tuberculose. Il y a également une suspicion d’augmentation des risques de cancers de la peau non-mélanome et de lymphomes B diffus à grandes cellules. Un arrêt brutal du ruxolitinib est déconseillé car il peut mener à un syndrome de discontinuation avec une augmentation rapide du volume de la rate et un syndrome de relargage des cytokines pouvant s’avérer très sévère. La durée médiane de la réponse au ruxolitinib est de 3.2 ans. 73% des patients arrêtent le ruxolitinib dans les 5 ans par suite d’un manque de réponse, une perte de réponse, une progression en phase blastique ou une intolérance. Le phénomène de ‘persistance’ a été décrit : les cellules mutées continuent à croître malgré leur sensibilité au ruxolitinib. Le mécanisme physiopathologique n’est pas connu. Le ruxolitinib est responsable d’un bénéfice clinique mais n’a pas d’impact majeur sur le clone muté et pas d’effet significatif sur les risques de progression. Certaines mutations comme ASXL1, EZH2, RAS peuvent être acquises durant le traitement par ruxolitinib. Le bénéfice du ruxolitinib sur la survie reste modéré. C’est pour ces raisons que d’autres inhibiteurs de JAK2 ont été développés.
Le fedratinib (Inrebic®), un inhibiteur de JAK2/FLT3 est le 2e inhibiteur de JAK approuvé dans la myélofibrose. Le fedratinib permet une diminution de la splénomégalie > 35% chez 47% des patients en 1re ligne et 31% en 2e ligne après intolérance ou résistance au ruxolitinib (JAKARTA-1/2). Il permet également une diminution des symptômes constitutionnels chez 30-40% des patients comme le ruxolitinib. Le fedratinib est actuellement remboursé en Belgique depuis septembre 2023 chez les patients en 2e ligne de traitement après échec du ruxolitinib ayant un score DIPSS intermédiaire 1-2 - haut risque avec une splénomégalie ≥ 5cm sous le rebord costal. Le fedratinib est responsable d’une toxicité gastrointestinale fréquente (Table 1). Un risque majoré d’encéphalopathie de Wernicke favorisé par une carence en vitamine B1 due à ces troubles digestifs a été décrit. Il est recommandé de substituer les patients en vitamine B1 et de suivre leur taux sanguin durant le traitement. En outre, on observe également comme effet secondaire une anémie, thrombopénie, toxicité hépatique, majoration de la créatinine, des lipases et des infections.
Le pacritinib est un inhibiteur de JAK2/FLT3 mais également d’IRAK1 qui régule la synthèse de cytokines pro-inflammatoires et d’ACVR1/ALK2. Le pacritinib n’est actuellement pas remboursé en Belgique. Le pacritinib permet une diminution de la splénomégalie > 35% chez 19% des patients en 1re ligne et 32% en 2e ligne après intolérance ou résistance au ruxolitinib (PERSIST-1/2). Ses effets secondaires sont principalement digestifs de type diarrhées (Tableau 1). Le ruxolitinib et le fedratinib sont contre-indiqués en cas de thrombopénie sévère de grade 3 (< 50.000/µL). Le pacritinib a été testé chez ce sous-groupe de patients avec une thrombopénie sévère (n=189 ; taux médian de plaquettes : 28.000/µL) (4). Il a permis un effet bénéfique sur la splénomégalie (23%) et les symptômes (27%) sans excès de saignement ni modification de dose. Le taux de plaquettes est resté bas mais stable sous pacritinib. Une étude de phase III (Pacificia) comparant le pacritinib versus Best Available Therapy est en cours chez ce sous-groupe de patients présentant une thrombopénie sévère. La pacritinib aurait également un effet bénéfique sur l’anémie par son action sur ACVR1/ALK2. 37% des patients sont devenus transfusion indépendants sous pacritinib versus 7% dans le bras contrôle dans l’étude PERSIST-2 (5).
Le momelotinib est un inhibiteur de JAK1/JAK2 mais aussi d’ACVR1/ALK2 qui est une kinase qui transduce le signal de BMP6 qui via la voie de signalisation des SMAD2/3 régule la synthèse hépatique d’hepcidine (6). L’hepcidine inhibe l’efflux cellulaire du fer par liaison et dégradation de la ferroportine. La voie de signalisation de SMAD2/3 est impliquée dans l’inhibition de la maturation érythroïde terminale et dans l’érythropoïèse inefficace. Le momelotinib diminue l’expression de l’hepcidine, restaure l’homéostasie du fer et stimule l’érythropoièse. Le momelotinib n’est actuellement pas remboursé en Belgique. Le momelotinib est responsable d’une diminution des symptômes, de la splénomégalie mais principalement d’une majoration du pourcentage de patients qui deviennent transfusion indépendant en 1re ou 2e ligne de traitement (SIMPLIFY 1-2). Ses effets secondaires sont principalement une thrombopénie, une majoration des tests hépatiques ou des lipases, une polyneuropathie sensitive périphérique, un effet 1re dose et une augmentation des infections (Tableau 1). Le momelotinib a été comparé au ruxolitinib en 1re ligne de traitement dans l’étude SIMPLIFY-1. Le taux d’indépendance transfusionnelle était de 66.5% sous momelotinib versus 49.3% sous ruxolitinib (7). Ce gain en besoins transfusionnels a été associé à une survie générale majorée (8). Vu ses effets bénéfiques sur la qualité de vie à savoir sur l’anémie, la splénomégalie, les symptômes constitutionnels/cachexie, le momelotinib pourrait devenir l’inhibiteur de JAK2 de choix en 1re ligne dans le futur (9).
Conclusion
Depuis 10 ans, les inhibiteurs de JAK2 ont indéniablement permis une amélioration de la qualité de vie des patients traités pour une myélofibrose. La majorité des patients présentent une diminution des symptômes constitutionnels (et de la cachexie) et de la taille de la splénomégalie. Les 2 inhibiteurs développés plus récemment (pacritinib et momelotinib) ont de plus un effet bénéfique sur l’anémie et diminuent la dépendance aux transfusions. Le pacritinib semble lui sécure en cas de thrombopénie sévère.
Malheureusement, ces inhibiteurs ont des effets secondaires, une durée d’action limitée, un manque d’activité sur le clone muté, sur la fibrose, sur les taux des blastes et un effet bénéfique modéré sur la survie. Des études cliniques récentes ont combiné le ruxolitinib avec des nouvelles molécules; ce qui permet une meilleure réponse sur la splénomégalie et les symptômes mais pas de modification de la maladie (10).
L’allogreffe de cellules souches périphériques reste le seul traitement curatif actuel de la myélofibrose mais elle n’est pas accessible à tous les patients vu leur âge ou comorbidités.
Les développements d’inhibiteur sélectif de JAK2V617F ou de JAK2WT activé par les mutants CALR ou MPL est donc indispensable. Les premiers tests d’un anticorps monoclonal et d’un anticorps bispécifique contre la protéine calreticuline mutée exprimée à la surface du clone myéloprolifératif semblent prometteurs et seront à suivre attentivement dans les mois à venir (11,12).
Références
- Tefferi A. Primary myelofibrosis: 2023 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023 May;98(5):801-821. doi: 10.1002/ajh.26857. Epub 2023 Feb 6.
- Vainchenker W, Yahmi N, Havelange V, Marty C, Plo I, Constantinescu SN. Recent advances in therapies for primary myelofibrosis. Fac Rev. 2023 Sep 26;12:23. doi: 10.12703/r/12-23. eCollection 2023.
- Devos T, Selleslag D, Granacher N, Havelange V, Benghiat FS. Updated recommendations on the use of ruxolitinib for the treatment of myelofibrosis. Hematology. 2022 Dec;27(1):23-31. doi: 10.1080/16078454.2021.2009645.
- Verstovsek S, Mesa R, Talpaz M, Kiladjian JJ, Harrison CN, Oh ST et al. Retrospective analysis of pacritinib in patients with myelofibrosis and severe thrombocytopenia. Haematologica. 2022 Jul 1;107(7):1599-1607.
- Oh ST, Mesa RA, Harrison CN, Bose P, Gerds AT, Gupta V et al. Pacritinib is a potent ACVR1 inhibitor with significant anemia benefit in patients with myelofibrosis. Blood Adv. 2023 Oct 10;7(19):5835-5842.
- Tefferi A, Pardanani A, Gangat N. Momelotinib (JAK1/JAK2/ACVR1 inhibitor): mechanism of action, clinical trial reports, and therapeutic prospects beyond myelofibrosis. Haematologica. 2023 Nov 1;108(11):2919-2932. doi: 10.3324/haematol.2022.282612.
- Mesa RA, Kiladjian JJ, Catalano JV, et al. SIMPLIFY-1: a phase III randomized trial of momelotinib versus ruxolitinib in Janus kinase inhibitor-naive patients with myelofibrosis. J Clin Oncol. 2017;35(34):3844-3850.
- Mesa R, Harrison C, Oh ST, Gerds AT, Gupta V, Catalano J, et al. Overall survival in the SIMPLIFY-1 and SIMPLIFY-2 phase 3 trials of momelotinib in patients with myelofibrosis. Leukemia. 2022 Sep;36(9):2261-2268. doi: 10.1038/s41375-022-01637-7
- Tefferi A, Pardanani A, Gangat N. Momelotinib expands the therapeutic armamentarium for myelofibrosis: Impact on hierarchy of treatment choices. Am J Hematol. 2024 Feb;99(2):300-308. doi: 10.1002/ajh.27163. Epub 2024 Jan 2.
- Gill H, Leung GMK, Kwong YL. Evolving landscape of JAK inhibition in myelofibrosis: monotherapy and combinations. Hematology Am Soc Hematol Educ Program. 2023 Dec 8;2023(1):667-675.
- Reis E, Buonpane R, Celik H, Marty C, Lei A, Jobe F, et al. Discovery of INCA033989, a Monoclonal Antibody That Selectively Antagonizes Mutant Calreticulin Oncogenic Function in Myeloproliferative Neoplasms (MPNs). Blood. 2022; 140, 14–15.
- Kuchnio et al. Discovery of JNJ-88549968, a Novel, First-in-Class CALRmutxCD3 T-Cell Redirecting Antibody for the Treatment of Myeloproliferative Neoplasms. Blood. 2023; 142, 1777-1779.
Hématologie « Bénigne » : PF4, hémophilie acquise, Fer IV et PTI réfractaire à l’honneur
Cédric Hermans, Catherine Lambert
Thrombose et thrombopénie : l’importance de rechercher les anticorps anti-PF4
Une patiente de 35 ans se présente avec des céphalées sévères et une thrombocytopénie (49.000 plaquettes/µL). La concentration des D-dimères est fortement élevée (>35 000 µg/L). Une thrombose veineuse cérébrale (TVC) est mise en évidence par résonance magnétique nucléaire. Ses antécédents médicaux se limitent à une infection récente des voies respiratoires supérieures environ 2 semaines auparavant. Cette patiente est en bonne santé et ne prend aucun médicament autre que sa contraception hormonale. Dans le décours de l’instauration d’un traitement par héparine, la TVC progresse.
La combinaison d’une thrombose et d’une thrombocytopénie motive la recherche d’anticorps anti-PF4. Celle-ci s’est avérée positive par ELISA. Un test de confirmation d’activation plaquettaire dépendant de l’héparine se révèle toutefois négatif. Malgré une majoration du nombre de plaquettes, la patiente développe une hémorragie intracérébrale secondaire et décède.
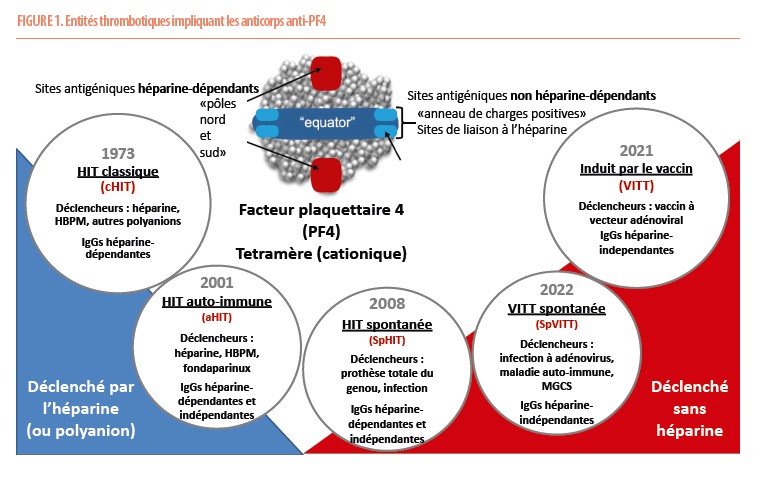
Le facteur plaquettaire 4 (FP4) est une molécule chargée positivement qui est stockée dans les granules alfa des plaquettes. Secrété lors de l’activation plaquettaire, le FP4 se lie physiologiquement aux glycosaminoglycans dotés de charges électriques négatives et présents à la surface endothéliale dont il neutralise leurs propriétés anticoagulantes. Le PF4 contribue donc au processus d’hémostase et à la formation de thrombi. Le PF4 peut également se lier à diverses substances exogènes chargées négativement telles que les héparines. Ceci entraîne la formation d’un nouvel antigène, cible d’une réponse immunitaire. Le développement d’anticorps dirigés contre le PF4 est relativement fréquent. Toutefois, seuls les anticorps anti-PF4 qui activent les plaquettes provoquent des troubles prothrombotiques graves avec thrombocytopénie associée.
Le prototype de maladie thrombotique liée au PF4 est sans conteste la thrombopénie à l’héparine (TIH). Cette entité est médiée par une forte activation par les anticorps anti-PF4/héparine des plaquettes via leurs récepteurs FcγIIa (FcγRIIa). L’activation pancellulaire concomitante (monocytes, neutrophiles, endothélium) déclenche un état thrombo-inflammatoire associé à un risque élevé de thrombose tant veineuse qu’artérielle. Les IgG anti-PF4/héparine, reconnaissent des sites antigéniques sur le PF4 cationique qui se forment en présence d’héparine anionique. Ce sont ces anticorps dépendants de l’héparine qui causent la TIH. En conséquence, la TIH est gérée par une anticoagulation avec un anticoagulant non héparinique.
En 2021, les vaccins COVID-19 utilisant les vecteurs adénoviraux ont été associés à de rares cas de « thrombocytopénie thrombotique immunitaire induite par le vaccin » ou TTIV. Il a été rapidement établi que cette entité était également causée par des IgG anti-PF4. La TTIV est un trouble d’activation plaquettaire toutefois indépendant de l’héparine. Cet état prothrombotique nécessite à la fois une anticoagulation à dose thérapeutique et une inhibition de l’activation plaquettaire médiée par le FcγRIIa par des immunoglobulines intraveineuses à haute dose (IVIG). Il est aujourd’hui établi que les anticorps responsables de la TIH et TTIV se lient à différents épitopes sur le PF4. De nouveaux tests immunologiques peuvent différencier ces anticorps distincts de type TIH et TTIV.
Par ailleurs, chez certains patients présentant une thrombose aiguë sévère avec thrombopénie (et parfois chronique ou récurrente), des anticorps de type TTIV peuvent être identifiés indépendamment d’une exposition récente à l’héparine ou d’une vaccination. Ceci suggère l’implication d’autres antigènes.
Il a été récemment proposé de classer les anticorps anti-PF4 en type 1 (non pathogènes, non activateurs de plaquettes), type 2 (dépendants de l’héparine, activateurs de plaquettes) et type 3 (indépendants de l’héparine, activateurs de plaquettes).
Face à toute thrombose associée à une thrombopénie, il est recommandé d’exclure la présence d’anticorps anti-PF4. Si de tels anticorps sont détectés, leur dépendance à l’héparine et capacité à activer les plaquettes doit être évaluée. S’il s’agit d’un TIH, l’éviction de l’héparine et une anticoagulation sans héparine sont formellement indiquées. La détection d’anticorps de type 3 (TIH auto-immune, TTIV) nécessite une anticoagulation associée à l’administration d’immunoglobuline intraveineuse à haute dose, pour désamorcer l’état d’hypercoagulabilité médié par les IgG anti-PF4 (Figure 1).
Hémophilie A acquise : prise en charge révolutionnée par l’emicizumab
Une femme de 53 ans se présente au service des urgences avec des ecchymoses étendues spontanées. Son temps de céphaline activée (TCA) est mesuré à 82 secondes (21 à 31 secondes) avec un temps de prothrombine normal et un fibrinogène de 4,3 g/L. Les tests de la fonction hépatique sont normaux. Elle a accouché de 4 enfants par césarienne sans complication hémorragique. Un mélange plasmatique ne permet pas de corriger le TCA. Le FVIII est indosable.
L’hémophilie A acquise (AHA) est une maladie auto-immune rare caractérisée par le développement d’auto-anticorps circulants qui inhibent le facteur VIII (FVIII) - appelés inhibiteurs. Son incidence estimée est de 1 à 1,5 cas pour 1 million de personnes, avec une prévalence plus élevée chez les patients âgés. Dans la plupart des cas, l’AHA est suspectée lors de l’apparition soudaine de manifestations hémorragiques graves et spontanées, surtout à un âge avancé, chez des individus sans antécédents personnels ou familiaux d’hémorragie. Dans certains cas, le diagnostic est posé même en l’absence de symptômes hémorragiques évidents et suggéré par un TCA prolongé de manière significative.
Les principaux symptômes de l’AHA sont des hématomes musculaires et des tissus mous, souvent étendus et conduisant à une anémie grave et/ou une compression nerveuse. Des hémorragies internes ou compliquant des gestes invasifs sont également fréquents Contrairement à l’hémophilie A congénitale, les saignements articulaires sont rares. D’autres symptômes peuvent inclure des saignements muqueux (épistaxis, saignement des gencives, métrorragies) et des saignements graves potentiellement mortels tels que des hémorragies gastro-intestinales, des hématomes rétropéritonéaux et des hémorragies intracrâniennes.
La moitié des cas d’AHA est associée à une pathologie sous-jacente, telle que des maladies auto-immunes, le cancer, l’utilisation de certains médicaments. L’AHA peut survenir durant la grossesse ou le postpartum. Dans l’autre moitié, aucune cause sous-jacente n’est identifiée. Reconnaître les patients atteints d’AHA est un défi en raison de l’hétérogénéité de la présentation clinique et du fait que cette condition n’est pas rapidement diagnostiquée, entraînant d’importants retards de traitement. La mortalité dans l’AHA est élevée, en particulier chez les patients âgés. Bien que l’hémorragie représente moins de 10% des décès, elle contribue à une morbidité considérable.
La prise en charge de l’AHA nécessite une approche globale, abordant plusieurs aspects, tels que l’évitement des procédures susceptibles de déclencher des saignements, le contrôle des épisodes aigus de saignement, l’éradication des inhibiteurs pour prévenir d’autres saignements et le traitement de la maladie sous-jacente.
Divers agents hémostatiques sont classiquement utilisés pour gérer les saignements. Ils ont en commun de court-circuiter le FVIII inhibé et/ou de ne pas être reconnus par les anticorps anti-FVIII. Il s’agit du concentré du complexe prothrombine activé (aPCC), du facteur VII activé recombinant (rFVIIa), ainsi du FVIII porcin (pFVIII).
Malgré leur efficacité pour favoriser l’hémostase, ces agents présentent certaines limitations, telles que l’administration intraveineuse, une demi-vie courte nécessitant des injections répétées, un contrôle hémorragique insatisfaisant, un suivi complexe de l’activité hémostatique, un potentiel thrombogène et des défis dans le traitement préventif.
L’éradication des anticorps implique l’utilisation de corticostéroïdes, de cyclophosphamide et de rituximab, ou d’autres immunosuppresseurs, seuls ou en combinaison. Cet aspect du traitement peut être très difficile, en particulier pour les patients âgés, et peut avoir un impact significatif sur leur morbidité et mortalité. Le choix du traitement dépend des concentrations résiduelles du FVIII et du titre de l’inhibiteur. La cause du décès est souvent liée au traitement immunosuppresseur et à la maladie sous-jacente.
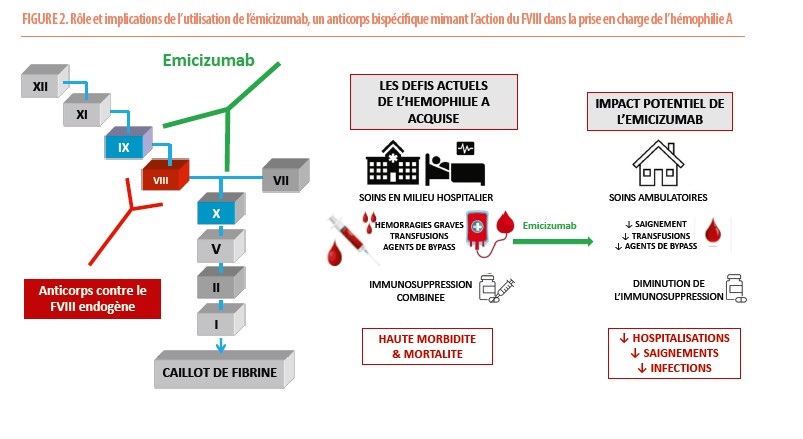
L’introduction de nouveaux agents thérapeutiques, tels que l’émicizumab, a récemment révolutionné la prise en charge de l’hémophilie A congénitale. Il s’agit d’un anticorps bispécifique qui mime l’activité catalytique du FVIII en se liant d’une part au FIXa et au FX dont il permet l’activation. Cet anticorps s’administre par voie sous-cutanée et permet de maintenir une activité hémostatique constante équivalent à 15-20% de FVIII. Aujourd’hui, l’émicizumab est devenu un traitement standard pour l’hémophilie A congénitale sévère, indépendamment de la présence d’inhibiteurs.
De études récentes rapportent l’efficacité de l’emicizumab pour prévenir les complications hémorragiques de l’AHA. L’utilisation de l’émicizumab dans l’AHA limite le recours aux autres agents hémostatiques et permet de postposer un traitement immunosuppresseur potentiellement dangereux chez des patients ayant un état général précaire (Figure 2).
Fer intraveineux et hypophosphatémie : une association méconnue
Une femme de 23 ans se présente avec une fatigue progressive et une tolérance à l’exercice diminuée. En raison d’une suspicion de carence en fer due à des saignements menstruels abondants, il lui avait été conseillé de prendre du fer oral, mais des troubles gastro-intestinaux limitent son adhérence. Les analyses de laboratoire révèlent une anémie ferriprive : hémoglobine à 7,8 g/dL et ferritine à 4 ng/mL. Elle est orientée vers un traitement intraveineux (IV) de fer et une prise en charge gynécologique des saignements menstruels abondants. Elle reçoit 2 doses hebdomadaires de fer carboxymaltose (FCM) (fer(III) (carboxymaltose) Injectafer), 750 mg chacune. Une semaine plus tard, elle continue de ressentir de la fatigue et de la faiblesse, et elle décrit de nouvelles douleurs musculaires. Son médecin attribue initialement ces symptômes à une carence en fer et estime qu’ils se résoudront bientôt, mais les symptômes progressent, l’amenant à se présenter aux urgences pour une évaluation plus approfondie. Les analyses de laboratoire révèlent une amélioration de l’hémoglobine, mais un taux de phosphate sérique de 0,9 mg/dL (normal : 2,6-4,6 mg/dL), nécessitant une admission en hospitalisation.
La thérapie par fer intraveineux (IV) est largement utilisée pour traiter l’anémie par carence en fer car c’est un moyen plus efficace et plus rapide pour reconstituer les réserves de fer par rapport au fer oral. Plusieurs formulations de fer IV existent, mais de nouveaux agents tels que le FCM, le derisomaltose ferrique (FDI) (Fer(III) dérisomaltose, Monoferric) permettent l’administration de fortes doses de fer en 1 à 2 perfusions. Malgré ces avancées, l’hypophosphatémie après l’administration de fer IV, qui était autrefois considérée comme bénigne et autolimitée, est désormais reconnue comme un effet indésirable grave de certaines formulations de fer IV, notamment le FCM.
Plusieurs essais randomisés et une revue systématique et méta-analyse complètes ont rapporté une incidence significativement plus élevée d’hypophosphatémie, allant de 47% à 75%, chez les personnes traitées par FCM par rapport à <10% parmi les patients traités par d’autres formulations.
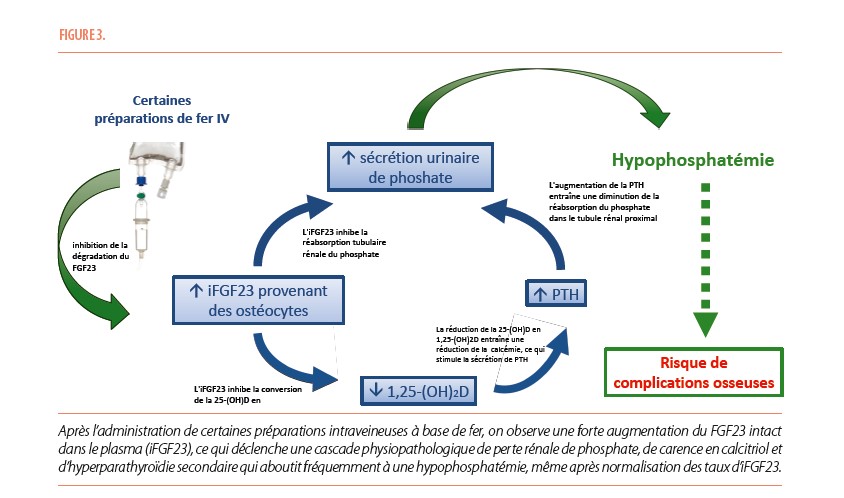
La perfusion de FCM provoque des augmentations aiguës de 3 à 6 fois des concentrations circulantes de facteur de croissance des fibroblastes-23 (FGF23), qui, avec le 1,25-dihydroxyvitamine D et la parathormone (PTH), est l’un des principaux régulateurs du phosphate sérique. Le pic de FGF23 entraîne une excrétion urinaire inappropriée de phosphate en raison d’une réabsorption tubulaire proximale réduite du phosphate filtré. En conséquence, les niveaux de phosphate atteignent généralement leur nadir environ 2 semaines après la première perfusion de FCM. Le FGF23 diminue également les concentrations circulantes de 1,25-dihydroxyvitamine D, conduisant à une absorption réduite de phosphate par l’intestin, à une diminution du calcium sérique et à des augmentations secondaires de PTH. Puisque la PTH augmente également l’excrétion rénale de phosphate, l’hypophosphatémie induite par le FCM est maintenue au-delà de la période initiale d’élévation du FGF23 par une seconde vague d’élimination rénale du phosphate médiée par la PTH.
En plus de la formulation spécifique de fer IV, d’autres facteurs de risque d’hypophosphatémie induite par le FCM incluent une fonction rénale normale, une carence en fer sévère, un poids corporel faible, un phosphate sérique de base plus bas, des saignements utérins anormaux comme étiologie de la carence en fer, et des doses répétées de fer IV. Les patients atteints de maladie rénale sont partiellement protégés de l’hypophosphatémie induite par le FCM en raison de la filtration glomérulaire réduite du phosphate, limitant ainsi l’excrétion urinaire de phosphate. Malgré ces constatations, il est important de souligner que même les patients sans facteurs de risque identifiés peuvent développer une hypophosphatémie sévère et prolongée après avoir reçu du FCM, et il reste difficile de prédire avec précision le risque, la gravité ou la durée de l’hypophosphatémie chez les patients individuels.
Les manifestations cliniques aiguës de l’hypophosphatémie induite par le fer IV comprennent l’asthénie, la fatigue et les myalgies, qui reflètent tous une déplétion énergétique spécifique des tissus due à une diminution de la production d’adénosine triphosphate (ATP). Les cas plus graves peuvent causer des douleurs osseuses, une myopathie, une arythmie cardiaque, une insuffisance respiratoire, une encéphalopathie et des convulsions. Anecdotiquement, de nombreux patients signalent un brouillard cérébral, peut-être comme conséquence de la déplétion de l’ATP dans le cerveau. Les symptômes de l’hypophosphatémie peuvent imiter ceux de l’anémie ferriprive, ce qui contribue probablement à des diagnostics manqués ou retardés chez de nombreux patients affectés. L’hypophosphatémie chronique, en particulier chez ceux traités par des doses répétées de FCM, peut entraîner des complications musculo-squelettiques, y compris une ostéomalacie et des fractures de fragilité.
La gestion de l’hypophosphatémie induite par le fer IV est un défi. La supplémentation en phosphate oral et IV ne maintient pas durablement un phosphate sérique normal en raison de la fuite rénale continue de phosphate causée par l’élévation du FGF23 et de la PTH. La supplémentation en 1,25-dihydroxyvitamine D peut aider à corriger l’hyperparathyroïdie secondaire, mais l’évidence scientifique de son utilisation dans l’hypophosphatémie induite par le fer IV est limitée. De plus, la supplémentation en phosphate et en 1,25-dihydroxyvitamine D sont des stimuli connus du FGF23, limitant leur efficacité. Par conséquent, la prévention primaire de l’hypophosphatémie en utilisant des formulations de fer autres que le FCM est préférée. Lorsque les formulaires obligent l’utilisation du FCM, nous recommandons un dosage du phosphate sérique à la semaine 1, avant d’administrer la deuxième perfusion de FCM. Si un patient manifeste déjà une hypophosphatémie, la deuxième dose doit être évitée pour prévenir l’exacerbation de l’hypophosphatémie. De plus, nous recommandons que le risque d’hypophosphatémie et ses conséquences potentielles soient discutés avec les patients avant toute perfusion.
Malgré la forte incidence de l’hypophosphatémie induite par le fer IV, de nombreux médecins ne sont toujours pas conscients et ne reconnaissent pas les complications aiguës et à long terme du FCM. Il est impératif d’éviter le FCM chez les patients qui nécessitent des doses de fer IV répétées (Figure 3).
Le récepteur FcRn, la tyrosine kinase de Bruton, le CD38 et le complément: nouvelles cibles du traitement du PTI
Une femme de 38 ans connue depuis 10 ans pour un PTI réfractaire aux corticoïdes, ayant répondu transitoirement au Rituximab, déjà traitée sans succès par agonistes du récepteur de la thrombopoïétine et bénéficiant mensuellement d’administrations intraveineuses d’immunoglobulines, consulte pour second avis et exploration des alternatives thérapeutiques.
La thrombocytopénie immunitaire (PTI) est une maladie hémorragique acquise auto-immune qui résulte de la combinaison d’une destruction accrue des plaquettes dans le système réticulo-endothélial et d’une compensation inadéquate de la production des plaquettes. De nombreux mécanismes physiopathologiques ont été étudiés et démontrés dans le PTI.
Le traitement aigu du PTI repose sur l’administration de corticostéroïdes et les immunoglobulines intra-veineuses. En 2024, l’arsenal thérapeutique du PTI à moyen et long terme inclut les agonistes du récepteur de la thrombopoïétine (TPO-RAs), le Rituximab, le Fostamatimib et la splénectomie. La plupart des patients atteints de PTI sont pris en charge avec succès par les traitements standards et approuvés actuellement. Les cas de PTI réfractaires ne sont toutefois pas rares. Il existe donc un besoin de nouvelles thérapies pour le PTI, essentiellement chez des patients réfractaires et lourdement prétraités.
Les antagonistes du récepteur néonatal Fc
Le récepteur néonatal Fc (FcRn) joue un rôle crucial dans le recyclage des immunoglobulines G (IgG) et de l’albumine. Les IgG qui se lient aux FcRn endosomaux sont préservés de leur dégradation dans les lysosomes, ce qui prolonge la demi-vie des IgG circulantes, sans impact sur l’albumine et les autres isotypes d’immunoglobulines. Les antagonistes du FcRn ont donc le potentiel de réduire la demi-vie des IgG circulantes et leur concentration plasmatique. Leur intérêt thérapeutique s’étend à des pathologies auto-immunes dont le PTI et la myasthénie. L’Efgartigimod est en cours de validation dans l’indication du PTI dans les études de phase 3 ADVANCE IV et ADVANCE SC. La validation du Rozanolixizumab dans le PTI est interrompue pour des raisons stratégiques de la firme qui le produit.
Les inhibiteurs de la tyrosine kinase de Bruton
La tyrosine kinase de Bruton (BTK) joue un rôle essentiel dans la voie de signalisation des récepteurs Fcγ médiés des macrophages, dans la maturation des cellules B et la production des anticorps. L’inhibition de BTK est un traitement prometteur du PTI compte tenu de son potentiel sur la production des autoanticorps et la destruction des plaquettes par phagocytose. Contrairement à d’autres BTK inhibiteurs, le Rizalbrutinib a la particularité d’être hautement sélectif, ce qui permet de préserver la fonction plaquettaire. Cette sélectivité permet également de réduire l’inhibition de la voie PI3K-AKT et donc de limiter le risque de toxicités comme la fibrillation auriculaire. Les études de phase 1 et 2 évaluant le Rizalbrutinib ont démontré une augmentation significative et durable des plaquettes chez 40% des participants (des PTI réfractaires chroniques dont certains multi-traités). La tolérance au traitement était bonne (surtout des événements gastro-intestinaux de grade 1 ou 2-transitoires). Une étude de phase 3 (LUNA 3) est en cours pour évaluer le Rizalbrutinib dans le PTI.
La déplétion plasmocytaire en ciblant CD38
Les plasmocytes médullaires et spléniques contribuent à la production des auto-anticorps dans le PTI. Les anticorps monoclonaux anti-CD38, déjà approuvés dans le myélome, sont donc une nouvelle piste dans le traitement du PTI. Le Daratumumab (étude DART) et le Mezagitamab sont en cours d’évaluation dans le PTI.
Les inhibiteurs du complément
Dans le PTI, les auto-anticorps liés aux plaquettes sont capables de fixer le complément, générant des dépôts de C3b sur la membrane plaquettaire qui vont entraîner la phagocytose et la destruction des plaquettes opsonisées. De plus, le complexe d’attaque membranaire contribue à la destruction plaquettaire. Cibler le complément constitue donc une nouvelle approche dans le PTI réfractaire. Deux molécules sont en cours d’étude dans ce domaine.
Le Sutimlimab, un anticorps monoclonal humanisé qui inhibe sélectivement le complexe C1 du complément et prévient son activation tout en préservant les voies alternes et de la lectine (et donc limite le risque d’infection à germes encapsulés). L’inhibition de la voie classique du complément réduit les dépôts de C3 et par conséquent atténue l’activation des cellules B auto-réactives et diminue la destruction des plaquettes. Le Sutimlimab, déjà approuvé par la FDA pour la maladie à agglutinines froides, est en étude de phase 1 pour le PTI.
L’Iptacopan, un inhibiteur oral sélectif du facteur B, réduit la C3 convertase de la voie alterne du complément et donc la production de C3a, C5a et du complexe d’attaque membranaire. L’Iptacopan est en cours d’investigation pour le PTI dans une étude de phase 2.
Nous assistons à une période florissante et encourageante dans le développement de médicaments pour le PTI réfractaire. Il convient de souligner que la validation et l’implémentation de ces nouvelles thérapies devra prendre en compte la qualité de vie liée à la santé, les bénéfices et les toxicités potentielles dans le cadre d’un trouble de la coagulation pour lequel peu de patients souffrent d’hémorragies mettant leur vie en danger.
Références
- Poston J, Kruse-Jarres R. The role of emicizumab in acquired hemophilia A. Hematology Am Soc Hematol Educ Program. 2023 Dec 8;2023(1):24-30. doi: 10.1182/hematology.2023000462
- Tiede A. Immunotherapy of acquired hemophilia A. Hematology Am Soc Hematol Educ Program. 2023 Dec 8;2023(1):19-23. doi: 10.1182/hematology.2023000461.
- Tiede A, Hart C, Knöbl P, Greil R, Oldenburg J, Sachs UJ, et al. Emicizumab prophylaxis in patients with acquired haemophilia A (GTH-AHA-EMI): an open-label, single-arm, multicentre, phase 2 study. Lancet Haematol. 2023 Nov;10(11):e913-e921. doi: 10.1016/S2352-3026(23)00280-6. Epub 2023 Oct 16.
- H. Al-Samkari and E.J. Neufeld. Novel therapeutics and future directions for refractory immune thrombocytopenia. British Journal of Haematology 2023; 203:65-78.
- Song AB, Al-Samkari H. Adenovirus-associated thrombosis and thrombocytopenia: an emerging anti-PF4 disorder. Haematologica. 2024 Feb 8. doi: 10.3324/haematol.2023.284460.
- Greinacher A, Warkentin TE. Thrombotic anti-PF4 immune disorders: HIT, VITT, and beyond. Hematology Am Soc Hematol Educ Program. 2023 Dec 8;2023(1):1-10.
- Dorgalaleh A, Shabannezhad A, Hassani S. COVID-19 vaccine-induced immune thrombotic thrombocytopenia: pathophysiology and diagnosis. Ann Hematol. 2023 Nov 30. doi: 10.1007/s00277-023-05563-1.
- Liu Z, Li L, Zhang H, Pang X, Qiu Z, Xiang Q, Cui Y. Platelet factor 4(PF4) and its multiple roles in diseases. Blood Rev. 2023 Nov 23:101155. doi: 10.1016/j.blre.2023.101155.
- Van Doren L, Steinheiser M, Boykin K, Taylor KJ, Menendez M, Auerbach M. Expert consensus guidelines: Intravenous iron uses, formulations, administration, and management of reactions. Am J Hematol. 2024 Jan 29. doi: 10.1002/ajh.27220. Online ahead of print
Actualités dans la prise en charge du myélome
Marie-Christiane Vekemans
Le traitement d’induction chez les patients éligible à la greffe, les triplettes enterrées…
Pas trois mais quatre drogues chez les patients éligibles à la greffe
En Belgique, le standard de traitement pour les patients avec un nouveau diagnostic de myélome multiple (NDMM) éligibles à la greffe consiste en un traitement d’induction associant un inhibiteur du protéasome (IP), un immunomodulateur (IMiD) et la dexamethasone suivi d’une chimiothérapie intensive avec autogreffe, puis d’un traitement de maintenance avec lénalidomide. Nous n’avons accès qu’au schéma VTD (bortezomib, thalidomide, dexamethasone) alors que le schéma VRD (bortezomib, lenalidomide, dexamethasone) est largement utilisé dans la plupart des pays. Mais le standard de traitement actuellement reconnu consiste en une quadruplette qui inclut le daratumumab, un anticorps monoclonal anti-CD38. Dans le contexte de greffe, cette molécule a fait l’objet de différentes études, que ce soit en association avec VTD (CASSIOPEIA)(1) ou VRD (GRIFFIN)(2), avec un bénéfice clinique significatif en terme de taux de réponse, de maladie résiduelle (MRD) ou de survie sans progression (SPP).
Lors du dernier congrès américain d’Hématologie à San Diego en décembre 2023, ont été rapportés les résultats de l’essai de phase 3 PERSEUS qui a étudié la combinaison du daratumumab au VRD (3), avec comme objectif principal, la SSP. Plus de 700 patients ont été inclus dans cet essai. Avec un suivi médian de 47 mois, l’objectif principal de l’essai est atteint avec une SSP très significativement supérieure dans le bras dara-VRD (SSP à 4 ans de 84% contre 67% dans le bras VRD (HR = 0,42)). Cet avantage est retrouvé pour tous les sous-groupes de patients, notamment ceux présentant un haut risque cytogénétique. Le pourcentage de patients obtenant une réponse complète ou mieux (≥RC) est plus élevé dans le bras dara-VRD (88% vs. 70%), de même que le pourcentage de patients atteignant une MRD négative (75% vs. 47%). Cet essai PERSEUS, publié maintenant dans le New England Journal of Medicine (4), permettra nous l’espérons, d’obtenir l’approbation de la combinaison dara-VRD chez les patients éligibles à l’autogreffe. Les résultats d’efficacité sont très impressionnants, avec une SSP médiane qui sera probablement proche de 10 ans, confirmant la transformation du pronostic du myélome déjà amorcée depuis plusieurs années.
Une autre étude a fait l’objet d’une présentation en séance plénière à ce congrès. Il s’agit de l’étude IsKia qui a investigué, chez des patients éligibles à la greffe, l’apport de l’isatuximab, un autre anticorps monoclonal anti-CD38, au schéma KRD (carfilzomib, lénalidomide, dexaméthasone), en induction pré-greffe et en consolidation post-greffe (5). L’objectif primaire de l’étude était l’évaluation du taux de MRD négative à 10-5 par NGS après la consolidation.
Un total de 302 malades a été inclus dans l’essai, avec près de 20% d’entre eux considérés à haut risque (HR) cytogénétique (del (17p) et/ou t(4 ;14) et/ou t(14 ;16)), 9%, à ultra HR (double ‘hit’, incluant del (17p) et/ou t(4 ;14) et/ou t(14 ;16) et gain/amp(1q)). L’addition d’isatuximab au schéma KRD permet d’augmenter de manière significative le taux de MRD (77% vs 67% dans le bras KRD (p = 0,049)), et ce, à toutes les phases de traitement et quel que soit le risque cytogénétique (76% chez les HR, 77% chez les double hit, taux comparable aux patients avec risque standard (SR)(79%)). Avec un suivi médian de 20 mois, il n’y a pas de différence en termes de SSP, la SSP à un an étant de 95% dans les 2 bras.
Au total, ces données enterrent définitivement l’induction par une triplette, qu’elle soit de type VRd ou KRd, et confirment le rôle d’une induction à base d’une quadruplette utilisant un anticorps monoclonal.
Iberdomide, un bon candidat pour la maintenance après autogreffe ?
Le lénalidomide est le standard de traitement en maintenance après autogreffe, avec un bénéfice démontré à la fois en termes de SSP et de survie globale. L’iberdomide est un modulateur de la cereblon E3 ligase, une molécule apparentée aux IMiDs, dont l’affinité pour sa cible est 20 fois plus forte que celle du lénalidomide ou du pomalidomide. Cette molécule est testée avec succès chez des patients atteints de MM en rechute avancée, réfractaire au lénalidomide et au pomalidomide.
L’étude EMN26 (6) est une étude de phase 2 menée dans 4 pays européens, qui a évalué 3 doses d’iberdomide administré en maintenance après autogreffe, avec comme objectif principal, l’amélioration de la réponse après autogreffe. L’étude a inclus 111 patients dans les différentes cohortes, les résultats rapportés concernent les 69 patients ayant reçu au moins 6 cycles de traitement, ou l’ayant interrompu pour une raison ou une autre. En terme d’efficacité, les résultats encore préliminaires sont encourageants avec un doublement du taux de RC/RC stringente entre l’inclusion et la fin du 6e cycle (passage de 26 et 29% à 50 et 60% respectivement pour les cohortes de 1 et 1,3 mg). Cette amélioration de la réponse se compare favorablement avec les résultats historiques obtenus avec le lénalidomide en entretien. La tolérance de l’iberdomide est très proche de celle observée avec le lénalidomide, les principaux effets indésirables de grade 3 ou 4 concernant des neutropénies, infections ou des plaintes de fatigue.
La prise en charge des rechutes dominée par l’immunothérapie
Teclistamab, premières données de vie réelle
Le teclistamab est un anticorps bispécifique anti-BCMAxCD3 approuvé pour le traitement des patients atteints de MM en rechute après au moins 3 lignes de traitement et exposés aux 3 classes thérapeutiques (IMiD, IP et anticorps anti-CD38), sur base de l’étude d’enregistrement MajesTEC-1. Après avoir bénéficié d’un accès précoce, cet anticorps est maintenant remboursé en Belgique depuis la fin de l’année 2023.
Les données de vie réelle sont capitales pour évaluer l’efficacité de ces nouvelles options thérapeutiques dans une population de patients moins sélectionnée que dans les essais cliniques. Les données de vie réelle de 102 patients traités dans 5 centres aux États-Unis ont été rapportées récemment (7). Il s’agit de patients en rechute (médiane de 6 lignes antérieures), réfractaires aux 3 classes thérapeutiques pour 92% d’entre eux. Point important, plus de 80% de ces patients ne remplissaient pas les critères d’inclusion de l’étude d’enregistrement MajesTEC-1, une proportion importante d’entre eux (55%) ayant déjà reçu un traitement anti-BCMA, les autres présentant un mauvais état général (ECOG ≥2, 28%) ou des cytopénies de grade 3-4 (26%). En terme de tolérance, 65% des patients ont présenté un syndrome de relargage des cytokines (CRS), tous de grade 1 ou 2, à l’exception d’un patient, ce qui est très semblable à ce qui est rapporté dans l’étude MajesTEC-1. En terme d’efficacité, avec un suivi médian très court (3 mois), le taux de réponse globale est de 64%, résultats semblables à ceux de l’étude d’enregistrement. En revanche, la SSP médiane n’est que de 5 mois, très inférieure aux 11 mois rapportés dans l’étude princeps.
Prédire la réponse au teclistamab ?
Malgré des taux de réponse excellents chez des patients présentant un MM en phase très avancée, environ un tiers d’entre eux ne répond pas au teclistamab (résistance primaire), et la grande majorité des patients répondeurs perdent leur réponse et finissent par progresser (résistance secondaire).
De manière à mieux appréhender ces phénomènes de résistance, une analyse des biomarqueurs de réponse a été conduite chez les patients traités par teclistamab dans l’étude MajesTEC-1 (8). Ni l’expression pré-thérapeutique de BCMA ni l’expression du BCMA soluble ne sont associés à la réponse au traitement. De plus, l’analyse des cellules tumorales à la progression ne signale pas de différence d’expression de BCMA, montrant que la perte de BCMA ne semble pas un mécanisme fréquemment impliqué dans la résistance secondaire, bien que des mutations de BCMA ne puissent être exclues. En revanche, le phénotype T semble un mécanisme majeur de résistance. En effet, la présence et la persistance d’un phénotype T « épuisé » (notamment expression LAG3, PD-1) sont plus fréquemment observées chez les patients non répondeurs, de même qu’une expression élevée de lymphocytes Treg immunosuppresseurs. Ces résultats soulignent l’importance d’une système immunitaire ‘en bonne forme’, de façon à maintenir la réponse aux anticorps bispécifiques.
La connaissance de ces mécanismes de résistance primaire et/ou secondaire à ces anticorps est indispensable pour identifier les patients les plus à même de répondre ou non, mais également pour permettre de déterminer les meilleures combinaisons (IMiD, anti-PD-1, etc.) et les meilleures séquences de traitement.
Infection sous anticorps bispécifiques anti-BCMA, données de vie réelle
Si on ne peut nier l’efficacité des anticorps bispécifiques chez les patients atteints de MM en phase avancée, il est bien établi que les infections sont un des effets indésirables les plus fréquents de cette classe thérapeutique.
Une étude rétrospective multicentrique (14 centres français de l’IFM) a colligé les données ayant trait à l’incidence et aux caractéristiques des infections chez 229 patients atteints de MM traités par anticorps bispécifiques ciblant BCMA (n = 200) ou GPRC5D (n = 29)(9). Après un suivi médian de 7 mois, 2/3 des patients ont présenté une infection, pour la moitié de grade >3 et ayant conduit à une hospitalisation dans 56% des cas, au décès dans 9% (20 patients). En majorité, ces infections surviennent au cours des 6 premières semaines de traitement et sont principalement bactériennes (56%), moins fréquemment virales (38%, dont 8 cas de CMV et 2 cas d’infections à JC virus). Il s’agit essentiellement d’infections respiratoires et de bactériémies. Le risque d’infection est plus élevé chez les patients traités par anti-BCMA (versus GPRC5D) et ceux ayant reçu une corticothérapie pour le traitement d’un CRS/ICANS.
Ces données de vie réelle sont fondamentales pour améliorer la prise en charge d’infections survenant sous anticorps bispécifiques, pour lesquelles les recommandations internationales insistent sur la prophylaxie (immunoglobulines, valaciclovir, cotrimoxazole, vaccinations, etc.).
Anticorps bispécifique, vers une association aux immunomodulateurs ?
Talquetamab, encore mieux avec le pomalidomide
Le talquetamab est un anticorps bispécifique qui cible GPRC5DxCD3 et qui a démontré son efficacité dans l’étude MONUMENTAL-1 chez des patients atteints de MM en rechute après au moins 3 lignes de traitement et exposés aux 3 classes thérapeutiques. Plusieurs études évaluent maintenant les possibilités de combiner un bispécifique avec un IMiD, lénalidomide ou pomalidomide, sur base de leurs propriétés de promouvoir l’activité des lymphocytes T. Dans l’étude de phase Ib MONUMENTAL-2, 35 patients avec un nombre médian de 3 traitements antérieurs, ont été inclus dans une cohorte associant le pomalidomide au talquetamab (10). Avec un suivi médian d’environ 1 an, le taux de réponse globale est de 94% (talquetamab 0,4 mg/kg hebdomadaire) et 84% (talquetamab 0,8 mg/kg toutes les 2 semaines), et la SSP à 9 mois est de 93% et 75% respectivement pour ces 2 dosages. Les principales toxicités de grade 3-4 sont hématologiques (neutropénie, 54%) et infectieuses (22%, dont 15% d’infections pulmonaires). Près de la moitié des patients ont dû bénéficier d’une réduction de dose du pomalidomide en raison d’effets indésirables. Les autres effets indésirables retrouvés sont liés au talquetamab et concernent un CRS (74%), et les toxicités cutanéo-muqueuses habituelles, essentiellement de grade 1/2. Ces résultats très prometteurs justifient les essais cliniques en cours évaluant les associations bispécifiques - agent immuno-modulateur.
CAR-T anti-BCMA, vers une utilisation dès la 2e ou la 3e ligne ?
Les CAR-T sont actuellement disponibles dans de nombreux pays -mais pas en Belgique- pour le traitement des patients atteints de MM en rechute après au moins 3 lignes de traitement et exposés aux 3 classes thérapeutiques.
L’essai de phase 3 KarMMa-3 a comparé l’ide-cel, CAR-T anti-BCMA, à différents traitements standard (dara-pomalidomide-dexaméthasone, dara-Vd, ixazomib-lénalidomide-dexaméthasone, carfilzomib-dexaméthasone ou élotuzumab-pomalidomide-dexaméthasone) chez 386 patients en rechute après 2 à 4 lignes de traitement.
Cette étude initialement publiée en 2023 dans le New England Journal of Medicine (11) a fait l’objet d’une mise à jour, avec un suivi médian actuel de 31 mois (12). L’objectif principal de l’étude, la SPP, est atteint avec un avantage très significatif de SSP avec une médiane de 13,8 mois pour ide-cel, contre 4,4 mois pour le bras contrôle (HR = 0,49 ; p < 0,0001). Cette actualisation confirme également un avantage significatif en SSP2 (23,5 contre 16,7 mois), montrant que le bénéfice en SSP est maintenu en incluant la ligne thérapeutique suivante. Ce suivi plus long ne met pas en évidence de nouveaux signaux de tolérance, en particulier, pas de toxicité neurologique tardive (syndrome parkinsonien, Guillain-Barré) comme cela a pu être observé avec d’autres CAR-T anti-BCMA. Cette actualisation de KarMMa-3 plaide pour une utilisation plus précoce des CAR-T, avant la 4e ligne comme c’est le cas actuellement dans les programmes d’accès précoce.
Dès la première rechute, l’autre CAR-T anti-BCMA, cilta-cel, a également démontré des résultats spectaculaires dans le cadre de l’essai de phase 3 CARTITUDE-4, chez des patients réfractaires au lénalidomide (13). On espère donc un accès rapide à cette thérapeutique pour nos patients dès la première rechute !
CAR-T, deux ciblent valent mieux qu’une… !
Améliorer l’efficacité des CAR-T est d’une importance capitale, cibler 2 antigènes tumoraux est certainement une des voies d’amélioration potentielles.
Dans une étude de phase 1, des auteurs chinois ont proposé un CAR-T dénommé GC012F, dirigé contre BCMA et CD19, et dont une des particularités repose sur une capacité de fabrication très courte (24-48 h)(14). Ce CAR a été étudié chez des patients atteints de NDMM, ayant des facteurs de mauvais pronostic (del (17p), t(4;14), t(14;16) ou amp(1q), ou une maladie extramédullaire). Avec un suivi médian de 13,6 mois, ce CAR testé chez 22 malades permet d’obtenir 100% de réponse globale, 96% de RC stringente, et une MRD négative avec un seuil de sensibilité à 10-6 chez tous les patients, dès le premier mois. Les durée médiane de réponse et de SPP ne sont pas atteintes à ce stade. Sur le plan de la tolérance, un CRS a été rapporté chez 6 patients (27%), mais de bas grade (grades 1 et 2). Il n’y a pas eu de cas de neurotoxicité ou de décès toxique, et une expansion rapide et robuste du CAR a été observée.
Ces données extrêmement encourageantes confortent le concept d’un ciblage double des CAR-T dans le MM. La pertinence d’utiliser le CD19 en tant que cible pourrait être mise en balance avec d’autres antigènes tumoraux comme le GPRC5D.
Références
- Moreau P, Hulin C, Perrot A, Arnulf B, Belhadj K, Benboubker L, et al. Maintenance with daratumumab or observation following treatment with bortezomib, thalidomide, and dexamethasone with or without daratumumab and autologous stem cell transplantation in patients with newly diagnosed multiple myeloma (CASSIOPEIA): an open-label, randomized, phase 3 trial. Lancet Oncol. 2021; 22(10): 1378-1390.
- Voorhees PM, Sborov DW, Laubach J, Kaufman JL, Reeves B, Rodriguez C, et al. Addition of daratumumab to lenalidomide, bortezomib, and dexamethasone for transplant-eligible patients with newly diagnosed multiple myeloma (GRIFFIN): final analysis of an open-label, randomized, phase 2 trial. Lancet Haematol. 2023; 10(10): e825-e837.
- Sonneveld P, Dimopoulos MA, Boccadoro M, Quach H, Ho PJ, Beksac M, et al. Phase 3 randomized study of daratumumab (dara) + borteomib, lenalidomide, and dexamethasone (VRd) versus VRd alone in patients (pts) with newly diagnosed multiple myeloma (NDMM) who are eligible for autologous stem cell transplantation (ASCT): primary results of the Perseus trial. Blood. 2023; 142(suppl 2): LBA-1.
- Sonneveld P, Dimopoulos MA, Boccadoro M, Quach H, Ho PJ, Beksac M, et al. Phase 3 randomized study of daratumumab (dara) + borteomib, lenalidomide, and dexamethasone (VRd) versus VRd alone in patients (pts) with newly diagnosed multiple myeloma (NDMM) who are eligible for autologous stem cell transplantation (ASCT): primary results of the Perseus trial. NEJM. 2024 ; 390 :301-313.
- Gay F, Roeloffzen W, Dimopoulos MA, Rosinol L, van der Klift M, Mina R, et al. Results of the phase 3 randomized Iskia trial: isatuximab-carfilzomib-lenalidomide-dexamethasone vs carfilzomib-lenalidomide-dexamethasone as pre-transplant induction and post-transplant consolidation in newly diagnosed multiple myeloma patients. Blood. 2023; 142(suppl 1): 4.
- Van den Donck NWCJ, Touzeau C, Terpos E, Perrot A, Mina R, de Ruijter M, et al. Iberdomide maintenance after autologous stem cell transplantation in newly diagnosed MM: first results of the phase 2 EMN26 study. Blood. 2023; 142(suppl 1): 208.
- Dima D, Davis DJ, Ahmed N, Sannareddy A, Shaikh H, Mahmoudjafari Z, et al. Real-world safety and efficacy of teclistamab for patients with heavily pretreated relapsed-refractory multiple myeloma; Blood. 2023; 142(suppl 1): 3330.
- Vishwamitra DS, Skerget S, Cortes D, Perova T, Lau O, Davis C, et al. Longitudinal correlative profiles of responders, ninresponders, and those with relapse on treatment with teclistamab in the phase 1/2 MajesTEC-1 study of patients with relapsed/refractory multiple myeloma. Blood. 2023; 142(suppl 1): 455.
- Cellerin E, Jourdes A, Brousse X, Vallet N, Cartau T, Denis B, et al. Cumulative incidence and characteristics of infections requiring treatment, delay in treatment administration or hospitalization in patients with relapsed or refractory multiple myeloma treated with anti-BCMA or anti-GPRC5D bispecific antibodies. Blood. 2023; 142(suppl 1): 1005.
- Matous JV, Biran N, Perrot A, Berdej aJG, Dorritie K, van Elssen J, et al. Talquetamab + pomalidomide in patients with relapsed/refractory multiple myeloma: safety and preliminary efficacy results from the phase 1b MonumenTAL-2 study. Blood. 2023; 142(suppl 1): 1014.
- Rodriguez-Otero P, Ailawadhi S, Arnulf B, Patel K, Cavo M, Nooka AK, et al. Ide-cel or standard regimens in relapsed and refractory multiple myeloma. NEJM. 2023; 388: 1002-1014.
- Rodriguez-Otero P, Ailawadhi S, Arnulf B, Patel K, Cavo M, Nooka AK, et al. Ide-cel or standard (std) regimens in patients with triple-class exposed (TCE) relapsed and refractory multiple myeloma (RRMM): an updated analysis from KarMMa-3. Blood. 2023; 142 (suppl 1): 1028.
- San Miguel J, Dhakal B, Yong K, Spencer A, Anguille S, Mateos MV, et al. Cilta-cel or standard care in lenalidomide-refractory multiple myeloma. N Engl J Med. 2023; 389: 335-347.
- Du J, Qiang W, Lu J, Jia Y, He H, Liu J, et al. Updated results of a phase 1 open-label single-arm study of dual targeting BCMA and CD19 Fastcar-T celles (GC012F) as first-line therapy for transplant-eligible newly diagnosed high-risk multiple myeloma. Blood. 2023; 142 (suppl 1): 1022.
Affiliations
1. Service d’hématologie, Cliniques universitaires Saint-Luc, Bruxelles, Belgique.
2. Université catholique de Louvain and de Duve Institute, Bruxelles, Belgique.
3. Ludwig Institute for Cancer Research Brussels, Bruxelles, Belgique.
4. Wel Research Institute, WelBio Department, Havren, Belgique.
5. Ludwig Institute for Cancer Research, Nuffield Department of Medicine, Oxford University, Oxford, UK.
Correspondance
Pre Violaine Havelange
violaine.havelange@saintluc.uclouvain.be
Pr Cédric Hermans
cedric.hermans@saintluc.uclouvain.be
Pre Marie-Christiane Vekemans
marie-christiane.vekemans@saintluc.uclouvain.be
Cliniques universitaires Saint-Luc
Service d’Hématologie
Avenue Hippocrate 10
B-1200 Bruxelles