La néphropathie reste en 2020 une complication fréquente et redoutable du diabète sucré (1). Dans nos pays occidentaux, elle s’impose comme la première cause d’insuffisance rénale. Une enquête récente aux États-Unis rapporte d’ailleurs qu’elle concerne directement 36.0% des patients diabétiques de type 1 et 2 (2). Cette néphropathie est associée, entre autres, à une augmentation de la mortalité globale et des décès cardiovasculaires. La littérature l’illustre sans concession : l’étude NHANES III (Nutrition Health and Examination Survey) rapporte que les incidences cumulées de mortalité, toutes causes confondues, et de décès cardiovasculaires sont très augmentées chez les sujets diabétiques avec néphropathie (31.1 et 19.6 % respectivement au cours d’un suivi de dix ans) par rapport à ceux indemnes de maladie rénale (11.5 et 6.7 %) (3). Dans l’enquête européenne de Tancredi et al., le risque de décès d’origine cardiaque est multiplié par un facteur 30 chez les diabétiques de type 2 âgés de moins de 55 ans au stade de l’insuffisance rénale terminale (IRT) vs. l’absence de pathologie rénale (4).
L’approche thérapeutique de cette néphropathie est conventionnellement fondée sur l’optimisation glycémique, le contrôle de l’hypertension artérielle, le blocage de l’axe rénine-angiotensine et la maîtrise des autres facteurs de risque (5). Récemment, il a été rapporté dans la littérature scientifique que l’administration de metformine aux patients diabétiques de type 2 était associée à un certain degré de néphroprotection (6-8).
Le but de cet article est de proposer un état des lieux concernant la relation clinique dans le diabète de type 2 entre les « nouveaux » médicaments antidiabétiques, en particulier les DDP- 4 inhibiteurs, les agonistes du GLP-1 et les gliflozines, et la néphroprotection qu’ils amèneraient, en termes de fonction rénale et/ou d’albuminurie.
Quelles classes de médicaments sont concernées ?
Inhibiteurs de la dipeptidyl peptidase 4 (DPP-4 i) (gliptines)
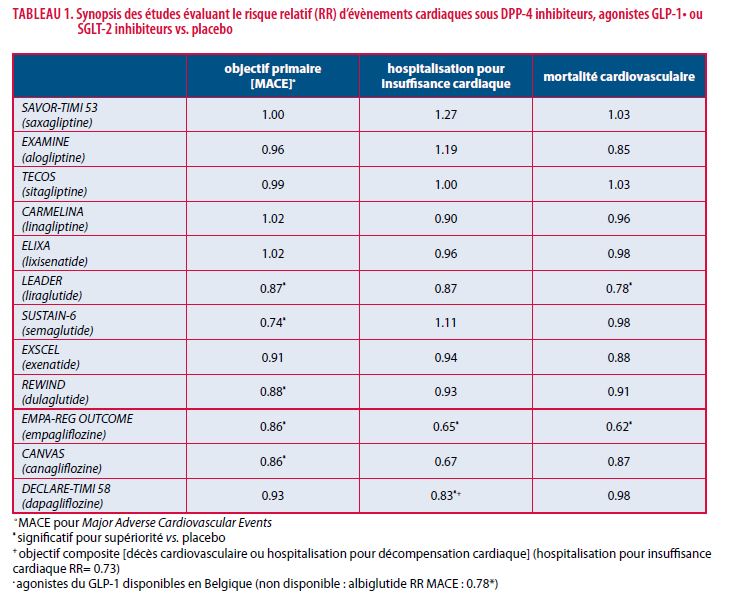
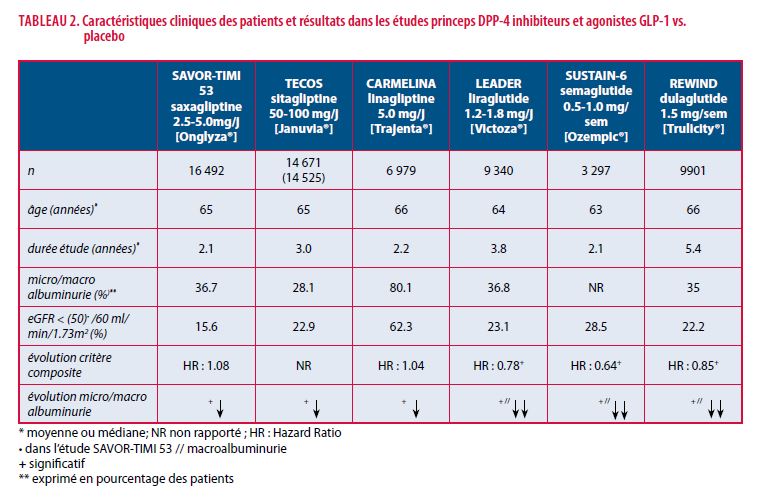
La littérature scientifique a mis en relief, au cours des dernières années, l’intérêt clinique patent des DPP-4 i sur le contrôle glycémique des diabétiques de type 2. Ils trouvent ainsi leur place dans l’algorithme thérapeutique, tel que proposé aujourd’hui par les Sociétés savantes de diabétologie (9). Les principales études interventionnelles (SAVOR-TIMI 53, EXAMINE, TECOS et CARMELINA) ont également démontré la sécurité des DDP-4 i et leur neutralité cardiovasculaire, tant au niveau des MACE (Major Adverse Cardiovascular Events) [décès cardiovasculaires, infarctus ou accident vasculaire cérébral non fatal] que des hospitalisations pour insuffisance cardiaque ou des décès d’origine cardiovasculaire (10-13) (Tableau1). Seuls SAVOR-TIMI 53 et EXAMINE avaient mis en évidence une légère augmentation du risque d’hospitalisation pour décompensation cardiaque (10,11). Ces essais, en particulier SAVOR-TIMI 53, TECOS et CARMELINA, avaient en outre comme objectif d’analyser l’évolution de la fonction rénale et l’excrétion urinaire d’albumine vs. un groupe contrôle (Tableau 2). Il est intéressant, dans ce contexte, de mentionner que sitaglitine (Januvia®), saxagliptine (Onglyza®), alogliptine (Vipidia®) et vildagliptine (Galvus®) peuvent être prescrits en présence d’une insuffisance rénale, à condition qu’il y ait ajustement de la posologie alors qu’aucune adaptation de dose n’est requise pour la linagliptine (Trajenta®), dont le métabolisme est extrarénal.
SAVOR-TIMI 53 (pour Saxagliptin Assessment of Vascular Outcomes recorded in patients with diabetes mellitus - Thrombolysis In Myocardial Infarction 53) [saxagliptine/placebo] a inclus 16 492 sujets à risque cardiovasculaire dont la majorité (84.4 %) avait une fonction rénale normale ou légèrement altérée (eGFR > 50 ml/min/1.73m2) (pour estimated Glomerular Filtration Rate). L’eGFR était de [30-50 ml/min] ou [< 30 ml/min] respectivement chez 13.6 % et 2.0 % des participants. Une micro – ou une macroalbuminurie était constatée chez 26.8 et 9.9 % des sujets (14). Au cours d’un suivi de 2.1 années (médiane), le risque d’événements rénaux (doublement de la créatinine sérique, IRT [dialyse ; transplantation ; créatinine > 6 mg/dl] ou décès d’origine rénale) était comparable dans les bras saxagliptine et placebo (HR : 1.08 [95 % IC 0.96-1.22]). Le déclin de la eGFR au cours de l’étude était également identique dans les deux groupes (-2.49 vs.-2.36 ml/min/1.73m2, p=0.57) . Un résultat comparable avait été retrouvé après 18 mois dans l’étude EXAMINE (Examination of Cardiovascular Outcomes with Alogliptin versus Standard of Care) (n=5 380) [alogliptine/placebo] chez des diabétiques de type 2 aux antécédents récents d’événements coronaires, quel que soit leur degré d’eGFR à l’inclusion (11). En revanche, le traitement par saxagliptine était associé à une réduction significative de l’excrétion urinaire d’albumine avec une différence [saxagliptine-placebo] de 19.3 mg/g de créatinine (si eGFR à l’inclusion > 50 ml/min/1.73m2) (p=0.033), de 105.0 mg/g (si eGFR 30-50 ml/min) (p=0.011) et de 245, 2 mg/g (si eGFR <30 ml/min) (p=0.086) (14) (Tableau 2).
TECOS (pour Trial Evaluating Cardiovascular Outcome with Sitagliptin) [sitagliptine/placebo] a inclus 14 671 patients diabétiques de type 2 aux antécédents cardiovasculaires. Une mesure de la eGFR était disponible chez 14 525 d’entre eux. 22.9 et 54.2 % des patients étaient classés en stade 1 et 2 de néphropathie, 17.5 % et 5.4 % en stades 3A et B (≥ 90, 60-89, 45-59 et 30-44 ml/min/1.73m2 respectivement). Une micro – ou une macroalbuminurie était observée chez 23.3 et 4.8 % des sujets à l’inclusion (Tableau 2). Au cours d’un suivi de 3.0 ans, le déclin de la eGFR était légèrement plus marqué sous sitagliptine (50-100 mg/j) que sous placebo (- 4.0±18.4 vs. - 2.8±18.3 ml/min/1.73m2, p<0.001), sans qu’il n’ait de différence eu égard au degré de néphropathie à l’inclusion. Par contre, une réduction significative de l’albuminurie sous sitagliptine était objectivée au terme de l’étude (Δ sitagliptine/placebo : - 0.18 mg/g/créatinine [95 % IC : - 0.35 à - 0.02, p=0.031]) quelle que soit l’atteinte rénale à l’inclusion (15).
CARMELINA (pour CArdiovascular safety and renal Microvascular outcomeE study with LINAgliptin) [linagliptine/placebo] (n= 6 979) est l’étude qui a inclus la plus grande proportion de diabétiques à fonction rénale (très) altérée, avec 62.3 % des participants ayant une eGFR inférieure à 60 ml/min/1.73m2. La eGFR moyenne était de 54.6 ml/min/1.73m2. De plus, une micro – ou une macroalbuminurie (> 30 mg/g) était observée chez 80.1 % des sujets (Tableau 2). Les résultats de CARMELINA étaient globalement en phase avec ceux des études gliptines antérieures (14,15). À nouveau, il n’y avait aucune différence sous linagliptine (vs. contrôle) d’un objectif rénal composite (réduction ≥ 40 % de la eGFR ; IRT ; décès rénal) (RR : 1.04 [95 % IC : 0.89-1.22]). Par contre, la linagliptine réduisait de 14 % la progression de l’albuminurie au cours des 2.2 années de suivi (HR : 0.86 [95 % IC : 0.78-0.95], p=0.0034) (13) (Tableau 2).
Agonistes du récepteur GLP-1 (Glucagon Like Peptide-1)
L’efficacité des agonistes du GLP-1 dans le traitement de l’hyperglycémie chronique du diabétique de type 2 a fait le consensus (16). Ils sont habituellement administrés, en fonction de l’agent utilisé, jusqu’à une eGFR de 15-30 ml/min/1.73m2 (9). Leur intérêt clinique est encore amplifié pour certains d’entre eux (liraglutide, semaglutide, dulaglutide, albiglutide) en raison de leurs dividendes cardiovasculaires (17-20). Comme l’illustre le Tableau 1, en termes d’objectif primaire (MACE), le risque relatif vs. placebo est en effet réduit significativement, dans ces études, de 12 à 26 % (17-20). Une réduction de 9 % des MACE était aussi observée dans EXSCEL (21). Les effets des agonistes du GLP-1 dans le champ néphrologique ont principalement été évalués dans les études LEADER, SUSTAIN-6, AWARD-7 et REWIND (Tableau 2).
LEADER (pour Liraglutide Effect and Action in Diabetes : evaluation of cardiovascular outcome Results) [liraglutide (Victoza®)/placebo] a inclus 9 340 sujets à haut risque cardiovasculaire dont la eGFR moyenne était de 80 ml/min/1.73m2. Une néphropathie de stade 3 et 4 était objectivée respectivement chez 20.7 et 2.4 % des sujets et une micro – ou macroalbuminurie chez 26.3 et 10.5 %. L’essai a mis en évidence au cours d’un suivi de 3.8 ans sous liraglutide vs. placebo une réduction de 22 % du risque d’un critère rénal composite [macroalbuminurie ; doublement de la créatinine ; IRT ; décès rénal] (HR : 0.78 [95 % IC :0.67 - 0.92], p=0.003) quel que soit le degré d’atteinte rénale à l’inclusion. C’est cependant la moindre probabilité de développement ou d’aggravation d’une macroalbuminurie dans le groupe interventionnel qui in fine rend compte de ce résultat (HR : 0.74 [95 % IC : 0.60- 0.91], p=0.004). Aucune différence significative n’était notée pour les autres composants du critère rénal pluriel. Cela étant, le déclin de la eGFR était (modestement) réduit de 2 %, en particulier au stade 3 de la néphropathie (p=0.01) et l’albuminurie de 17 % (p<0.001) dans le bras liraglutide (22).
SUSTAIN-6 (pour Trial to Evaluate Cardiovascular and other long term outcomes with semaglutide in subjects with type 2 diabetes) [semaglutide (Ozempic®)/placebo] montre que la probabilité de développer ou d’aggraver, au cours d’un suivi de 2.1 années, une néphropathie [macroalbuminurie, doublement de la créatinine sérique, clairance de la créatinine < 45 ml/min/1.73m2, dialyse, transplantation] dans une cohorte de 3 297 sujets à haut risque cardiovasculaire était réduite de 36 % dans le groupe semaglutide vs. placebo (HR :0.64 [95 % IC : 0.46-0.88], p=0.005). C’est cependant à nouveau une diminution de 46 % du nombre de patients avec macroalbuminurie persistante sous semaglutide (2.7 vs. 4.9 %) qui sous-tendait l’excellence de ce résultat (HR :0.54 [95 % IC : 0.37-0.77], p=0.01) (18).
AWARD-7 (pour Assessment of Weekly Administration of LY2189 265 [dulaglutide] in diabetes) [dulaglutide (Trulicity®)/glargine (Lantus®)] a inclus 577 sujets diabétiques de type 2 traités pendant 52 semaines par dulaglutide (1.5-0.75mg/sem) ou par glargine. Tous les sujets avaient une néphropathie modérée à sévère (stades 3-4). La eGFR moyenne était de 38 ml/min/1.73m2. Une micro – ou une macroalbuminurie était retrouvée chez 83 %, 76 % et 75 % des patients respectivement dans les groupes dulaglutide 1.5 mg, 0.75 mg et glargine. Le traitement par dulaglutide a été associé à une moindre diminution de la eGFR (-0.7ml/min/1.73m2) par rapport à la glargine (- 3.3 ml/min) avec, à la 52e semaine, une eGFR à 34.0 ml/min/1.73m2 [dulaglutide 1.5 mg, p=0.005 vs. glargine], 33.8 ml/min [dulaglutide 0.75 mg, p=0.009 dulaglutide vs. glargine] et 31.3 ml/min [glargine]. Une réduction comparable de l’albuminurie était observée dans les trois bras de l’étude (-22.5 %, -20.1% et -27.1 % respectivement sous dulaglutide 1.5, 0.75 et glargine (23). Très récemment, Gerstein et al., dans l’étude REWIND, ont rapporté, au cours d’un suivi de 5.4 ans de patients dont l’eGFR à l’inclusion était de 76.9 ml/min/1.73m2, une réduction significative de 15 % d’un objectif rénal composite (HR : 0.85 [95 % CI : 0.77-0.93], p=0.0004), principalement lié à une réduction de risque de macroalbuminurie (HR : 0.77 [95 % CI : 0.68-0.87], p<0.0001) (24).
Les DDP-4 i et agonistes du GLP-1 ont donc principalement démontré un effet antiprotéinurique, ce que l’étude ELIXA en 2015 [lixisenatide (Lyxumia®) vs. placebo] avait déjà suggéré (25). Le(s) mécanisme(s) physiopathologique(s) rendant compte de ces observations sont multifactoriels. À côté de leurs effets glycémique, pondéral et tensionnel, cette classe de médicaments pourrait surtout agir directement sur le rein, via une liaison aux récepteurs GLP-1 au sein des glomérules. Ceci amènerait secondairement l’activation d’une cascade de réactions biochimiques conduisant à une réduction du stress oxydatif rénal et de l’inflammation ainsi qu’à une moindre hypoxémie (26).
Les sglt-2 inhibiteurs (gliflozines)
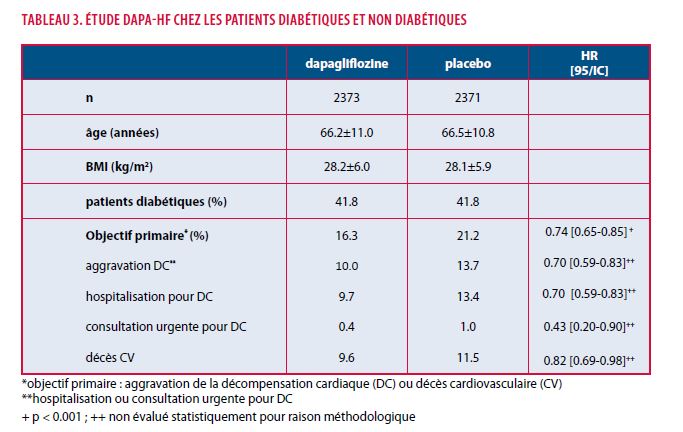
Le bénéfice glycémique et cardiovasculaire des SGLT-2 inhibiteurs (pour Sodium-Glucose Cotransporter-2) a été démontré de manière péremptoire chez les diabétiques de type 2 (Tableau 1). Dans EMPA-REG OUTCOME (Empagliflozin Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients) (99 % des patients en prévention cardiovasculaire secondaire), une réduction des MACE de 14 %, associée à une diminution du risque d’hospitalisation pour décompensation cardiaque (- 35 %) et de décès cardiovasculaire (- 38 %) a été mise en évidence (27). Des résultats globalement comparables en termes de MACE et d’insuffisance cardiaque ont été retrouvés dans CANVAS (CANagliflozin CardioVascular Assessment Study) (65.6 % des patients en prévention secondaire) (28). Enfin, dans DECLARE-TIMI 58 (Dapagliflozin Effect on Cardiovascular Events–Thrombolysis in Myocardial Infarction 58), le critère composite [décès cardiovasculaire ou hospitalisation pour insuffisance cardiaque] a également diminué de 17 %. Il faut mentionner que, dans cette étude, la majorité des sujets (59.4 %), contrairement aux deux précédentes, était en prévention cardiovasculaire primaire (29,30). Très récemment, dans l’étude DAPA-HF, publiée dans le New Engl J Med, McMurray et al. démontrent un bénéfice clinique de la dapagliflozine vs. placebo dans une cohorte de 4744 patients avec décompensation cardiaque (NYHA classe II, III, IV) et une fraction d’éjection ≤ 40 %. Comme indiqué dans le Tableau 3, l’objectif composite principal (aggravation de l’insuffisance cardiaque ou décès CV) était réduit de 26 % dans le groupe dapagliflozine (IC : 0.65-0.85, p < 0.001). Important, ces résultats remarquables étaient constatés tant chez les patients diabétiques que non diabétiques (31).
Des essais en cours comme EMPEROR et EMPERIAL avec l'empagliflozine devraient prochainement rapporter d'autres résultats dans le champ de l'insuffisance cardiaque à fraction d'éjection réduite ou préservée. Toutes ces études ont également mis en évidence une « plus-value » rénale (par rapport au placebo) (même si l’efficacité antihyperglycémique per se de cette classe de médicaments s’émousse sous un seuil d’eGFR < 60 ml/min/1.73m2). Elles ont inclus majoritairement des diabétiques à fonction rénale « normale » ou légèrement altérée, avec une eGFR moyenne au-delà de 70 ml/min/1.73m2 et une albuminurie normale chez plus de la moitié des sujets (Tableau 4) (28,30,32). Le Tableau 5 montre sous gliflozines vs. placebo une réduction de 24 à 40 % du risque de survenue d’un objectif rénal préspécifié : empagliflozine : HR : 0.61 [95 % IC : 0.53-0.70], (p<0.001) ; canagliflozine : HR : 0.60 [95 % IC : 0.47- 0.77] (non testé statistiquement pour raisons méthodologiques) et dapagliflozine : HR : 0.76 [0.67-0.87] [HR :0.53 [95 % IC : 0.43-0.66]. La réduction de ce risque se retrouvait tant chez les patients en prévention cardiovasculaire primaire que secondaire, et quel que soit le degré d’atteinte rénale à l’inclusion (33). Comme illustré dans le tableau 3, EMPA-REG a aussi mis en évidence une diminution significative des différents composants du critère rénal pluriel, ainsi qu’une réduction de 38 % du risque de progression vers une macroalbuminurie (HR : 0.62 [95 % IC 0.54-0.72], p<0.001), ce qui fut aussi retrouvé sous canagliflozine vs. placebo dans CANVAS (HR : 0.73 [95 % IC : 0.67-0.79]) et dapagliflozine (HR : 0.73 [95 % IC : 0.67-0.79] (Tableau 4) (28,32, 34,35).


L’étude CREDENCE (pour Canagliflozin and Renal Events in Diabetes with Established Nephropathy Clinical Evaluation) a inclus 4 401 diabétiques de type 2, âgés de 63 ans, avec une atteinte rénale modérée à sévère préexistante (35). Soixante pourcent des patients avaient une eGFR inférieure à 60 ml/min. Une albuminurie > 300 mg/g était présente chez 88 % des sujets. Tous bénéficiaient déjà à l’inclusion d’un traitement par ACE-i ou sartans à dose maximale. L’objectif principal de l’étude était de déterminer le risque d’IRT (dialyse, transplantation, eGFR <15 ml/min/1.73m2), de doublement de la créatinine ou de décès d’origine rénale ou cardiovasculaire sous 100 mg de canagliflozine (Invokana®) ou placebo au cours d’un suivi de 2.6 ans. Plusieurs objectifs secondaires ont aussi été analysés (dans un ordre statistiquement hiérarchisé). Les principaux résultats de CREDENCE montrent une réduction de 30 % de l’objectif primaire, quel que soit le degré de fonction rénale ou d’albuminurie à l’inclusion et de 34 % d’un objectif secondaire « ciblé » intégrant spécifiquement l’IRT, le doublement de la créatinine et le décès rénal. Ces résultats sont observés tant chez les patients en prévention cardiovasculaire primaire que secondaire (p=0.91 pour interaction) (congrès ADA 2019, San Francisco). Une réduction d’IRT per se et d’autres objectifs exploratoires, comme le risque de dialyse, transplantation et décès rénal, consolident ces résultats exemplaires, renforcés encore par une réduction de 31 % de l’albuminurie (95 % IC : 26-35) et par un moindre déclin annuel de la fonction rénale sous canagliflozine (Δ canagliflozine/placebo : 1.52 ml/min/1.73m2/an [-1.11 à 1.93]). L’étude n’a pas mis en évidence d’augmentation d’effets secondaires, y compris rénaux vs. placebo (36,37). Sur base de cette étude, la US Food and Drug Administration (FDA) a validé le 1e octobre 2019 la place de la canagliflozine comme traitement ralentissant l’évolution de la maladie rénale et diminuant le risque d’hospitalisation pour décompensation cardiaque chez les diabétiques de type 2 avec néphropathie. Très récemment, en phase avec ces données, chez des patients diabétiques de type 2 avec néphropathie modérée à sévère, Pollock et al. ont également observé sous dapagliflozine une réduction de 21 % (95 % CI - 34 à -5.2) de l’excrétion urinaire d’albumine après 24 semaines de traitement (38).
Plusieurs mécanismes ont été évoqués pour rendre compte de l’effet de néphroprotection de la classe des gliflozines (39). Parmi eux, les auteurs privilégient le rétablissement sous glucorétiques de la boucle de rétrocontrôle tubuloglomérulaire par l’apport dans le tubule distal de glucose et de sodium. Ceci amène une vasoconstriction réflexe de l’artériole afférente du glomérule avec, en conséquence, une diminution de la perfusion glomérulaire et une réduction de la pression intraglomérulaire. D’autres mécanismes font appel à une réduction de l’inflammation locale et à une meilleure oxygénation intrarénale via, entre autres, une diminution du taux d’angiotensine II et d’hormone natriurétique cardiaque. L’absence de différence marquée entre bras interventionnel et contrôle (eu égard au design des études) en termes d’Hba1c, de poids et de pression artérielle plaide contre une contribution physiopathologique proactive de ces différents paramètres dans les résultats observés (39).
Discussion et conclusions
La néphropathie diabétique est une complication chronique aux conséquences cliniques et humaines considérables. L’optimisation glycémique en est le premier pilier thérapeutique. Cette approche est surtout efficace aux stades des micro - et macroalbuminurie. Son efficacité est moindre sur les critères de fonction rénale tels que le doublement de la créatinine, l’IRT ou le décès rénal, comme rapporté dans la méta-analyse de Coca et al. (40). Le second pilier de traitement est le contrôle tensionnel. Dans ce contexte, les ACE-i et les sartans restent un premier choix comme traitements antihypertenseurs et antiprotéinuriques. Une troisième voie thérapeutique fondée sur les résultats des études interventionnelles met en évidence un effet collatéral de protection rénale de plusieurs médicaments hypoglycémiants. C’est le cas pour les DPP-4 i, et surtout pour les agonistes du GLP-1 avec leur effet de réduction de l’albuminurie. C’est encore le cas pour les gliflozines avec une néphroprotection qui concerne à la fois la fonction rénale et l’excrétion urinaire d’albumine. Ces dividendes semblent physiopathologiquement liés au médicament per se, (et à sa classe) (41), indépendamment de ses effets sur les autres facteurs de risque (glycémie, tension artérielle et/ou poids). C’est ce qui ressort de l’ensemble des essais où les différences de ces paramètres (HbA1c, tension artérielle, poids) entre bras interventionnel et contrôle au cours du suivi étaient ténues, eu égard d’ailleurs aux exigences méthodologiques des protocoles. Ces résultats renforcent l’intérêt en 2020 de ces médicaments pour lesquels une sécurité ou un bénéfice cardiovasculaire avaient déjà été mis en relief (42,43). Il n’est donc guère étonnant au vu de ce double bénéfice rénal et cardiovasculaire que les sociétés savantes de diabétologie recommandent, en cas d’insuffisance rénale chez le diabétique de type 2, après échec de la metformine, d’abord les SGLT-2 inhibiteurs ou, s’il y a contre-indication et/ou une eGFR inadéquate, les agonistes du GLP-1. En termes cardiovasculaires, en prévention secondaire, en présence d’une macroangiopathie cardiaque, elles privilégient les agonistes du GLP-1 et/ou les SGLT-2i et, s’il y a insuffisance cardiaque, logiquement, les SGLT-2 i, avant les agonistes du GLP-1, après échec des biguanides. Cette démarche thérapeutique doit cependant intégrer, pour les cliniciens, les effets secondaires éventuels de ses médicaments – et leur coût sociétal. Leur prescription rentre dès lors dans le cadre d’un traitement personnalisé et d’une approche holistique du patient diabétique. Quoi qu’il en soit, cette avancée thérapeutique contribue à l’optimisation de la prise en charge, sur le terrain, du patient diabétique de type 2.
Affiliations
1. Cliniques universitaires UCL Saint-Luc, Service d’Endocrinologie et Nutrition, Avenue Hippocrate 10, B-1200 Bruxelles, Belgique
2. CHR de Huy, Service de Néphrologie, Rue des Trois-Ponts, 2, B-4500 Huy
3. CHR de Mons, Service d'Endocrino-diabétologie, Av. B. Constantinople 5, B-7000 Mons
4. Oporto Medical School, University of Oporto, Portugal
5. NYU School of Medicine, NYU Diabetes Prevention Program, USA
Correspondance
Pr. (ém.) Martin Buysschaert
Cliniques universitaires Saint-Luc
Service d’Endocrinologie et Nutrition
Avenue Hippocrate 10
B-1200 Bruxelles, Belgique
E-mail: martin.buysschaert@uclouvain.be
Références
- Gregg EW, Li Y, Wang J, Burrows NR, et al. Changes in diabetes-related complications in the United States, 1990-2010. N Engl J Med. 2014 Apr 17;370(16):1514-23.
- Saran R, Robinson B, Abbott KC, et al. US Renal Data System 2018 Annual Data Report: Epidemiology of Kidney Disease in the United States. Am J Kidney Dis. 2019 Mar;73(3S1):S1-S28.
- Afkarian M, Sachs MC, Kestenbaum B, et al. Kidney disease and increased mortality risk in type 2 diabetes. J Am Soc Nephrol. 2013 Feb;24(2):302-8.
- Tancredi M, Rosengren A, Svensson AM, et al. Excess Mortality among Persons with Type 2 Diabetes. N Engl J Med. 2015 Oct 29;373(18):1720-32.
- Buysschaert M. Diabétologie Clinique, 4e Edition, De Boeck, Louvain-la-Neuve, Paris, 2011.
- Neven E, Vervaet B, Brand K, et al. Metformin prevents the development of severe chronic kidney disease and its associated mineral and bone disorder. Kidney Int. 2018 Jul;94(1):102-113. doi: 10.1016/j.kint.2018.01.027.
- De Broe ME, Kajbaf F, Lalau JD. Renoprotective Effects of Metformin. Nephron. 2018;138(4):261-274. doi: 10.1159/000481951.
- Buysschaert M, Djrolo F, Amoussou Guenou et al. La metformine revisitée et consolidée en 2016 : un point de vue consensuel de l’Afrique à l’Europe. Médecine des maladies métaboliques. 2016 ; doi : 10.1016/S1957-2557(16)30034-7.
- Davies MJ, D’Alessio DA, Fradkin J, et al. Management of Hyperglycemia in Type 2 Diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2018 Oct 4. pii: dci180033. doi: 10.2337/dci18-0033.
- Scirica BM, Bhatt DL, Braunwald E, et al.; SAVOR-TIMI 53 Steering Committee and Investigators. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med. 2013 Oct 3;369(14):1317-26. doi: 10.1056/NEJMoa1307684.
- White WB, Cannon CP, Heller SR, et al.; EXAMINE Investigators. Alogliptin after acute coronary syndrome in patients with type 2 diabetes. N Engl J Med. 2013 Oct 3;369(14):1327-35. doi: 10.1056/NEJMoa1305889.
- Green JB, Bethel MA, Armstrong PW, et al.; TECOS Study Group. Effect of Sitagliptin on Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2015 Jul 16;373(3):232-42. doi: 10.1056/NEJMoa1501352.
- Rosenstock J, Perkovic V, Johansen OE, et al.; CARMELINA Investigators. Effect of Linagliptin vs Placebo on Major Cardiovascular Events in Adults With Type 2 Diabetes and High Cardiovascular and Renal Risk: The CARMELINA Randomized Clinical Trial. JAMA. 2019 Jan 1;321(1):69-79.
- Mosenzon O, Leibowitz G, Bhatt DL, et al. Effect of Saxagliptin on Renal Outcomes in the SAVOR-TIMI 53 Trial. Diabetes Care. 2017 Jan;40(1):69-76.
- Cornel JH, Bakris GL, Stevens SR, et al.; TECOS Study Group. Effect of Sitagliptin on Kidney Function and Respective Cardiovascular Outcomes in Type 2 Diabetes: Outcomes From TECOS. Diabetes Care. 2016 Dec;39(12):2304-2310.
- Hemmer A, Maiter D, Buysschaert M, et al. Long-term effects of GLP-1 receptor agonists in type 2 diabetic patients: A retrospective real-life study in 131 patients. Diabetes Metab Syndr. 2019 Jan - Feb;13(1):332-336. doi: 10.1016/j.dsx.2018.09.007.
- Marso SP, Daniels GH, Brown-Frandsen K, et al. LEADER Steering Committee; LEADER Trial Investigators. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2016 Jul 28;375(4):311-22. doi: 10.1056/NEJMoa1603827.
- Marso SP, Bain SC, Consoli A, et al.; SUSTAIN-6 Investigators. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016 Nov 10;375(19):1834-1844.
- Hernandez AF, Green JB, Janmohamed S, et al. Harmony Outcomes committees and investigators. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised placebo-controlled trial. Lancet. 2018 Oct 27;392(10157):1519-1529. doi: 10.1016/S0140-6736(18)32261-X.
- Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet. 2019; Published online June 10, 2019 http://dx.doi.org/10.1016/S0140-6736(19)31149-3
- Holman RR, Bethel MA, Mentz RJ, et al. EXSCEL Study Group. Effects of Once-Weekly Exenatide on Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2017 Sep 28;377(13):1228-1239. doi: 10.1056/NEJMoa1612917.
- Mann JFE, Ørsted DD, Brown-Frandsen K, et al.; LEADER Steering Committee and Investigators. Liraglutide and Renal Outcomes in Type 2 Diabetes. N Engl J Med. 2017 Aug 31;377(9):839-848.
- Tuttle KR, Lakshmanan MC, Rayner B, et al. Dulaglutide versus insulin glargine in patients with type 2 diabetes and moderate-to-severe chronic kidney disease (AWARD-7): a multicentre, open-label, randomised trial. Lancet Diabetes Endocrinol 2018 Aug;6(8):605-617. doi: 10.1016/S2213-8587(18)30104-9.
- Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutide and renal outcomes in type 2 diabetes: an exploratory analysis of the REWIND randomised, placebo-controlled trial. Lancet. 2019 Jun 7. pii: S0140-6736(19)31150-X. doi:
- Pfeffer MA, Claggett B, Diaz R, et al.; ELIXA Investigators. Lixisenatide in Patients with Type 2 Diabetes and Acute Coronary Syndrome. N Engl J Med. 2015 Dec 3;373(23):2247-57. doi: 10.1056/NEJMoa1509225.
- Neumiller JJ, Alicic RZ, Tuttle KR. Therapeutic Considerations for Antihyperglycemic Agents in Diabetic Kidney Disease. J Am Soc Nephrol. 2017 Aug;28(8):2263-2274. doi: 10.1681/ASN.2016121372.
- Zinman B, Wanner C, Lachin JM, et al. ; EMPA-REG OUTCOME Investigators. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med. 2015 Nov 26;373(22):2117-28.
- Neal B, Perkovic V, Mahaffey KW, et al. ; CANVAS Program Collaborative Group. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med. 2017 Aug 17;377(7):644-657.
- Buysschaert M. Dapagliflozin and cardiovascular events in type 2 diabetes : the model of the DECLARE-TIMI 58 TRIAL. Louvain Med. 2019; 138 (1): 3-7.
- Wiviott SD, Raz I, Bonaca MP, et al.; for DECLARE–TIMI 58 Investigators. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2018 Nov 10. doi: 10.1056/NEJMoa1812389.
- McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019 Sep 19. doi: 10.1056/NEJMoa1911303.
- Wanner C, Inzucchi SE, Lachin JM, et al. ; for EMPA-REG OUTCOME Investigators. Empagliflozin and Progression of Kidney Disease in Type 2 Diabetes. N Engl J Med. 2016;375: 323-334.
- Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet. 2018 Nov 9. pii: S0140-6736(18)32590-X. doi: 10.1016/S0140-6736(18)32590-X
- Mosenzon O, Wiviott SD, Cahn A, et al. Effects of dapagliflozin on development and progression of kidney disease in patients with type 2 diabetes: an analysis from the DECLARE-TIMI 58 randomised trial. Lancet Diabetes Endocrinol. 2019 Aug;7(8):606-617. doi: 10.1016/S2213-8587(19)30180-9.
- Raz I, Wiviott SD, Yanuv I, et al. Effects of dapagliflozin on the urinary-to-creatinine ratio in type 2 D: a predefined analysis from the DECLARE-TIMI 58 randomized placebo control trial. Abstract, American Diabetes Association, June 7/011.2019, San Francisco
- Perkovic V, Jardine MJ, Neal B, et al.; CREDENCE Trial Investigators. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy. N Engl J Med. 2019 Apr 14. doi: 10.1056/NEJMoa1811744.
- Buysschaert M. La canagliflozine (invokana®) est associée à une néphro – cardioprotection exemplaire dans le diabète de type 2. Synopsis de l’étude CREDENCE. Louvain Med. 2019; 139 (5): 255-260.
- Pollock C, Stefánsson B, Reyner D, et al. Albuminuria-lowering effect of dapagliflozin alone and in combination with saxagliptin and effect of dapagliflozin and saxagliptin on glycaemic control in patients with type 2 diabetes and chronic kidney disease (DELIGHT): a randomised, double-blind, placebo-controlled trial. Lancet Diabetes Endocrinol. 2019 Jun;7(6):429-441. doi: 10.1016/S2213-8587(19)30086-5.
- Heerspink HJ, Perkins BA, Fitchett DH, et al. Sodium Glucose Cotransporter 2 Inhibitors in the Treatment of Diabetes Mellitus: Cardiovascular and Kidney Effects, Potential Mechanisms, and Clinical Applications. Circulation. 2016 Sep 6;134(10):752-72.
- Coca SG, Ismail-Beigi F, Haq N, et al. Role of intensive glucose control in development of renal end points in type 2 diabetes mellitus: systematic review and meta-analysis intensive glucose control in type 2 diabetes. Arch Intern Med. 2012 May 28;172(10):761-9. doi: 10.1001/archinternmed.
- Clegg LE, Heerspink HJL, Penland RC, et al. Reduction of Cardiovascular Risk and Improved Estimated Glomerular Filtration Rate by SGLT2 Inhibitors, Including Dapagliflozin, Is Consistent Across the Class: An Analysis of the Placebo Arm of EXSCEL. Diabetes Care. 2019 Feb;42(2):318-326. doi: 10.2337/dc18-1871.
- Buysschaert M. Les SGLT-2 inhibiteurs sont-ils une approche thérapeutique holistique du diabète de type 2 ? Le point après l’essai EMPA-REG OUTCOME. Louvain Med. 2017 ; 136 : 293-299.
- Buysschaert M, Preumont V Buysschaert B. Médicaments hypoglycémiants dans le diabète de type 2 et néphroprotection : un nouvel axe thérapeutique ? Med Mal Metab 2019 ; accepté