Introduction
Les occlusions vasculaires rétiniennes comprennent l’occlusion veineuse rétinienne (OVR) et l’occlusion artérielle rétinienne (OAR). La neuropathie optique ischémique antérieure non artéritique (NOIA) est secondaire à une souffrance microvasculaire de la tête du nerf optique, cette portion étant vascularisée par un réseau issu de l’artère centrale de la rétine, des artères piales et des artères ciliaires courtes postérieures. Leur prévalence est indiquée dans la tableau 1.
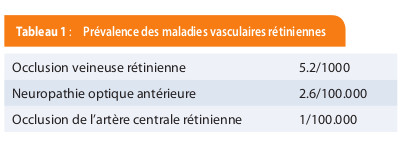
L’OVR, deuxième affection vasculaire rétinienne la plus fréquente après la rétinopathie diabétique, est une cause majeure de perte de l’acuité visuelle. Selon Hayreh, on peut distinguer l’occlusion de la veine centrale rétinienne (OVCR), l’occlusion de la branche d’une veine rétinienne (OBVR), et l’occlusion veineuse hémi-rétinienne (OVHR) (1). L’occlusion de la branche est quatre fois plus fréquente que l’occlusion centrale. La prévalence augmente avec l’âge.
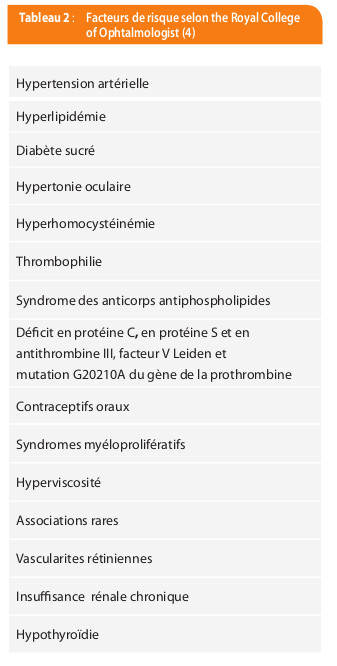
La pathogénèse n’est pas entièrement élucidée. En règle générale, elle représente le résultat d’événements multifactoriels, dont les principaux mécanismes incluent une lésion endothéliale, un ralentissement circulatoire et un état d’hypercoagulabilité. L’occlusion de branche semble être liée à la compression de la branche veineuse par une artériole rétinienne sclérotique et rigide aux points de croisement artério-veineux, l’artère et la veine partageant la même adventice à leur croisement. L’occlusion centrale est habituellement associée à la formation d’un thrombus fibrineux-plaquettaire dans la veine (2). Les principaux facteurs de risque associés au développement d’une OVR sont des facteurs locaux, notamment l’hypertonie oculaire, et systémiques, tels que les facteurs de risque cardiovasculaire (3).
Discussion
Dans la pathogénèse de l’OVR peuvent être affectées les plaquettes, la coagulation, la fibrinolyse et la viscosité.
Fonction plaquettaire
Elle a une place importante dans l’athérosclérose. Elle est difficile à étudier et l’a très peu été dans les OVRs, avec des résultats discordants. Une augmentation de la réponse plaquettaire à la thrombine (5), au collagène (6) et plus récemment à l’adénosine diphosphate (7) ont été signalées.
Coagulation
Dans la méta-analyse de Janssen (2005), les odds ratio (OR) étaient 1.5 pour le facteur V Leiden (FVL), 1.6 pour la mutation G20210A du gène de la prothrombine, 3.9 pour le syndrome des anticorps antiphospholipides (APL) et 8.9 pour l’hyperhomocystéinémie (8). Dans celle de Rehak (2008) l’OR pour le FVL était 1.66 (9). Plus récemment, dans 132 cas d’OVRs, Glueck a trouvé une association avec APL, déficit en protéine S, augmentation du Facteur VIII et hyperhomocystéinémie (10). Schockman a découvert au moins 1 facteur de thrombophilie sur 7 dans 50% d’OVRs. L’hyperhomocystéinémie et le facteur VIII étaient les deux plus importants facteurs de risque. Les patients avec FVL et G20210A n’avaient pas d’antécédents de maladie thromboembolique veineuse mais étaient sujets à une maladie vasculaire ischémique (11). Parmi les patients les plus jeunes (< 60 ans), sans facteur de risque cardiovasculaire, Arsene a trouvé 22 cas de thrombophilie sur 234 cas d’OVRs (9.4%). Le FVL, l’APL, le déficit en antithrombine III/protéine C/protéine S constituaient les anomalies les plus fréquentes (12). Les déficits thrombophiliques multiples semblent être plus fréquents chez les patients âgés de moins de 65 ans. L’augmentation du facteur VIII, le taux plasmatique élevé de lipoprotéine (a) (LpA) et la résistance à la protéine C activée sont les marqueurs de risque les plus courants (13). Une grande étude rétrospective récente menée en Suède sur un échantillon de 6.007.042 personnes a souligné que la maladie thromboembolique veineuse ne partage pas la familiarité avec l’OVR et le glaucome (14). Une fréquence particulière d’OVR a été signalée chez des jeunes femmes coréennes enceintes, la pré-éclampsie/éclampsie représentant un facteur de risque (15). L’hyperhomocystéinémie et le facteur VIII élevé sont d’importants facteurs de risque d’OVRs et de complications de la grossesse (16) (17). Le fait que l’OVR puisse constituer un facteur de risque d’accident vasculaire cérébral est un sujet très controversé. Il semble que les plaques carotidiennes athéroscléreuses y soient plus fréquemment associées, tandis que l’incidence des accidents vasculaires cérebraux est la même avant et après le diagnostic d’une OVR. Elle est associée à une augmentation de la mortalité cardiovasculaire chez les patients en dessous de 70 ans (HR 2.5) (18). Enfin, le score de Framingham à 10 ans est de 10.1% (19) (6% dans la population générale).
Fibrinolyse
Une altération de la fibrinolyse peut être responsable d’un état de thrombophilie (20). L’inhibiteur type 1 du plasminogène activé (PAI 1) augmente dans le diabète et l’obésité. Il a aussi été retrouvé augmenté dans 15% des cas d’OVRs (21). La lipoprotéine A (LpA) est une lipoprotéine de basse densité qui a un rôle athérogène et thrombotique, également lié à son effet anti-fibrinolytique. Vu qu’elle est structurellement similaire au plasminogène, elle entre en concurrence au niveau de la fibrine et sa dégradation en est alors bloquée. Ce qui expliquerait pourquoi l’hypercholestérolémie est un facteur de risque d’OVR. Les résultats des études récentes sont contradictoires, mais un niveau de LpA > 300 mg/L semble être un facteur de risque indépendant pour une maladie thromboembolique veineuse (22).
Viscosité du sang
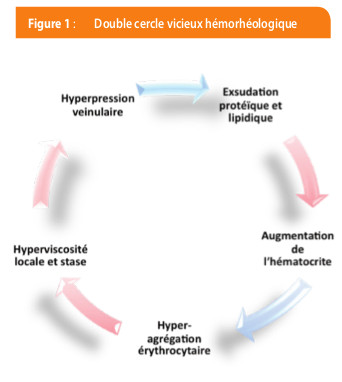
Un syndrome d’hyperviscosité peut être influencé par différents facteurs, tels que l’augmentation des éléments figurés du sang (polyglobulie, leucocytose, thrombocytose), le taux élevé des protéines plasmatiques (macroglobulinémie de Waldenstrom, myélome multiple), l’hyperviscosité plasmatique (paraprotéinémies et crioglobulinémies), l’altération de l’élasticité de la membrane et de l’agrégation des globules rouges. La rétinopathie du syndrome d’hyperviscosité est caractérisée par la dilatation et la tortuosité de l’ensemble des veines rétiniennes (aspect “saucisse-like”) et une présentation la plus souvent bilatérale. Une OVCR peut compliquer ce tableau et peut s’améliorer suite à un traitement de plasmaphérèse (23). L’augmentation de la viscosité dans la microcirculation rétinienne et la stase conséquente déclenchent ce que Stoltz a défini un « double cercle vicieux hémorhéologique » (24) (Figure 1).
Wautiers et al. ont trouvé que l’adhésion aux cellules endothéliales était significativement augmentée chez 20 patients atteints d’OVCR par rapport aux sujets normaux. Elle peut être induite par une surexpression de la phosphatidylsérine à la surface des globules rouges qui se lie aux cellules endothéliales exprimant des récepteurs pour une telle molécule d’adhésion (25). En dehors d’un syndrome d’hyperviscosité, l’ischémie rétinienne, qui est secondaire à l’occlusion veineuse rétinienne et au ralentissement du flux sanguin rétinien, conduit à la synthèse accrue du facteur de croissance endothélial vasculaire (VEGF) intraoculaire par les cellules gliales périvasculaires (26). Ce dernier induit une leucostase qui entretient un cercle vicieux ischémique local. Le VEGF est une cytokine primaire qui inhibe la synthèse des protéines structurales des jonctions serrées de l’endothelium, ce qui entraîne une augmentation de la perméabilité trans-endothéliale en contribuant au développement de l’œdème maculaire, une cause fréquente de déficience visuelle (27). L’utilisation d’agents anti-facteur de croissance endothélial vasculaire (anti-VEGF), ranibizumab et aflibercept, a révolutionné le traitement des conditions vasogéniques rétiniennes et notamment de l’œdème maculaire après occlusion de la veine rétinienne (28). La pharmacothérapie intravitréale avec agents anti-VEGF est efficace et de bon profil de sécurité (29). Le pronostic de l’acuité visuelle et le déclin de l’œdème maculaire dépendent d’une mise sous traitement rapide et de son maintien constant, à la fois dans l’ OVCR et dans l’OBVR (30) (31).
Conclusions
Le dépistage systématique de la thrombophilie chez les patients présentant une occlusion veineuse rétinienne n’est pas recommandé (32). Une thrombophilie est à suspecter en présence d'au moins une de ces conditions (33) :
- patient jeune ;
- absence de facteurs de risque cardiovasculaire ;
- histoire personnelle de maladie thromboembolique veineuse ;
- occlusion bilatérale ;
- grossesse.
La recherche d’une thrombophilie devra alors comprendre la détermination de l’ATIII, des protéine C et S, des APL, de l’homocystéine, de la résistance à la protéine C activée, de la mutation G20210A, du FVIII et de la LpA.
Un traitement anti-thrombotique de routine n’est pas indiqué, mais peut être envisagé chez certains patients présentant un début de symptômes et aucun facteur de risque local ou présentant des facteurs de risque prothrombotique majeur tels que le syndrome des anticorps antiphospholipides. L’aspirine et le clopidogrel ont montré une tendance favorable à la récupération de l’acuité visuelle (34). L’héparine de bas poids moléculaire initiée à l’apparition des symptômes et poursuivie pendant 1-3 mois a montré un effet favorable sur la récupération de l’acuité visuelle et une réduction du 78% du risque relatif des effets indésirables oculaires, sans entraîner une augmentation d’hémorragie vitréenne (35). Un traitement fibrinolytique à faible dose doit être réservée à des cas très sélectionnés, par exemple chez les sujets avec une perte totale de la vision. Le rôle des anticoagulants directs reste indéterminé. Un traitement prophylactique avec de l’aspirine à long terme est justifié par le risque de récidive dans le même œil (2,5% après 4 ans) et dans l’œil controlatéral (11,9% après 4 ans) et par le risque accru de mortalité cardiovasculaire (36).
Recommandations pratiques
- Une étude systématique de la thrombophilie dans l’OVR est à faire chez les sujets jeunes, en absence de facteurs de risque cardiovasculaire, en cas d’histoire personnelle de maladie thromboembolique veineuse, dans les occlusions bilatérales et en grossesse.
- Les anomalies les plus fréquentes sont le syndrome des anticorps antiphospholipides et l’hyperhomocystéinémie.
- Aucune mutation de JAK2 a été signalée.
- Des altérations plaquettaires, de la fibrinolyse et de la viscosité sont possibles.
- Un traitement anticoagulant peut être proposé en phase aiguë, en cas d’occlusion centrale de la veine rétinienne.
- Un traitement antiagrégant prophylactique à long terme est justifié.
- L’usage des anti-VEGF par voie intravitréenne a une place de plus en plus importante dans la prise en charge de cette pathologie, permettant d’interrompre un cercle vicieux de stase veineuse et d’ischémie rétinienne.
L'auteur déclare aucun conflit d'intérêts
Correspondance
Dr. Gianfilippo Nifosì
CHU Brugmann
Hémato-Oncologie
Place Van Gehuchten 4
B-1020 Bruxelles
Références
- Hayreh SS. Retinal vein occlusion. Indian J Ophtalmol 1994 Sep;42(3):109-32.
- Glacet-Bernard A, Coscas G, Pournaras CJ. Occlusions veineuses rétiniennes. Bulletin des Sociétés d’Ophtalmologie de France. Rapport annuel 11/2011.
- Kolar P. Risk factors for central and branch retinal vein occlusion: a meta-analysis of published clinical data. J Ophthalmol 2014;2014:724780.
- The Royal College of Ophtalmologist. Retinal vein occlusion (RVO) guidelines. July 2015
- Leoncini G, Signorello MG, Segantin A et al. In retinal vein occlusion platelet response to thrombin is increased. Thromb Res 2009 Dec;124(6):e48-55.
- Leoncini G, Bruzzese D, Signorello MG et al. Platelet activation by collagen is increased in retinal vein occlusion. Thromb Haemost 2007 Feb;97(2):218-27.
- Kuhli-Hattenbach C, Hellstern P, Kohnen T et al. Platelet activation by ADP is increased in selected patients with anterior ischemic optic neuropathy or retinal vein occlusion. Platelets 2017 Feb;16:1-4.
- Janssen MC, den Heijer M, Cruysberg JR et al. Retinal vein occlusion: a form of venous thrombosis or a complication of atherosclerosis? A meta-analysis of thrombophilic factors. Thromb Haemost 2005 Jun;93(6):1021-6.
- Rehak M, Rehak J, Müller M et al. The prevalence of activated protein C (APC) resistance and factor V Leiden is significantly higher in patients with retinal vein occlusion without general risk factors. Case-control study and meta-analysis. Thromb Haemost 2008 May;99(5):925-9.
- Glueck CJ, Hutchins RK, Jurantee J et al. Thrombophilia and retinal vascular occlusion. Clin Ophthalmol 2012;6:1377-84.
- Schockman S, Glueck CJ, Hutchins RK. Diagnostic ramifications of ocular vascular occlusion as a first thrombotic event associated with factor V Leiden and prothrombin gene heterozygosity. Clin Ophthalmol 2015 Apr 3;9:591-600.
- Arsène S, Delahousse B, Regina S et al Increased prevalence of factor V Leiden in patients with retinal vein occlusion and under 60 years of age. Thromb Haemost 2005 Jul;94(1):101-6.
- Kuhli-Hattenbach C, Hellstern P, Miesbach W et al. Multiple thrombophilic risk markers in patients < 65 years of age with retinal vein occlusion. Ophtalmologie 2017 Feb 9.
- Zöller B, Li X, Sundquist J et al. Venous thromboembolism does not share familial susceptibility with retinal vascular occlusion or glaucoma: a nationwide family study. J Thromb Thrombolysis 2016 Nov;42(4):505-12.
- Park SJ, Choi NK, Seo KH et al. Retinal vein occlusion and pregnancy, pre-eclampsia, and eclampsia: the results from a nationwide, population-based study using the national claim database. PLoS One 2015 Mar 16;10(3):e0120067.
- Dixon SG, Bruce CT, Glueck CJ. Retinal vascular occlusion: a window to diagnosis of familial and acquired thrombophilia and hypofibrinolysis, with important ramifications for pregnancy outcomes. Clin Ophthalmol 2016 Aug 9;10:1479-86.
- Kurtz WS, Glueck CJ, Hutchins RK et al. Retinal artery and vein thrombotic occlusion during pregnancy: markers for familial thrombophilia and adverse pregnancy outcomes. Clin Ophthalmol 2016 May 23;10:935-8.
- Cugati S, Wang JJ, Knudtosn MD et al. Retinal vein occlusion and vascular mortality. Ophtalmology 2007;114:520-4.
- Khan Z, Almeida DR, Rahim K et al. 10-year Framingham risk in patients with retinal vein occlusion: a systematic review and meta-analysis. Can J Ophthalmol 2013;48:40-45.
- Glueck CJ, Wang P, Bell H et al. Associations of thrombophilia, hypofibrinolysis, and retinal vein occlusion. Clin Appl Thromb Hemost 2005 Oct;11(4):375-89.
- Gori AM, Marcucci R, Fatini C et al. Impaired fibrinolysis in retinal vein occlusion: a role for genetic determinants of PAI-1 levels. Thromb Haemost 2004 Jul;92(1):54-60.
- Kuhli-Hattenbach C, Hellstern P, Miesbach W et al. Elevated lipoprotein (a) levels are an independent risk factor for retinal vein occlusion. Acta Ophthalmol 2017 Mar;95(2):140-145.
- Rajagopal R, Apte RS. Seeing through thick and through thin: Retinal manifestations of thrombophilic and hyperviscosity syndromes. Surv Ophthalmol 2016 Mar-Apr;61(2):236-47.
- Stoltz J. Les grands déterminants de la viscosité sanguine: étiologie des syndromes d’hyperviscosité. Conv Méd 1982;1:225-31.
- Wautiers MP, Héron E, Picot J et al. Red blood cell phosphatidylserine exposure is responsible for increased erythrocyte adhesion to endothelium in central retinal vein occlusion. J Thromb Haemost 2011 9:1049–1055.
- Aiello LP, Avery RL, Arrigg PG et al. Vascular endothelial growth factor in ocular fluid of patients with diabetic retinopathy and other retinal disorders. N Engl J Med 1994 Dec 1;331(22):1480-7.
- Fujikawa M, Sawada O, Miyake T et al. Correlation between vascular endothelial growth factor and nonperfused areas in macular edema secondary to branch retinal vein occlusion. Clin Ophthalmol 2013;7:1497-501.
- Tah V, Orlans HO, Hyer J et al. Anti-VEGF Therapy and the Retina: An Update. J Ophthalmol 2015;2015:627674.
- Ho M, Liu DT, Lam DS, et al. Retinal vein occlusion, from basic to the latest treatment. Retina 2016 Mar;36(3):432-48.
- Gerding H. Intravitreal anti-VEGF Treatment in Central Retinal Vein Occlusion (CRVO): a Meta-Analysis of One Year Results. Klin Monbl Augenheilkd 2017 Apr;234(4):546-550.
- Ehlers JP, Kim SJ, Yeh S et al. Therapies for Macular Edema Associated with Branch Retinal Vein Occlusion: A Report by the American Academy of Ophthalmology. Ophtalmology 2017 Sep;124(9):1412-1423.
- Kirkegaard K, Heegaard S, Hvas AM. No evidence for thrombophilia in patients with retinal venous occlusion: a systematic GRADE-based review. Acta Ophthalmol 2017 Feb;95(1):12-19.
- Kuhli-Hattenbach C, Miesbach W, Scharrer I et al. Thrombophilic and systemic risk factors in patients with retinal vein occlusion. Ophthalmologie 2011 Feb;108(2):104-10.
- Ageno W, Beyer-Westendorf J, Garcia DA et al. Guidance for the management of venous thrombosis in unusual sites. J Thromb Thrombolysis 2016;41:129-143.
- Lazo-Langner A, Hawel J, Ageno W et al. Low molecular weight heparin for the treatment of retinal vein occlusion: a systematic review and meta-analysis of randomized trial. Haematologica 2010; 95(9):1587-1593.
- Squizzato A, Manfredi E, Bozzato S et al. Antithrombotic and fibrinolytic drugs for retinal vein occlusion: a systematic review and a call for action. Thromb Haemost 2010 Feb;103(2):271-6.