Le traitement de la néphrite lupique : vraiment du neuf !
Farah Tamirou, Charlotte Baert, Pauline Montigny, Frédéric A. Houssiau
La néphrite lupique (NL) concerne 35 à 60% des patients souffrant de lupus érythémateux disséminé (LED) (1, 2). Cinq à 20% des patients souffrant de NL développeront une insuffisance rénale terminale (IRT). Les buts du traitement sont de contrer rapidement la réaction inflammatoire et auto-immune afin de limiter au maximum la perte des néphrons, de minimiser l’hyperfiltration sur les néphrons restants, d’éviter les rechutes par un traitement immunosuppresseur prolongé, de traiter les comorbidités et d’éviter au maximum les effets secondaires des médicaments, en particulier des glucocorticoïdes.
Les stratégies traditionnelles n’atteignent que partiellement leur objectif
Le traitement actuel de la NL repose sur un protocole séquentiel qui consiste à induire une réponse par un traitement immunosuppresseur initial et de la maintenir par un traitement d’entretien prolongé dans le but d’éviter de nouveaux épisodes. Selon les recommandations de plusieurs sociétés scientifiques (3, 4), on prescrit généralement de la méthylprednisolone par voie intraveineuse (IV) (3x500-750mg/j pendant trois jours) relayée par une corticothérapie orale (0,3-0,5mg/kg/j), rapidement réduite à 5-10 mg/jour dès le troisième mois. Du mycophénolate mofetil (MMF) ou de la cyclophosphamide prescrite par voie IV selon le schéma Euro-Lupus (6x500 mg à 15 jours d’intervalle) (5) sont recommandés comme traitement immunosuppresseur initial. Une néphroprotection optimale est essentielle (inhibition du système rénine-angiotensine), de même que la prise d’hydroxychloroquine, sauf en cas d’intolérance. Après la phase d’induction, de l’azathioprine (AZA) ou du MMF sont recommandés pour au moins trois ans.
S’il est exact que le pronostic de la NL s’est considérablement amélioré grâce à ces traitements, il n’empêche que les résultats restent en-deçà des espérances, en particulier au long cours. Le taux de réponse rénale complète (RRC), définie comme une protéinurie ≥0.5g/j, ne dépasse pas 20 à 30% après 6 à 12 mois de traitement (6) et 20 à 35% des patients en rémission récidivent dans un délai de 3 à 5 ans (7). Plus grave, au moins 20% des patients souffrent d’une réduction de la filtration glomérulaire (FG) (<60ml/min/1,73m2) et 5 à 20% requièrent une substitution rénale (dialyse ou transplantation) (8).
Un changement de paradigme
Deux études récentes de phase 3 ont permis de démontrer la supériorité d’un traitement combiné d’emblée, associant un traitement ciblé par belimumab (BEL ; Benlysta®) ou par voclosporine (VOC ; Lupkinys®) aux immunosuppresseurs classiques.
Le belimumab (BEL) est un anticorps monoclonal anti-BLyS/BAFF utilisé dans le lupus sans complication rénale depuis 10 ans. Une large étude de phase 3 (BLISS-LN) (9), incluant des patients souffrant de NL, a démontré que la combinaison de BEL (10mg/kg/mois en IV) et de MMF permettait d’obtenir significativement plus de RRC à 2 ans (30% dans le groupe BEL/MMF comparé à 20% dans le groupe PBO/MMF). Davantage de patients traités par BEL prenaient ≤7,5 mg de prednisolone/j après 2 ans. La réduction de la FG était moins importante dans le groupe BEL. Les patients traités par BEL souffraient moins vite d’un nouvel épisode de NL. La toxicité était comparable dans les deux groupes.
La VOC est un inhibiteur de calcineurine plus moderne que la ciclosporine, avec une meilleure stabilité métabolique et une élimination plus rapide des métabolites, supprimant ainsi la nécessité de monitorer les taux sanguins et réduisant la fréquence des effets secondaires. Dans une étude phase 3 (AURORA) (10), l’ajout de VOC au MMF a permis d’obtenir significativement plus de RRC à un an (41% dans le groupe VOC/MMF versus 23% dans le groupe MMF seul), sans signaux de toxicité inquiétants dans le groupe VOC/MMF.
D’autres molécules sont en cours d’investigation comme l’obinutuzumab (anticorps monoclonal anti-CD20) ou l’anifrolumab (anticorps monoclonal dirigé contre le récepteur des interférons de type I) (IFNAR).
Même s’il est très probable que la norme thérapeutique évoluera progressivement d’un traitement séquentiel vers des traitements combinés, de nombreuses questions sont mises à l’agenda :
- L’effet de la VOC est-il majoritairement anti-protéinurique, plutôt qu’immunosuppresseur ?
- Le gain en terme de RRC se traduira-il par une baisse du taux d’IRT au long cours ?
- Faut-il prescrire ces nouvelles molécules en première intention, comme le suggèrent les études ou les réserver aux patients qui ne répondent pas rapidement au traitement standard, afin d’éviter le risque de sur-traitement ?
- Peut-on utiliser ces molécules, en particulier la VOC, chez des patients avec une insuffisance rénale inaugurale ?
- Combien de temps faut-il les prescrire ?
- Peut-on identifier a priori les patients qui répondront mieux à l’une ou l’autre des nouvelles molécules ?
Au-delà des traitements immunosuppresseurs
Ces progrès, qui ont mené à l’enregistrement du BEL et de la VOC par les agences de médicaments (FDA et EMA pour BEL et FDA pour VOC), ne peuvent pas nous faire oublier les mesures importantes à prendre dans toute néphropathie chronique : arrêt du tabac, lutte contre l’excès pondéral, limitation des apports sodés, contrôle strict de la pression artérielle (cible : 120/80mm Hg), contrôle lipidique rigoureux, évaluation régulière du risque cardio-vasculaire, adhésion au traitement médicamenteux, pratique de l’exercice physique, etc. Dans ce même registre, il est probable que les gliflozines, des inhibiteurs du co-transporteur sodium/glucose 2 (SGLT2i), seront utilisées dans le traitement de la NL comme elles le sont déjà dans d’autres néphropathies glomérulaires compliquées d’IR et de protéinurie (en particulier la néphropathie diabétique). Les gliflozines bloquent la réabsorption proximale du sodium et du glucose (expliquant son effet hypoglycémiant). L’augmentation de la concentration en sodium dans le tubule distal et dans la macula densa induit une vasoconstriction de l’artériole glomérulaire afférente, réduit l’hyperfiltration et restaure le feeback tubuloglomérulaire. Dans l’étude DAPA-CKD, réalisée chez 4.309 patients souffrant de pathologie glomérulaire chronique avec une FG entre 25 et 75ml/min/1,73m2, l’administration de 10mg/j de dapagliflozine a réduit de 34% l’outcome rénal défavorable défini comme le risque de dégradation de la FG de plus de 50% de sa valeur initiale, d’IRT ou de décès de cause rénale ou cardiovasculaire (11).
Références
- Anders HJ, Saxena R, Zhao MH, et al. Lupus nephritis. Nat Rev Dis Primers. 2020;6:7.
- Pons-Estel GJ, Serrano R, Plasin MA, et al. Epidemiology and management of refractory lupus nephritis. Autoimmun Rev. 2011;10:655-63.
- Fanouriakis A, Kostopoulou M, Cheema K, et al. 2019 Update of the Joint European League Against Rheumatism and European Renal Association-European Dialysis and Transplant Association (EULAR/ERA-EDTA) recommendations for the management of lupus nephritis. Ann Rheum Dis. 2020;79:713-23.
- Rovin BH, Adler SG, Barratt J et al. Executive summary of the KDIGO 2021 Guideline for the Management of Glomerular Diseases. Kidney Int. 2021;100:753-79.
- Houssiau FA, Vasconcelos C, D’Cruz D et al. Immunosuppressive therapy in lupus nephritis: the Euro-Lupus Nephritis Trial, a randomized trial of low-dose versus high-dose intravenous cyclophosphamide. Arthritis Rheum. 2002;46: 2121-31.
- Wofsy D, Diamond B and Houssiau FA. Crossing the Atlantic - The Euro-Lupus Nephritis Regimen in North America. Arthritis Rheumatol. 2015; 67: 1144-6.
- El Hachmi M, Jadoul M, Lefèbvre C, Depresseux G, Houssiau FA. Relapses of lupus nephritis: incidence, risk factors, serology and impact on outcome. Lupus. 2003; 12: 692-6.
- Gasparotto M, Gatto M, Binda V, Doria A and Moroni G. Lupus nephritis: clinical presentations and outcomes in the 21st century. Rheumatology. 2020; 59; suppl. 5: v39-v51.
- Furie R, Rovin BH, Houssiau F, et al. Two-Year, Randomized, Controlled Trial of Belimumab in Lupus Nephritis. N Engl J Med. 2020;383:1117-28.
- Rovin BH, Teng YKO, Ginzler EM, et al. Efficacy and safety of voclosporin versus placebo for lupus nephritis (AURORA 1): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2021;397:2070-80.
- Heerspink HJL, Stefánsson BV, Correa-Rotter R et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020; 383:1436-46.
Nouveautés et actualisations de la prise en charge de la polyarthrite rhumatoïde en 2021
Emilie Sapart, Aleksandra Avramovska, Laurent Meric de Bellefon, Stéphanie de Montjoye, Stéphanie Dierckx, Adrien Nzeusseu, Valérie Pirson, Tatiana Sokolova, Maria Stoenoiu, Patrick Durez
Introduction
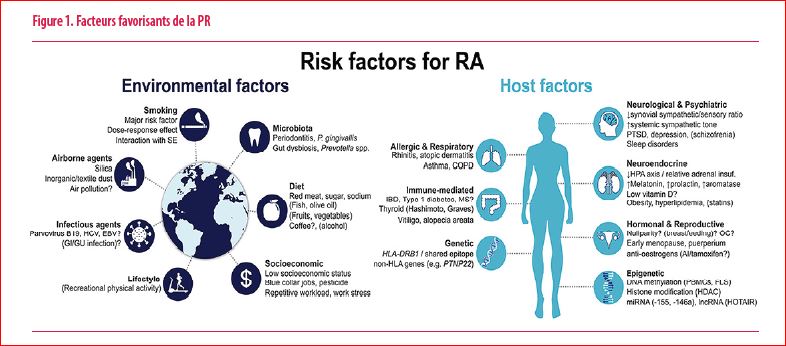
La PR est une des maladies inflammatoires chroniques les plus fréquentes (1). Elle touche 0,2 à 1% de la population (2) avec un sex-ratio de 3 femmes pour 1 homme. Elle peut survenir à tout âge mais préférentiellement après la grossesse ou la ménopause. Elle atteint en priorité les articulations mais peut être à l’origine d’une atteinte pulmonaire, oculaire, de nodules rhumatoïdes et d’un risque cardio-vasculaire augmenté (1,3,4). L’atteinte typique de la PR associe des douleurs et des gonflements articulaires bilatéraux et symétriques, d’apparition récente, avec une raideur matinale et des résurgences algiques nocturnes (1,3,4). Son étiologie reste inconnue et repose sur différents facteurs génétiques, environnementaux et immunitaires (figure 1). La prise en charge et les traitements sont assez similaires pour les autres formes d’arthrite inflammatoire périphérique telles que l’arthrite psoriasique ou les spondyloarthropathies.
Le diagnostic précoce
La reconnaissance de toute arthrite inflammatoire débutante est cruciale. L’anamnèse et l’examen clinique sont les piliers essentiels afin de distinguer les différentes formes d’arthrites inflammatoires des atteintes métaboliques liées aux dépôts dans les articulations ou des atteintes mécaniques liées à l’usure du cartilage.
L’évaluation clinique minutieuse est essentielle à la recherche des signes de synovite principalement localisée au niveau des mains et des pieds. Il est recommandé de faire un compte articulaire en notant les articulations douloureuses et gonflées. L’examen systémique est indispensable car l’arthrite peut s’accompagner de manifestations extra articulaires et il permet d’affiner le diagnostic différentiel.
Un syndrome inflammatoire biologique est présent dans 90% des cas d’arthrite. La PR est une maladie auto-immunitaire caractérisée souvent par la production de 2 auto-anticorps, le facteur rhumatoïde et les anticorps anti-peptides citrullinés (ACPA). Les ACPA ont une spécificité de 98% pour une sensibilité de 50-60% et leur détection est dès lors très utile dès le début des symptômes articulaires inflammatoires. Le facteur rhumatoïde n’est quant à lui pas très spécifique (sensibilité 70-80% et spécificité 65-85%).
Le bilan de base radiologique peut être enrichi par la réalisation d’une échographie articulaire qui permet de détecter de manière précoce les synovites, ténosynovites et érosions ou d’une IRM qui pourra mettre en évidence toutes ces lésions précoces et l’œdème osseux (zone de développement potentiel d’érosions) (1). Ces examens sont en effet plus sensibles pour détecter l’arthrite débutante mais leur interprétation devra être prudente car les synovites a minima peuvent être influencées par des facteurs mécaniques, métaboliques et l’âge.
A noter que, actuellement, l’intérêt des biopsies synoviales dans le diagnostic des PR reste du domaine de la recherche et de protocoles scientifiques mais pourrait devenir un élément capital et indispensable à l’avenir.
Le diagnostic repose sur tous ces éléments cliniques et paracliniques. Il est validé par des critères internationaux de classification de la polyarthrite. Les critères de l’American College of Rheumatology de 1987 ont été remplacés en 2010 par des critères américains et européens incluant la présence des ACPA et sont dès lors plus sensibles. Il est cependant essentiel avant d’utiliser ces critères d’exclure toute autre arthropathie (arthrose, chondrocalcinose, arthrite virale, autres rhumatismes inflammatoires…).
L’évaluation et les objectifs
Les rhumatologues ont développé ces dernières années des outils cliniques et paracliniques très utiles pour évaluer l’arthrite et la PR. Ils permettent de mesurer de manière plus précise l’activité de la maladie et la réponse thérapeutique. La première démarche, une fois le diagnostic de PR confirmé, sera de compter les articulations douloureuses et gonflées par un examen minutieux des différents sites articulaires. Il sera également demandé au malade de compléter un questionnaire évaluant sur une échelle analogique de 0 à 10 le degré d’activité de la maladie, de la douleur, de la fatigue et de répondre à des questions évaluant le degré de difficultés de réaliser des activités courantes (questionnaire HAQ).
L’intégration du nombre d’articulations douloureuses, gonflées, de l’activité de la maladie évaluée par le patient et du taux inflammatoire (CRP ou VS) permet de calculer un score composite d’activité de la maladie (score DAS, le plus utilisé étant le DAS28-CRP en se limitant aux articulations des membres supérieurs et des genoux). Ce score validé dans de nombreux essais cliniques (5) permet à la fois de définir le degré d’activité (importante, modérée, légère ou rémission) et permet d’évaluer de manière plus précise la réponse thérapeutique. Ce score reste cependant imparfait car il inclut des paramètres subjectifs comme le compte articulaire douloureux et l’évaluation de la maladie par le malade ; il doit dès lors faire l’objet d’une interprétation et d’une analyse des composantes objectives et subjectives du score DAS (4).
D’autres scores ont été développés pour évaluer l’activité de la maladie comme le SDAI (Simplified Disease Activity Index) et le CDAI (Clinical Disease Activity Index) (5). Ce dernier est facile à réaliser car il consiste en une simple addition des articulations douloureuses et gonflées, de l’activité de la maladie évaluée par le patient mais également par le médecin (4). Le SDAI prend en compte la CRP en plus des éléments précités et constitue donc le score le plus global.
La rémission, ou si elle n’est pas possible une activité faible de la maladie, doivent être l’objectif à atteindre (6,7). L’inflammation est la cible thérapeutique principale (1). En réduisant l’inflammation rapidement, nous pouvons prévenir les dommages articulaires irréversibles et améliorer la fonction physique du patient à long terme (6). Les 3 objectifs centraux sont la rémission, la prévention des déformations articulaires liées au dommage radiologique et la restauration de la qualité de vie sans handicap fonctionnel. Des objectifs additionnels seront intégrés dans la prise en charge chronique tels que l’amélioration des plaintes des patients (douleur, fatigue...), la prévention des maladies associées (cardiovasculaire, ostéoporose...), la prévention des complications infectieuses et la diminution des doses voire l’arrêt de certains traitements tels que la cortisone.
Le traitement
Le traitement repose sur 3 objectifs principaux et 4 additionnels selon l’évolution et la présentation clinique des patients souffrant de PR (figure 2).
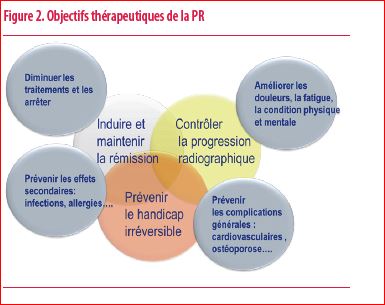
La littérature récente nous indique qu’une prise en charge précoce et intensive permet de modifier l’évolution de l’arthrite et de la PR (6,7).
La première médication pendant la phase de diagnostic et d’évaluation repose sur un traitement symptomatique par exemple par AINS (3) ou antalgiques en évitant les corticostéroïdes pour ne pas masquer la maladie.
Une fois le diagnostic établi, un traitement de fond par un csDMARD (conventional synthetic Disease-Modifying Antirheumatic Drug), idéalement le méthotrexate sera débuté (4,8). La dose initiale de méthotrexate peut être d’emblée de 15 mg par semaine associée à 5 mg d’acide folique le lendemain. La dose pourra être majorée jusque 20 mg/semaine après 4 semaines. Des glucocorticoïdes à faible dose (prednisolone inférieure à 7,5 mg par jour) peuvent être associés au méthotrexate en début de traitement. Les glucocorticoïdes devront cependant être réduits puis arrêtés endéans les 6 mois (1,3,9,10).
En cas d’échec après 3 à 6 mois d’évaluation ou d’intolérance, le méthotrexate pourra être associé ou remplacé par d’autres csDMARDs tels que la sulfasalazine, l’hydroxychloroquine ou le leflunomide (10).
Si une activité élevée de la maladie persiste malgré les csDMARDs, les patients peuvent bénéficier d’un traitement par bDMARDs (biologic Disease-modifying Antirheumatic Drug) ou par un inhibiteur des JAK kinases (10,11). L’indication d’un bDMARD est indispensable chez les patients réfractaires au csDMARDs avec des facteurs de mauvais pronostics (érosion précoce, DAS élevé, facteur rhumatoïde ou ACPA positifs). Ces traitements ont pu être développés suite à une meilleure compréhension de l’activation du système immunitaire en bloquant certaines protéines inflammatoires (TNF, IL-6...) ou en modulant les lymphocytes (T ou B). Les critères utilisés en Belgique sont une maladie active (DAS28-CRP > 3.7) malgré l’utilisation de 2 csDMARDs.
Il existe actuellement 4 types de bDMARDs avec des mécanismes d’action différents(1) :
- Agents bloquant le TNF (infliximab, adalimumab, certolizumab, etanercept et golimumab).
- Agents bloquant la co-stimulation avec le lymphocyte T (abatacept).
-Agents bloquant le récepteur de l’IL6 (tocilizumab, saralimumab).
- Agents inhibant les lymphocytes B (rituximab).
On dispose également de biosimilaires pour certaines de ces molécules. Les biosimilaires sont des molécules pharmaceutiques qui sont hautement similaires aux traitements biologiques déjà approuvés (11).
Les inhibiteurs des JAK kinases sont les dernières molécules arrivées sur le marché. Ce ne sont pas des traitements biologiques mais des molécules synthétiques ciblées permettant de moduler la voie enzymatique intracellulaire de la production des cytokines pro inflammatoires. Nous disposons des molécules suivantes en Belgique : tofacitinib, baricitinib, upadacitinib et filgotinib. Elles sont administrées une fois par jour par voie orale.
Lorsque le patient est en rémission sous traitement biologique depuis plus de 6 mois, une réduction de la dose du traitement biologique peut être proposée (après avoir réduit puis arrêté les glucocorticoïdes) (1,6,10).
En général, les bDMARDs sont bien tolérés. Il est à noter qu’ils majorent légèrement le risque infectieux, surtout respiratoire et cutané. Le risque d’apparition de tumeurs solides n’est pas augmenté dans la population traitée au long cours, seul le risque des cancers baso- ou spinocellulaires est légèrement augmenté. Le lymphome peut être observé sous biothérapie mais il est attribué à une complication potentielle de la PR et ce risque augmente en fonction de la sévérité de la maladie (12).
Les bDMARDs sont chers, un traitement d’une année représente un coût de 8 000 à 15 000 €. Il faut cependant prendre en considération les économies réalisables grâce à l’introduction précoce des traitements biologiques, avec une réduction des frais médicaux à long terme d’une maladie chronique par la prévention du handicap fonctionnel, des maladies associées et de la préservation de la vie socioprofessionnelle.
Outre les traitements médicamenteux, la prise en charge de la polyarthrite rhumatoïde doit être multidisciplinaire et reposer sur une prise en charge holistique par des moyens médicamenteux et non médicamenteux (infirmière coordinatrice et d’éducation, kinésithérapie…).
La recherche
Elle s’oriente vers des aspects de caractérisation physiopathologique de la PR débutante et sur des schémas thérapeutiques visant à maximaliser les taux de rémission. Des nouveaux auto-anticorps ont été découverts tels que les anti-protéines carbamylées, acétilées, les anti-PAD4, les anti-b-Raf ou anti-RA33. Ceux-ci ne peuvent malheureusement pas encore être demandés en pratique courante.
L’intérêt des biopsies synoviales réalisée par miniarthroscopie ou biopsie échoguidée des petites articulations permet de mieux explorer cette pathologie complexe sur le plan immunitaire. Les informations obtenues à partir de l’analyse du tissu synovial des patients souffrant d’arthrite sont susceptibles d’apporter une aide considérable au diagnostic en distinguant différents pathotypes selon les infiltrats cellulaires et, dans un futur peut-être proche, à la prise de décisions thérapeutiques en se basant sur l’analyse de l’expression des gènes inflammatoires et des signatures moléculaires. On pourrait en effet identifier des marqueurs de diagnostic précoce, de pronostic et de réponse thérapeutique. Nous avons d’ailleurs participé à une étude évaluant le bénéfice du Tocilizumab versus Rituximab chez des patients présentant une PR sévère et réfractaire. Cette étude a pu démontrer une majoration de la réponse selon un choix orienté par les marqueurs synoviaux (13). De plus, des études ayant réalisé du RNAseq en masse ont permis de montrer une corrélation entre certaines signatures transcriptomiques et la réponse au traitement (14,15). Nous pensons que l’analyse en single cell RNAseq permettra d’aller plus loin dans la mécanique de la PR débutante. Cette approche sera poursuivie dans notre service en 2022.
Par ailleurs, les études cliniques ont démontré que l’utilisation précoce des bDMARDs chez des patients présentant une PR débutante sévère apporte un bénéfice surtout marqué sur la prévention des destructions articulaires (11). Le traitement futur de la PR pourrait utiliser un bDMARD dès le diagnostic selon l’indication de biomarqueurs synoviaux et relayer le traitement par une phase de maintenance sous MTX. Cette approche ciblée et intensive dans la phase très précoce de la maladie permettrait d’induire un « reset » immunitaire. Nous nous orientons peut-être à l’avenir vers une médecine personnalisée où chaque patient aurait un schéma thérapeutique adapté aux caractéristiques et au pronostic de sa polyarthrite.
Conclusion
La connaissance plus précise de la physiopathologie, une meilleure évaluation clinique et l’avènement de nouveaux traitements ont permis de changer l’évolution de la polyarthrite. Des stratégies thérapeutiques ont ensuite pu être établies avec comme objectif principal la rémission ou du moins une activité faible de la maladie. Comme nous l’avons évoqué, la polyarthrite rhumatoïde peut causer un handicap fonctionnel majeur et impacter la qualité de vie de manière significative. Un diagnostic et une prise en charge précoces sont donc essentiels pour prévenir les conséquences potentielles de cette maladie.
Références
- Smolen JS, Aletaha D, McInnes. Rheumatoid arthritis. Lancet. 2016 Oct22;388(10055):2023-2038.
- Cross M, Smith E, Hoy D, Carmona L, Wolfe F, Vos T, et al. The global burden of rheumatoid arthritis: estimates from the global burden of disease 2010 study. Ann Rheum Dis. 2014 Jul;73(7):1316-22.
- Littlejohn EA, Monrad SU. Early Diagnosis and Treatment of Rheumatoid Arthritis. Prim Care. 2018 Jun;45(2):237-255.
- Aletaha D, Smolen JS. Diagnosis and Management of Rheumatoid Arthritis: A Review. JAMA. 2018 Oct 2;320(13):1360-1372.
- Mian A, Ibrahim F, Scott DL. A systematic review of guidelines for managing rheumatoid arthritis. BMC Rheumatol. 2019 Oct 22;3:42.
- Ajeganova S, Huizinga T. Sustained remission in rheumatoid arthritis: latest evidence and clinical considerations. Ther Adv Musculoskelet Dis. 2017 Oct;9(10):249-262.
- Legrand J, Kirchgesner T, Sokolova T, Vande Berg B, Durez P: Early clinical response and long-term radiographic progression in recent-onset rheumatoid arthritis: Clinical remission within six months remains the treatment target. Joint Bone Spine. 2019 Oct; 86(5):594-599.
- Bortoluzzi A, Furini F, Generali E, Silvagni E, Luciano N, Scirè CA. One year in review 2018: novelties in the treatment of rheumatoid arthritis. Clin Exp Rheumatol. 2018 May-Jun;36(3):347-361.
- Nam JL. Rheumatoid arthritis management of early disease. Curr Opin Rheumatol. 2016 May;28(3):267-74.
- Smolen JS, Landewé R, Bijlsma J, Burmester G, Chatzidionysiou K, Dougados M, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update. Ann Rheum Dis. 2017 Jun;76(6):960-977.
- Burmester GR, Pope JE. Novel treatment strategies in rheumatoid arthritis. Lancet. 2017 Jun 10;389(10086):2338-2348.
- Caporali R, Crepaldi G, Codullo V, Benaglio F, Monti S, Todoerti M, Montecucco C. 20 years of experience with tumour necrosis factor inhibitors: what have we learned? Rheumatology (Oxford). 2018 Oct 1 ;57 :7.
- Humby F, Durez P, Buch MH, et al. Rituximab versus tocilizumab in anti-TNF inadequate responder patients with rheumatoid arthritis (R4RA): 16-week outcomes of a stratified, biopsy-driven, multicentre, open-label, phase 4 randomised controlled trial. Lancet. 2021;397(10271):305-317.
- De Groof, Aurélie et al. “Higher expression of TNFα-induced genes in the synovium of patients with early rheumatoid arthritis correlates with disease activity, and predicts absence of response to first line therapy.” Arthritis research & therapy. 2016; vol. 18 19. 20.
- Humby, Frances et al. “Synovial cellular and molecular signatures stratify clinical response to csDMARD therapy and predict radiographic progression in early rheumatoid arthritis patients.” Annals of the rheumatic diseases. 2019 ; 78,6 (2019): 761-772.
Affiliations
1. Cliniques universitaires Saint-Luc, Pôle de Pathologies Rhumatismales Inflammatoires et Systémiques, Service de Rhumatologie, Département de Médecine interne, UCLouvain, B-1200 Bruxelles, Belgique
2. CHU UCL Namur, Hôpital de Mont-Godinne, Service de Rhumatologie, B-5530 Yvoir, Belgique
Correspondance
Dr. Emilie Sapart
Cliniques universitaires Saint-Luc
Service de Rhumatologie
Avenue Hippocrate 10
B-1200 Bruxelles
emilie.sapart@uclouvain.be