La radiothérapie adaptative devient une réalité aux Cliniques universitaires Saint-Luc : une nouvelle prouesse de l’intelligence artificielle au service du patient
Xavier Geets
Dans sa quête de précision, l’innovation technologique est au cœur des plus grands progrès de la radiothérapie. L’amélioration des techniques d’imagerie, de monitoring du patient, et de délivrance de dose des accélérateurs modernes offre aujourd’hui des traitements d’une précision sans précédent. Mais l’arrivée récente de l’intelligence artificielle ouvre de nouvelles perspectives, qui vont profondément modifier la prise en charge de nos patients : la radiothérapie adaptative et individualisée pour chaque patient et à chaque séance de traitement devient enfin une réalité.
Les enjeux de la radiothérapie adaptative
La radiothérapie conventionnelle se contente de définir la balistique d’irradiation sur base d’un unique CT scanner de simulation acquis quelques jours avant le début de la radiothérapie. Par nature, elle néglige donc les modifications anatomiques qui surviennent durant le traitement de radiothérapie, généralement délivré sur plusieurs semaines. Pourtant, les changements de volume de la tumeur, de la position et de la forme des organes de voisinage, par exemple liées aux fluctuations du remplissage de la vessie, de l’estomac, des intestins ou du rectum, ou encore l’amaigrissement, affectent la majorité des patients.
Ces changements anatomiques imprévisibles impactent souvent sévèrement la précision du traitement, conduisant tantôt à un sous-dosage de la tumeur, tantôt à une surexposition des organes de voisinage, au détriment de l’efficacité et de la sécurité du traitement. La solution à ce problème est conceptuellement simple, et consiste à adapter la balistique d’irradiation en fonction de l’anatomie du patient à chaque séance de radiothérapie. C’est ce qu’on appelle la radiothérapie adaptive. Néanmoins, son implémentation clinique s’avère complexe…
Une première solution consiste à obtenir un nouveau CT scanner avant chaque séance de radiothérapie, sur lequel le radiothérapeute délimite la tumeur et les organes à risque dans leur configuration actuelle, et le physicien médicale ré-optimise la dose. Ces tâches manuelles sont néanmoins extrêmement laborieuses et consommatrices de temps. Elles requièrent d’énormes ressources en personnel, et sont incompatibles avec la généralisation de cette approche à l’ensemble des patients.
Pour devenir une réalité clinique, la radiothérapie adaptative nécessite donc l’automatisation des tâches de planification du traitement. Bien que de nombreux outils informatiques aient vu le jour pour assister les opérateurs, ils étaient jusqu’à présent imparfaits, et nécessitaient trop de temps et d’interventions humaines que pour envisager une intégration efficiente en routine clinique.
L’intelligence artificielle, la clé du succès
Le succès de la radiothérapie adaptative repose sur sa simplicité et sa rapidité d’exécution. Un traitement adaptatif court limite le risque de mouvements du patient et des organes pendant la séance de radiothérapie, qui anéantiraient les bénéfices de la radiothérapie adaptative. De plus, un traitement rapide permet d’améliorer le rendement de l’accélérateur afin d’offrir cette innovation au plus grand nombre.
Afin de délivrer un traitement adaptatif en 15 à 20 minutes, les outils d’optimisation doivent être précis, rapides et robustes, pour limiter les interventions humaines gourmandes en temps et en ressource. L’intelligence artificielle entrainée sur de grandes bases de données offre ces performances, tant pour la délimitation automatique des organes que pour l’optimisation intelligente de la dose.
Quand le rêve devient réalité
Le service de radiothérapie des Cliniques universitaires Saint-Luc s’est équipé en 2021 d’une solution commerciale de radiothérapie adaptative, l’accélérateur Ethos® (Varian), une première en Belgique ! (Figure 1)
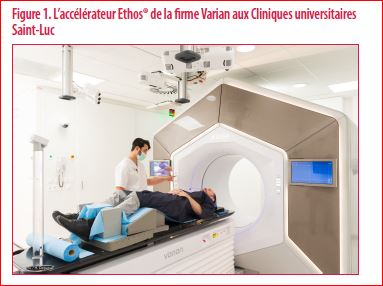
Cette solution résolument innovante a été entièrement conçue pour répondre aux exigences de la thérapie adaptative. Elle combine un accélérateur équipé des dernières technologies de radiothérapie par modulation d’intensité, une imagerie embarquée par Cone-Beam CT de haute qualité pour capturer l’anatomie du patient à chaque séance, et de puissants outils d’intelligence artificielle. Chaque étape du traitement a été entièrement repensée pour une exécution simple, largement automatisée, au travers d’une interface intuitive guidant l’utilisateur pas à pas dans la procédure adaptative.
Lors de la planification initiale du traitement, l’Ethos® propose de façon automatique plusieurs configurations de traitement sur base des contours et des objectifs de dose souhaités, fournis par l’utilisateur. Il ne reste alors au radiothérapeute qu’à choisir le plan de traitement qui convient le mieux au patient.
Lors du traitement adaptatif, l’intelligence artificielle génère automatiquement les contours des organes à partir de l’imagerie par Cone-Beam CT, et ré-optimise le plan de traitement à l’anatomie du jour afin de rencontrer les objectifs de dose initialement fixés par le radiothérapeute. L’utilisateur peut alors opter pour le plan adaptatif si la situation le justifie. Simple et efficace !
L’Ethos® au quotidien
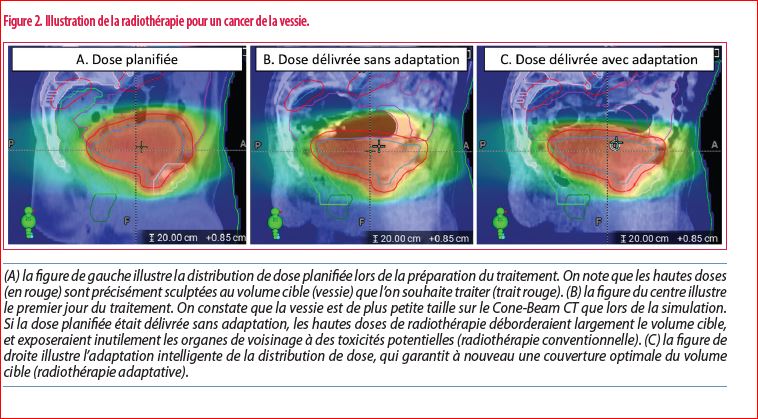
Les patients porteurs d’un cancer de la prostate ont été les premiers à bénéficier de cette innovation, accessible dans notre service depuis le mois d’aout 2021. Ce choix est justifié à la fois par la prévalence élevée de cette pathologie en radiothérapie, et par le bénéfice attendu de la radiothérapie adaptative dans une anatomie pelvienne en perpétuel changement (lié au remplissage de la vessie, du rectum et des intestins). Pour cette même raison, nous avons récemment étendu les indications aux cancers de la vessie et des lymphomes de l’estomac, pour lesquelles un ciblage précis nécessite une thérapie adaptative (Figure 2).
Néanmoins, ces traitements requièrent une supervision humaine afin de valider ce que propose l’intelligence artificielle, et de le corriger si nécessaire. Aujourd’hui, cette supervision est encore assurée par le radiothérapeute et le physicien médical. L’impact sur ces ressources humaines limite donc le nombre de plages disponibles pour les patients. Mais demain, cette tâche sera largement déléguée aux infirmières et technologues (RTT). Une formation spécifique aux tâches de contourage et de dosimétrie, en plus d’un entrainement sur le terrain, sont actuellement en cours. Le train du changement est en route, et offrira aux infirmières et technologues plus de responsabilités, de diversité dans leur travail, et permettra d’étendre les indications de cette technique innovante à plus de patients.
Lorsque évolution technologique rime avec révolution clinique, soignants et patients ne peuvent que se réjouir. La radiothérapie adaptative deviendra certainement la nouvelle référence de demain, à l’instar des thérapies ciblées en oncologie, pour des traitements toujours plus personnalisés, efficaces et sûrs.
La ventilation mécanique non-invasive (MANIV) en radiothérapie : première expérience clinique
Loic Vander Veken
Etat des lieux
Parce qu’elle met en mouvement la tumeur à irradier, la respiration est une source majeure d’incertitudes en radiothérapie de la région thoracique et abdominale haute. L’irradiation délivrée lors d’apnées inspiratoires s’est donc imposée comme une technique de choix. En effet, elle supprime les incertitudes géométriques liées au mouvement respiratoire, et permet ainsi de réduire le volume d'irradiation. En outre, la distension pulmonaire augmente la distance entre la tumeur et des organes à risque critiques tels que le cœur. Cependant, la délivrance d’une fraction requiert en moyenne une dizaine d’apnées successives de 20 à 30 secondes. La reproductibilité et la stabilité positionnelle de la tumeur lors de chaque apnée constitue ainsi un enjeu crucial pour que la cible reçoive la dose thérapeutique prescrite. De plus, les comorbidités du patient mettent souvent à mal la faisabilité d’un tel exercice. En reproduisant parfaitement les mêmes paramètres ventilatoires au cours du temps tout en allégeant le travail respiratoire du patient, la ventilation mécanique non-invasive (MANIV) offre une solution simple et accessible à cette problématique complexe.
Aspects techniques et implémentation clinique
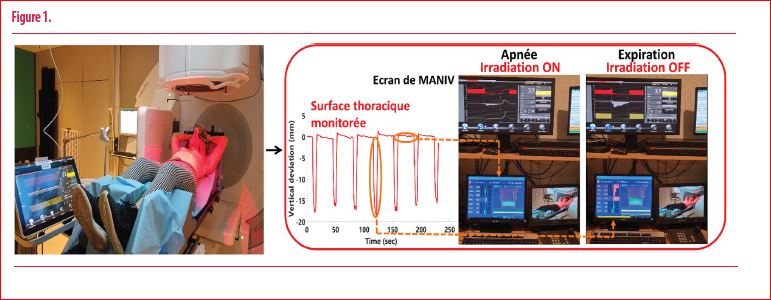
Comme illustré à la figure n°1, le patient est connecté au respirateur sans aucune médication ni sédation préalable. La ventilation mécanique fonctionne sur un mode BiPAP où deux niveaux de pression s’alternent avec de l’air enrichi en oxygène (FiO2 60 %) : le niveau élevé (18 à 20 mbar) est maintenu pendant 25 à 30 secondes et induit une inspiration puis une apnée. La pression chute ensuite à 0 mbar permettant au patient d’expirer avant de réenclencher la même pression positive. Ce cycle est maintenu pendant toute la durée d’une fraction soit 10 à 20 minutes. Le faisceau d’irradiation est synchronisé au pattern respiratoire du patient et s’interrompt automatiquement en phase expiratoire grâce à une imagerie optique qui capte en temps réel le mouvement de la surface thoracique. Notons enfin que le respirateur est interfacé avec la salle de commande de la machine de traitement d’où il peut être entièrement contrôlé.
Traitement du cancer du sein
Un essai randomisé comparant apnées spontanées guidées par imagerie surfacique et apnées induites par MANIV a été mené aux Cliniques Universitaires Saint-Luc (CUSL)1. Les patientes inclues présentaient un cancer du sein gauche sans envahissement ganglionnaire. Il en ressort que la reproductibilité et la stabilité positionnelle du sein irradié est la même dans les deux bras. En outre, le bras MANIV démontre une réduction significative de la dose au cœur et au poumon gauche grâce à l’effet combiné d’une plus grande inflation du volume pulmonaire et d’une réduction plus importante du volume cardiaque en apnée. Par ailleurs, aucune dégradation du confort ni déviation anormale des paramètres vitaux n’a été détectée.
Traitement des tumeurs du poumon par radiothérapie stéréotaxique
La première patiente au monde a été traitée dans notre service par radiothérapie stéréotaxique avec MANIV en mai 2021 pour un adénocarcinome pulmonaire lobaire supérieur droit. Un grain d’or a été implanté dans la tumeur afin de pouvoir reconstruire la trajectoire de la tumeur au départ de ses projections radiologiques acquises en cours d’irradiation. Il en résulte un très haut niveau de précision d’irradiation où la quasi-totalité des positions de la tumeur était à moins de 5 mm de sa position de référence et 85 % des positions à moins de 3 mm. Deux autres patients ont été traités avec succès pour la même indication dans le cadre d’un essai clinique de faisabilité.
Références
- Vander Veken L., van Ooteghem G., Longton E., Ledoux B., Abdel Massih C., Delvaux C. et al. (2021). PO-1141 Voluntary vs. mechanically induced DIBH for left breast cancer : a randomized trial. Radiotherapy and Oncology. 161, S948-S950. https://doi.org/10.1016/s0167-8140(21)07592-7
Imprimante 3D et radiothérapie
Antoine Delor, Emmanuel Bonnarens, Françoise Vanneste
Le service de radiothérapie des Cliniques Universitaires Saint-Luc a fait l’acquisition d’une imprimante 3D Raise Pro2 Plus en 2021 toujours dans le but d’améliorer la qualité des traitements.

L’impression 3D permet la création de toute sorte d’objets utilisés lors du traitement des patients.
Ces objets peuvent-être :
- Des bolus, matériel utilisé pour traiter avec un faisceau de photons des zones proches de la peau, ou la peau elle-même. Les bolus sont généralement des feuilles de silicone d’épaisseur variant en fonction de la profondeur de la zone d’intérêt (de 5mm à 2cm). Ces feuilles sont de dimension standard et souples, il faut donc les coller au patient pour essayer de les garder le plus possible en contact avec celui-ci. Cette solution n’est pas parfaite, car le bolus n’est pas toujours contre la peau du patient, dans les zones ayant des plis par exemple. Grâce à l’impression 3D, on peut créer le bolus dans le logiciel de planification de la délivrance de dose et envoyer le contour créé vers l’imprimante pour mouler un bolus qui épouse bien la forme du patient tout en restant légèrement souple pour s’adapter aux modifications anatomiques du patient tout au long de son traitement.
- Des protections en plomb: ceux-ci permettent de mieux conformer la dose autour de la zone à traiter dans les traitements superficiels en électrons. L’impression de la zone à irradier a remplacé la découpe d’un bloc de polystyrène expansé avec un fil chauffé, technique moins précise. On peut ensuite couler du plomb autour de ce bloc.

- Des protections pulmonaires sont parfois utilisées en radiothérapie, par exemple lors de irradiations corporelles totales. Ces protections sont composées de feuilles de plomb découpées suivant la forme des poumons. Cette forme est créée dans le logiciel de calcul de dose, et est ensuite envoyée vers l’imprimante 3D. Elle servira de patron pour la découpe des feuilles de plomb.

On voit ainsi qu’une imprimante 3D peut être utilisée pour des projets qui, par le passé, nécessitaient différentes machines spécialisées. On peut aussi mieux adapter certains traitements au patient.
D’autres façons d’utiliser l’impression 3D existent encore, comme l’impression de matériel pour les mesures de vérification de plan de traitements spécifiques à chaque patient, la création de fantômes permettant de faire des mesures dans des conditions non-standard, du matériel pour mieux positionner le patient, etc.
Affiliations
1. Chef de service de radiothérapie
2. Physicien médical en radiothérapie
3. Ingénieur chef de projet
4. Responsable du service de physique médicale aux CUSL
5. Assistant en radiothérapie, aspirant FNRS
Correspondance
Pr. Xavier Geets
Cliniques universitaires Saint-Luc
Service de Radiothérapie
Avenue Hippocrate 10B-1200 Bruxelles