OBSERVATION
Le premier cas remonte à l’année 2000. La patiente, alors âgée de 30 ans, présente, le lendemain de la 5ème séance de sclérose de télangiectasies, une douleur importante et un gonflement de la jambe traitée (jambe droite). Une douleur était apparue dans la soirée. Une thrombose veineuse profonde distale (veine jumelle interne) est diagnostiquée par écho doppler et un traitement médicamenteux par héparine de bas poids moléculaire (HBPM) à dose thérapeutique est débuté (Fraxiparine ® 0,5 ml 2X/J) associé à un traitement mécanique par des bas de contention.
L’anamnèse n’avait pas permis de mettre en évidence un facteur de risque particulier. Elle est sous contraception orale à base de désogestrel (Cerazette®) car elle est fumeuse. Elle a eu deux grossesses sans complication thrombo-embolique.
L’anamnèse familiale n’est pas contributive. Elle est de taille et de corpulence normale (BMI : 21,41 Kg/m2).
Le bilan thrombophilique documente une hétérozygotie pour la mutation G20210A du gêne du facteur II (prothrombine) sans mutation Leiden du facteur V ni autre anomalie thrombophilique (absence de déficit en antithrombine, protéines C et S, anticorps anti-phospholipidies). Malgré le port de bas de contention, cette patiente a présenté, douze ans plus tard, une embolie pulmonaire spontanée à la suite de laquelle un traitement par antivitamine K (acenocoumarol) a été introduit.
La deuxième patiente est âgée de 42 ans. Elle a deux enfants. Elle ne présente pas de facteur de risque particulier connu de maladie thromboembolique veineuse. Nous apprenons cependant par la suite qu’elle a présenté une thrombose ophtalmique il y a de nombreuses années qui avait probablement orienté, à l’époque, le choix d’une contraception par une pilule progestative faiblement dosée (Cerazette®). Elle en est à sa 8ème séance de sclérothérapie pour télangiectasies, sans incident. Elle est de corpulence normale (BMI : 20,2 kg/m2).
Seule la jambe gauche est sclérosée. La patiente omet de nous signaler qu’elle a prévu un séjour à New York une semaine plus tard. Le lendemain de son arrivée, elle présente une thrombose veineuse profonde de la veine fémorale droite malgré le port de bas de bas de compression pour le vol. Elle a été traitée par Héparine de Bas Poids Moléculaire (HBPM) à dose thérapeutique et contention.
Le bilan thrombophilique documente également une hétérozygotie isolée pour la mutation G20210A du facteur de la prothrombine (facteur II) sans mutation Leiden du facteur V associée. Le reste du bilan ne montre aucune autre anomalie de nature thrombophilique. Le dépistage familial démontre que seul, le père, est porteur de cette mutation.
DISCUSSION
Rappel des principes de la sclérose et du lauromacrogol (1-10)
La sclérose est le traitement le plus courant des varices de petit et moyen calibre et des télangiectasies. Elle peut également être utilisée après chirurgie pour traiter les varices résiduelles. Elle est réalisée en ambulatoire, son coût est peu important. La dose et la concentration du sclérosant sont modulables selon le site et le calibre à traiter. La technique consiste à injecter un produit sclérosant dans les varices, au cours de différentes séances. Le principe de la sclérothérapie consiste donc à injecter une substance irritante pour la paroi du vaisseau entraînant son occlusion par thrombose locale.
Le lauromacrogol (polidocanol) est le principe actif. Initialement, il a été développé comme anesthésique. Il n’a qu’un effet anesthésiant faible et uniquement en administration topique. Il est utilisé dans des produits cosmétiques (crèmes hydratantes, solaires, shampooings). Son pouvoir sclérosant est durable pour les varices de tout calibre. L’importance des lésions de l’endothélium vasculaire après injection dépend de la concentration et du volume injecté. Le lauromacrogol 400 est utilisé à différents dosages en Belgique : 0,5%, 1%, 2% et 3%. Il est conditionné en ampoules de 2 ml. Il est indiqué pour la sclérose de varices (y compris les télangiectasies et les varices œsophagiennes) et d’hémorroïdes. Pour la sclérose des télangiectasies, on emploie généralement le dosage de 0,5%. On peut cependant utiliser le 1% pour des télangiectasies de calibre plus important.
L’injection est réalisée à l’aide d’aiguilles très fines, en petites doses individuelles (0,3 à 0,5 ml). La forme mousse peut être utilisée pour des télangiectasies fines mais elle est le plus souvent utilisée pour des varices de plus de 3 mm (3,4). Lors des scléroses, il est recommandé d’appliquer un morceau de coton et un bandage compressif pendant minimum 1-2 jours après la sclérose à l’endroit traité. Cependant, l’intérêt de la compression pour les télangiectasies est controversé. Il n’est démontré que par un petit nombre de publications (5).
Les contre-indications sont l’hypersensibilité au lauromacrogol ou à l’un des excipients (éthanol, phosphate disodique hydraté, potassium dihydrogen phosphate, eau pour injection), une maladie systémique aiguë grave (en particulier si non traitée), la prise de disulfiram. L’effet disulfiram se caractérise par des bouffées vasomotrices, vasodilatation, céphalées, nausées, vomissements, tachycardie, dyspnée, lipothymie lors de l’absorption d’alcool en association avec la prise de disulfiram. Les injections sont également contre-indiquées chez les patients immobiles (alitement...), les patients atteints de maladie artérielle occlusive grave (Fontaine stade III et IV), les patients atteints de maladie thromboembolique et les patients à risque de thrombose (les patients avec thrombophilie héréditaire connue). Cette contre-indication est cependant relative. Les modalités thérapeutiques et précautions en cas de thrombophilie génétique sont détaillées plus loin. La sclérose est fortement déconseillée chez les patients avec de multiples facteurs de risque de maladie thrombo-embolique veineuse tels que l’utilisation d’un contraceptif ou substitut hormonal (ménopause), l’obésité, le tabagisme ou les périodes longues d’immobilité. Il est recommandé d’éviter les scléroses pendant la grossesse et d’interrompre l’allaitement pendant 3 jours après la sclérose. Le port d’une compression est nécessaire après la sclérose. L’immobilisation (alitement ou long voyage) doit être évitée après la sclérose (minimum une semaine) ainsi que l’exposition au soleil et à la chaleur (plusieurs semaines).
L’injection intra-artérielle est, bien évidemment, proscrite. Pour cette raison, il est recommandé de n’injecter qu’une très faible quantité au niveau du pied et de la malléole vu le risque accru d’injection accidentelle en intra-artériel. L’injection au niveau du visage n’est pas conseillée (l’injection intravasculaire peut inverser la pression artérielle et engendrer une cécité).
La prudence est recommandée si l’épiderme est altéré à l’endroit de la sclérose (atrophie blanche), en présence de signes de micro-angiopathie ou de neuropathie, en présence d’œdème, en cas de fièvre, en cas d’asthme ou de prédisposition aux allergies, en cas d’altération de la santé (cardiopathie, âge avancé..), en cas de maladie artérielle occlusive (Fontaine II) pour les télangiectasies.
La sclérose sous forme de mousse peut être relativement contre-indiquée chez des patients présentant un foramen ovale perméable connu, des symptômes visuels, mentaux ou neurologiques survenus lors de sclérose antérieure sous forme de mousse. La fréquence d’un foramen ovale ouvert est estimée, chez l’adulte, à 20%. (2,9). Il n’est cependant pas recommandé de réaliser de dépistage préalable.
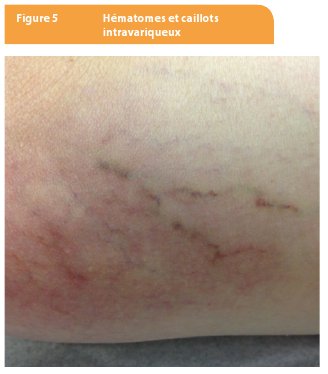
Les effets indésirables les plus fréquents sont les réactions indésirables locales, la nécrose de la peau et des tissus sous-jacents (Figures 1 et 2). Ces réactions sont dépendantes de la dose et de la concentration. On observe fréquemment (≥1/100, <1/10) de l’hyperpigmentation locale, des ecchymoses, peu fréquemment (≥ 1/1000, <1/100) de la dermatite allergique, de l’urticaire de contact, de l’érythème et très rarement de l’hypertrichose (<1/10000). La dermite livédoïde de Nicolau (Figures 3-4) n’est pas reprise dans le résumé des caractéristiques du produit (RCP) mais a été observée (8). Elle est exceptionnelle après sclérose de télangiectasies. Les douleurs au site d’injection sont fréquentes ainsi que les caillots sanguins intravariqueux (Figure 5). Les nécroses, indurations, tuméfactions, persistance de cicatrices, escarres, œdèmes des chevilles sont peu fréquentes. Les bouffées vasomotrices, malaises, asthénie et pyrexie sont très rares.
D’autres effets sont décrits : réactions allergiques plus ou moins sévères, céphalées, syncopes, étourdissement, paresthésies, diminution de la sensibilité locale, accident vasculaire cérébral, perturbation de la vue (surtout avec la forme mousse), palpitations, troubles tensionnels, hématomes, thrombophlébite superficielle, périphlébite. On décrit également des douleurs des extrémités (rare), Les thromboses veineuses profondes sont rares (≥ 1/10.000, <1/1000) et probablement liées à une pathologie sous-jacente. On a très rarement (< 1/10.000) décrit des embolies pulmonaires, syncopes vaso-vagales, collapsus circulatoires et vasculites. On observe très rarement (<1/10000) des symptômes respiratoires (dyspnée, toux), de la dysgueusie, des nausées.


Rôle du lauromacrogol (Aethoxysclérol®)
Si, dans le premier cas décrit ci-dessus, le rôle de la sclérose semble évident, dans le second cas présenté, la thrombose concerne la jambe non traitée. Elle survient une semaine après la sclérose et la patiente a effectué un vol en avion d’une durée de 7 heures. On peut envisager une action systémique du lauromacrogol associée à la thrombophilie génétique et à la durée du vol. Le rôle de la sclérose ne peut cependant être démontré en raison des deux autres facteurs de risque.
Rôle du désogestrel (Cerazette®) (11-12)
Celui-ci n’a probablement pas favorisé le développement d’une thrombose chez nos patientes car les contraceptifs à base d’un progestatif seul sont recommandés chez les femmes qui présentent des antécédents ou des facteurs de risque de thrombo-embolie veineuse car ils exercent peu d’effet sur la coagulation et n’ont pas montré d’augmentation significative du risque d’accident cardiovasculaire ou de TEVP (thrombo-embolie veineuse profonde) dans les études épidémiologiques. Les contraceptifs à base d’un progestatif seul faiblement dosé sont généralement considérés comme un bon choix chez les femmes avec un risque accru de thrombose veineuse. Bien que le RCP de Cerazette® rappelle que les études épidémiologiques montrent une augmentation de l’incidence des thrombo-embolies veineuses avec les contraceptifs oraux, elle souligne que l’importance de cette observation n’est pas connue pour le désogestrel en l’absence de composant œstrogénique. Il est cependant recommandé d’interrompre la prise de désogestrel en cas de thrombose ou en cas d’immobilisation prolongée et d'avertir les femmes ayant des antécédents d’affection thrombo-embolique du risque de récidive.
Thrombophilie et mutations génétiques (13-22)
Le terme thrombophilie est utilisé pour désigner une prédisposition à la thrombose (thrombose veineuse profonde, embolie pulmonaire) suite à des troubles de l’hémostase d’origine acquise ou liés à une prédisposition héréditaire.

L’anamnèse personnelle et familiale est capitale : antécédents personnels médicaux, chirurgicaux, prise médicamenteuse, antécédents familiaux... La thrombo-embolie est souvent multifactorielle. Le rôle des contraceptifs oraux œstro-progestatifs, de la grossesse, de l’immobilisation n’est plus à démontrer. Des tests sanguins permettent de dépister un déficit en anticoagulants naturels (antithrombine, protéine C, protéine S). La question est de savoir quand et chez qui les bilans doivent être effectués et lesquels.

Le syndrome des anticorps antiphospholipides est une affection acquise, auto-immune, qui est présente chez 0,5-3% de la population (20-40% en cas de lupus systémique) (20).
Les thrombophilies héréditaires sont des mutations génétiques : le facteur V de Leiden (résistance à la protéine C activée) et la mutation du gène de la prothrombine ainsi que des déficits en anticoagulants naturels (antithrombine, protéine C, protéine S).
La mutation du facteur V de Leiden est l’anomalie génétique la plus fréquente. Cette mutation est présente chez 2-5% de la population caucasienne pour la forme hétérozygote et 0,02% pour la forme homozygote mais les chiffres varient fortement selon les sources (13-14). Elle toucherait une personne sur 20 en Belgique.
La mutation du gène de la prothrombine (facteur II) (17) est la seconde en fréquence et engendre une augmentation du taux de prothrombine (précurseur de la thrombine). Elle touche 2-4% de la population de race blanche. Sa transmission est autosomique dominante.
Les mutations génétiques responsables d’un déficit d’un des anticoagulants naturels (AT, PC, PS) sont rares (moins de 1%). Leur transmission est généralement autosomique dominante. Puisqu’il existe de nombreuses mutations, on ne réalise pas de test génétique pour établir le diagnostic. On dose l’activité de la protéine et son antigène.
La prévalence de ces affections et le risque relatif d’accidents thrombo-emboliques varient quelque peu selon les sources. Le risque thrombo-embolique est donc, comme nous l’avons signalé ci-dessus, lié à plusieurs facteurs acquis, environnementaux et génétiques. Pour évaluer le risque thrombo-embolique, l’histoire personnelle et familiale est essentielle.


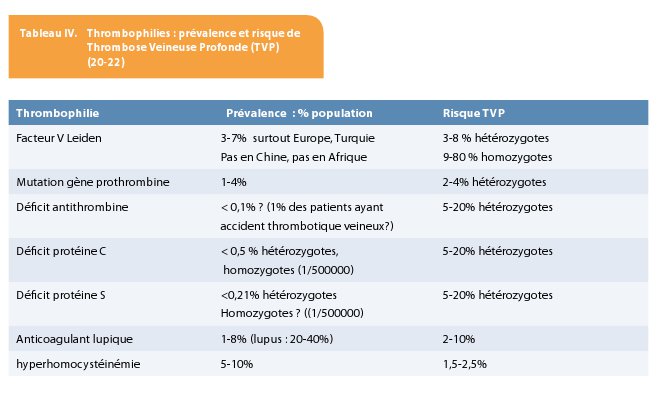
Quand faut-il rechercher une thrombophilie?
La Haute Autorité de Santé française a établi les indications suivantes (Tableau V).

Les bilans devraient idéalement être décidés en concertation avec un médecin biologiste spécialisé dans la coagulation ou un hématologue. Celui-ci peut aider le clinicien à réaliser les examens les plus appropriés et à évaluer le cas échéant l’intérêt d’un bilan génétique (personnel et familial). Le coût de ces examens doit également être pris en compte.
Sclérose et thrombophilie (23-39)
Si l’on tient compte de toutes les causes de thrombophilie (acquises ou héréditaires), le nombre de thrombophiles peut être estimé à un minimum de 15% dans la population générale. En outre, on estimait, en 2005, rien qu’en France, le nombre de scléroses de varices à 5-6 millions par an. En Belgique, en 2015, 123 481 séances d’injections sclérosantes de veines ont été réalisées, toutes spécialités confondues (codes 144071-144082 : injection sclérosante des veines, pour varices, par séance) (32). On peut donc suspecter que les scléroses réalisées chez des thrombophiles connus ou non sont nombreuses.
Le nombre d’accidents thrombo-emboliques (ATE) après sclérose dans une population générale semble très faible d’après la littérature. Le nombre de TVP, toutes scléroses confondues, serait de 0,02%- 0,6% (25-36) mais il est probablement sous-estimé car de nombreuses thromboses évoluent à bas bruit, les médecins ne déclarent pas systématiquement les accidents et le lien n’est pas nécessairement fait avec l’acte sclérosant car le patient consulte généralement un service d’urgence. De plus, après un ATE, un bilan de thrombophilie n’est pas toujours réalisé. Il n’y a que peu de cas rapportés où la thrombophilie a été révélée par la sclérose (29-38). En Belgique, les deux cas présentés dans cet article sont les deux seuls enregistrés dans EudraVigilance rapportant une TVP survenue en Belgique, pour lesquels le lauromacrogol 400 est suspecté d’avoir joué un rôle, et ce, depuis la commercialisation du produit.
Sur le site public de l’EMA (Agence Européenne des Médicaments) donnant accès à EudraVigilance, on peut voir qu’il y a, à ce jour, 16 rapports de «deep vein thrombosis» associés à la substance lauromacrogol 400 (total cumulé des cas spontanés graves notifiés dans le monde depuis la commercialisation du produit). Les informations présentées sur ce site ont trait aux effets indésirables suspectés, en d’autres termes, aux effets qui ont été observés à la suite de l’administration d’un médicament ou d’un traitement par un médicament. Cependant, ces effets indésirables suspectés peuvent ne pas être liés au médicament ou provoqués par ce dernier (34). Thiollet et Lajou ont, comme nous, décrit deux cas de thrombose veineuse profonde révélant une thrombophilie. Il s’agissait d’une mutation hétérozygote du gène codant pour le facteur V (facteur V de Leiden). Cette mutation était, dans ces deux cas, ignorée avant la sclérose (35). Azoulay et ses collaborateurs ont réalisé une enquête téléphonique auprès des angiologues français en 1997 et 1999. Ceux-ci ont observé 18 accidents thromboemboliques dont 13 cas de TVP dans les suites d’une sclérothérapie. Tous ces cas étaient féminins. 12 patientes étaient porteuses d’une thrombophilie constitutionnelle (2 cas sur 3) (36). Une revue rétrospective de 2003, en France, fait état de 134 patients présentant une thrombophilie dont 56 ont été traités par sclérose, 5 patients (9%) ont présenté une thrombose veineuse. Dans ces 5 cas, il s’agissait de patients dont la thrombophilie était ignorée avant la sclérose (37).
Le praticien doit être conscient que la sclérose peut être un facteur favorisant de TVP et ce, même en cas de sclérose de varicosités comme dans les deux cas présentés où la thrombophilie était ignorée.
Bien que le RCP de l’Aethoxysclérol® stipule que la thrombophilie est une contre-indication pour la sclérose, plusieurs auteurs considèrent qu’une thrombophilie n’est pas une contre-indication absolue. Il faut tenir compte du type de thrombophilie et du traitement de celle-ci. Une étude a été réalisée par Hamel-Desnos et collaborateurs sur 199 scléroses, dont 105 chez des patients thrombophiles connus et sous traitement. Les incidents étaient rares (thrombophlébites superficielles : 1,5% et réactions inflammatoires : 1,5%) et n’étaient pas supérieurs à ce qui est observé dans la population générale (38). Ces auteurs ont établi les propositions suivantes pour le sclérothérapeute (37-38). La sclérose est absolument contre-indiquée dans les cas de déficit en antithrombine et dans le syndrome des anticorps antiphospholipides confirmé. Le risque de thrombose est élevé dans le cas de la mutation du facteur V (homozygote) et de la prothrombine (homozygote) ainsi que dans les déficits en protéines C et S mais des scléroses pourraient être effectuées si le patient est sous antivitamine K depuis longtemps ou, si ce traitement est récent, en ajoutant, à l’antivitamine K, une injection d’héparine de bas poids moléculaire (4000 UI) 1X/j pendant 7j. Le risque est modéré en cas de mutation du facteur V (hétérozygote), de la prothrombine (hétérozygote), d’hyperhomocystéinémie, du syndrome des anticorps antiphospholipides asymptomatique et d’un taux élevé de facteur VIII. Dans ces cas, ils proposent d’évaluer la situation selon la clinique. La sclérose pourrait être effectuée si le patient est sous antivitamine K depuis longtemps. Si le patient n’est pas sous antivitamine K depuis longtemps, on ajoute à celui-ci soit une seule injection d’héparine de bas poids moléculaire lors de la sclérose à la dose de 4000 UI, soit une injection d’héparine de bas poids moléculaire (4000 UI) 1X/j pendant 7j.
Il n’est pas recommandé de réaliser un bilan de thrombophilie avant la sclérose mais une bonne anamnèse personnelle et familiale est indispensable.
Cet article est l’occasion de rappeler aux professionnels de la santé l’importance de notifier les effets indésirables suspectés à l’afmps, via le système des fiches jaunes (39).
CONCLUSIONS
La sclérothérapie est un traitement des télangiectasies et des varices de petits et moyens calibres. Elle est également utilisée en complément ou en alternative à la chirurgie. Elle peut être effectuée en ambulatoire, son coût est peu important et est réalisée en plusieurs séances. La fréquence, la dose et la concentration du sclérosant sont modulables selon le site et le calibre. L’anamnèse est très importante, pour ne pas négliger une thrombophilie sous-jacente. L’immobilisation (alitement ou long voyage) doit être évitée après la sclérose (minimum une semaine) ainsi que l’exposition au soleil et à la chaleur (plusieurs semaines). Il n’est pas recommandé de réaliser une sclérose pendant la grossesse et une interruption d’allaitement de 3 jours est recommandée après la sclérose.
Les thromboses veineuses profondes (TVP) survenant après sclérose sont probablement sous estimées. Elles peuvent révéler une thrombophilie.
Il est important d’insister sur l’anamnèse des patients avant tout traitement par sclérose et sur la déclaration de tout incident thérapeutique.
À l’heure où la demande de sclérose pour des raisons esthétiques est constamment en augmentation, la question de la responsabilité médico-légale en cas d’accident doit être prise en compte.
Recommandations pratiques
- L’anamnèse personnelle et familiale est fondamentale avant tout acte de sclérose. Il n’est pas recommandé de réaliser un bilan de thrombophilie.
- La sclérose veineuse peut engendrer un accident thromboembolique, si minimes soient les concentrations et les doses injectées.
- La thrombophilie est fréquente : 15% de la population mais ne constitue pas une contre-indication absolue à la sclérose.
- Les patients doivent être éduqués afin de consulter en cas de plaintes ou de signes cliniques suspects de complications thrombotiques.
- L’anamnèse de tout patient se présentant avec une thrombose veineuse doit explorer des antécédents récents de sclérose veineuse, même limitée.
Affiliations
(1) Service de dermatologie
(2) Dermatologie, chef de service
(3) Médecin biologiste, chef de service
Clinique Saint-Pierre, Avenue reine Fabiola 9, B-1340 Ottignies
Correspondance
Dr. Cécile Courtin
Clinique Saint-Pierre
Dermatologie
Avenue reine Fabiola 9
B-1340 Ottignies
docteurcourtin@hotmail.fr
Références
1) Aethoxysclerol lauromacrogol 400 (polidocanol) Sclérose des télangiectasies et des varices pour des jambes saines et belles Sigma Tau, Pharma Belgium s.p.r.l. Bruxelles sclerotherapy@sigma-tau.be 2013.
2) http///bijsluiters.fagg-afmps.be/?localeValue=fr . Résumé des Caractéristiques du Produit (RCP)
3) Haxhe J-P. La sclérothérapie. Glem dermatologie, Ottignies, 2016
4) Breu FX, Guggenbichler S, Wollmann JC. 2nd European Consensus Meeting on Foam Sclerotherapy 2006, Tegernsee, Germany. VASA Zeitschrift fur Gefasskrankheiten 2008;37 Suppl 71:1-29.
5) Breu FX, Guggenbichler S. European Consensus Meeting on Foam Sclerotherapy, April, 4-6, 2003, Tegernsee, Germany. Dermatol Surg 2004;30(5):709-17; discussion 17.
ouvrir dans Pubmed
6) Kern P, Ramelet AA, Wutschert R, Hayoz D. Compression after sclerotherapy for telangiectasias and reticular leg veins: a randomized controlled study. J Vascular Surg 2007;45(6):1212-6.
7) Guex J.-J. Les contre-indications de la sclérothérapie. J Maladies Vasculaires 2005; 30 (3): 144-149.
8) Ramelet AA, Parmentier L. Delayed Nicolau's Livedoid Dermatitis after Ultrasound-Guided Sclerotherapy. Dermatol Surg 2010;36(1):155-8.
ouvrir dans Pubmed
9) Ramelet AA, Perrin M, Kern P, Bounameaux H. Phlélobologie. Masson, 2005; 364-365.
10) Goldman PP, Guex JJ, Weiss R. Sclerotherapy, Treatment of Varicose and Telangiectatic leg Veins. Sunders Elsevier 2011; 144-147, 162, 163, 171-173, 190-191, 209-210.
11) Mantha S, Karp R, Raghavan V, Terrin N, Bauer KA, Zwicker Jl, Assessing the risk of venous thromboembolic events in women taking progestin-only contraception : a meta-analysis. BMJ 2012 Aug 7;345.
ouvrir dans Pubmed
12) U S. Medical Eligibility Criteria for Contraceptive Use, MMWR Recomm Rep Centers Centers for Disease Control and Prevention (CDC) 2010 jun 18;59 (RR-4): 1-86.
13) Cochrane. Dépistage de la thrombophilie pour la prévention de la récidive de thromboembolie veineuse.2012 http://www.cochrane.org/fr/CD007069/depistage-de-la-trhombophilie-pour-l...
14) Demers C. Les thrombophilies, comment s'y retrouver. Le médecin du Quebec 2007; 42 (12): 61-67.
15) Schulman S, Svenungsson E, Granqvist S. Anticardiolipin antibodies predict early recurrence of thromboembolism and death among patients with venous thromboembolism following anticoagulant therapy. Am J Med 1998 ; 104 (4) : 332-8.
ouvrir dans Pubmed
16) Granel B, Morange P-E, Serratrice J, Ene N, Cremades S, Swiaer L, et al. Mutation G20210 A du gêne de la prothrombine à l'état hétérozygote et pathologies associées . La revue de médecine interne 2003; 24 (5) : 282-287.
ouvrir dans Pubmed
17) http://www.labtestonlin.fr/tests/FactorVLeiden.htlm?mode=print "facteur V Leiden et Mutation G20210A du gêne de la prothrombine.
18) Callum P, Bowles L, Keeling D. Diagnosis and management of heritable thrombophilias. BMJ 2014; 349:4387.
19) HAS Haute Autorité de Santé. Test de résistance à la protéine C activée, Recherche de la mutation du facteur V Leiden, recherche de la mutation G.20210GA de l prothrombine. Sept 2006. Service évaluation des actes professionnels. http://has-sante.fr
20) Mean M, Angelillo-Scherrer A. Thrombophilie : investiguer ou ne pas investiguer? Rev Med Suisse 2011; 294: 1025-1027
21) genetests.org
22) orphanet
23) Hamel-Desnos C, Moraglia L, Ramelet AA. Sclérothérapie. In: Guilmot JL, Hamel-Desnos C, editors. La Maladie veineuse Chronique. Issy les Moulineaux: Elsevier Masson; 2015:89-126.
24) Rabe E, Breu F, Cavezzi A, Smith PC, Frullini A, Gillet J, et al. European guidelines for sclerotherapy in chronic venous disorders. Phlebology / Venous Forum of the Royal Society of Medicine 2014;29(6):338-54.
ouvrir dans Pubmed
25) Goldman MP, Weiss RA, Guex JJ. Sclérotherapy, treatment of varicose and telangiectatic Leg Veins. 2011, fifth edition.
26) Feid CF. Deep venous thrombosis : the risk of sclérotherapy in hypercoagulable states. Semin dermatol 1993; 12:135-49.
ouvrir dans Pubmed
27) Stevenson JM, Seddon JA, Parry EW. The occurrence of deep venous thrombosis following compression sclerotherapy. Angiology 1976;27: 311.
28) Williams RA, Wilson SE. Sclerosant treatment of varicose veins and deep vein thrombosis. Arch Surg 1984 ; 119:1183.
29) Benhamou AC, Natali J. Les accidents des traitements sclérosant et chirurgical des varices des membres inférieurs. A propos de 90 cas. Phlébologie 1981; 1:41-51.
ouvrir dans Pubmed
30) Conrad P, Malouf GM, Stacey MC. The Australian Polidocanol (Aethoxysclerol®) study. Results at 2 years. Dermatol Surg 1995; 21:334-6.
31) James MP, Grech H. Subclinical, primary antiphospholipid syndrome unmasked by sclerotherapy. Br J Dermatol 2002 ;146:527-528.
32) ABSYM : Association Belge des Syndicats Médicaux.
33) Hamel-Desnos C, Desnos P, Guias B. Sclérothérapie mousse et thrombophilie. Phlébologie 2005;58( 4): 327-337.
34) http://www.adrreports.eu/fr/index.htlm
35) Thiollet M, Lajou J. Thrombose veineuse profonde, sclérose et thrombophilie : à propos de deux observations. Angio-Pratique Act Med Int Angiologie 1998 ; 242 : 4854-4856.
36) Azoulay J-P, Franchiti D. Sellier, Vin F. Accidents thrombo-emboliques au décours de la sclérothérapie. Thrombophilie et sclérothérapie. Phlébologie 2000 ; 53 : 442-468.
37) Hamel-Desnos C, Ouvry P, Desnos P, Escalard JM, Allaert FA. Sclérothérapie et thrombophilie : démarche pour un consensus dans la sclérothérapie chez les thrombophiles. Phlébologie 2003; 56:165-9.
38) Hamel-Desnos CM, Gillet J-L, Desnos PR, Allaert FA. Sclérotherapy of varicose veins in patients with documented thrombophilia : a prospective controlled randomized study of 105 cases. Phlebology 2009; 24:176-182.
ouvrir dans Pubmed