Présentation du cas
Un patient de 23 ans se présente aux urgences pour altération de l’état général, avec confusion, nausées, diarrhées et troubles de la marche en aggravation depuis 2 semaines. A noter que le patient est connu pour des troubles sensitivo-moteurs des membres inférieurs séquellaires d’une polyneuropathie sensitivo-motrice axonale d’apparition subaiguë en 2021, attribuée à un syndrome de Guillain-Barré et traitée par immunoglobulines intraveineuses sans amélioration significative. Depuis lors, le patient marche habituellement avec l’aide d’une béquille, mais la marche est devenue impossible au moment de l’admission. Comme autre antécédent notable, nous retenons un bypass gastrique en 2021, ayant entraîné une perte de poids de 60 kg. Il n’est pas compliant quant à la prise des suppléments vitaminiques. Récemment il s’est présenté aux urgences pour une brûlure au second degré à la face interne droite de la cuisse. A l’hétéro-anamnèse, la mère du patient rapporte une consommation récréative de protoxyde d’azote ( N2O) par le patient depuis 2018, progressivement intensifiée avec inhalation quasi continue dans les 3 semaines avant l’admission.
À l’admission, l’examen clinique révèle des troubles sensitifs des quatre membres, prédominant sur la sensibilité profonde et un syndrome tétrapyramidal, évoquant un tableau de dégénérescence combinée de la moelle. Les résultats des analyses sanguines effectuées aux urgences montrent une légère carence en vitamine B12 (172 pg/mL, intervalle de référence : 191-663 pg/mL), un taux d’homocystéine très élevé (219,32 μmol/L, intervalle de référence 5,00 - 15,00 μmol/L), un dosage d’acide méthylmalonique (AMM) urinaire élevée (91,0 mmol/mol de créatinine, intervalle de référence : < 20,0 mmol/mol de créatinine) ainsi qu’une légère anémie normocytaire (hémoglobine à 11,0 g/dL ; volume globulaire moyen (VGM) à 91fL). Dans ce contexte, le patient est hospitalisé pour bilan complémentaire. L’imagerie par résonance magnétique nucléaire ne montre aucune lésion significative au niveau cérébral ou médullaire. L’électroneuromyographie révèle une polyneuropathie périphérique sensitivo-motrice à prédominance axonale et sévère. Les potentiels évoqués visuels sont normaux. Au vu de la haute suspicion d’une myéloneuropathie au protoxyde d’azote, une supplémentation en vitamine B12 à haute dose a été administrée, ainsi qu’une supplémentation en vitamine B1 et acide folique. Le patient a également bénéficié d’une kinésithérapie de rééducation neurologique et un soutien psychothérapeutique. Son état s’est partiellement amélioré en cours d’hospitalisation.
N2O et risques associés à une surconsommation
Le N2O est un gaz utilisé comme anesthésique et analgésique dans le domaine médical, mais aussi en tant que gaz propulseur pour la préparation de crème chantilly. Il est également de plus en plus utilisé à des fins récréatives en raison de ses effets psychotropes, de son faible coût et de sa disponibilité (1). Cet usage détourné a entraîné l’apparition de conditionnements de plus en plus grands sur le marché mettant en avance la problématique de cette utilisation excessive (Image 1). Le protoxyde d’azote n’est pas classé sur la liste des stupéfiants en Belgique, ni même en Europe. Cependant, l’utilisation et la possession de ce gaz à des fins récréatives sont interdites dans les 19 communes de Bruxelles depuis avril 2020, et la vente aux mineurs n’est plus autorisée en Belgique depuis février 2022.

Malgré cette évolution de la législation, la consommation récréative de N2O a connu une forte augmentation ces dernières années. Celle-ci touche principalement les individus dans le début de la vingtaine, mais s’étend à toute la population (2). Effectivement, 3,2% des élèves de l’enseignement secondaire supérieur de la fédération Wallonie Bruxelles ont déclaré avoir déjà consommé ce gaz (3). Les effets recherchés sont une sensation d’euphorie, de désinhibition, ainsi que des symptômes de type dissociation et désorientation, voire des hallucinations. En cas d’intoxication aiguë, le tableau clinique associe notamment des céphalées, des nausées et vomissements, des diarrhées, des crampes abdominales, de la somnolence ainsi que des acouphènes (1, 4). Des brûlures par le froid au niveau de la cuisse, ainsi qu’au niveau des mains et des lèvres, de la bouche et des voies aériennes supérieures liées à l’utilisation des bonbonnes ont été rapportées. Afin d’éviter ces brûlures, les utilisateurs inhalent le gaz indirectement en remplissant des ballons, ce qui permet de le réchauffer (4-6). Des cas d’asphyxie entraînant une hypoxie létale ont également été décrits (7). Une accoutumance est souvent observée, ce qui peut renforcer la consommation et conduire à divers problèmes de santé majeurs. A moyen et long terme, il a été établi qu’une consommation régulière de N2O peut entraîner des symptômes neurologiques sensitivo-moteurs, pouvant être d’origine périphérique (polyneuropathie) et/ou centrale (sclérose combinée de la moelle épinière). Des symptômes thrombotiques ont également été observés (4, 8, 9). Ces symptômes sont expliqués par l’inactivation fonctionnelle de la vitamine B12 par le N2O.
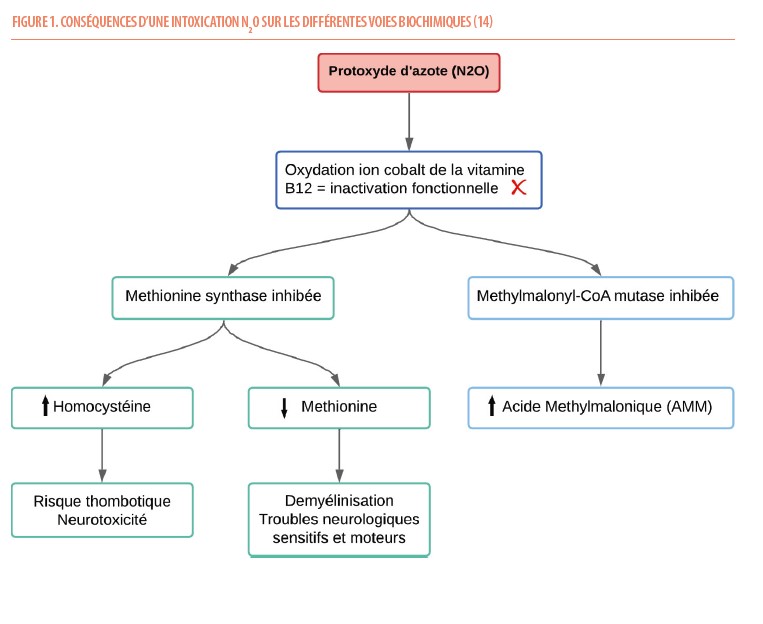
La vitamine B12, également connue sous le nom de cobalamine, est une vitamine essentielle au bon fonctionnement d’une série de processus physiologiques, notamment la synthèse de la myéline (10). Lorsque la vitamine B12 est présente en quantité suffisante dans l’organisme, elle agit comme cofacteur de la méthionine synthase qui convertit l’homocystéine en méthionine. Le N2O, en oxydant l’ion cobalt de la vitamine B12, va inhiber l’action de ce cofacteur, entraînant une inactivation fonctionnelle. En cas de carence ou d’inactivation fonctionnelle en vitamine B12, la conversion de l’homocystéine en méthionine est compromise (8, 11). Par conséquent, les niveaux d’homocystéine plasmatiques augmentent et ceux de méthionine diminuent (10). La méthionine jouant un rôle dans la synthèse de la myéline, sa diminution expliquerait les symptômes neurologiques sensitifs et moteurs observés chez les consommateurs de N2O (10, 12). Cependant, une étude récente, a montré qu’il n’existait pas de déficit quantitatif en méthionine plasmatique chez les consommateurs de N2O avec gravité clinique importante, d’autres mécanismes physiopathologiques sont donc à rechercher (13).
La vitamine B12 joue également un rôle en tant que cofacteur dans un autre processus métabolique : la synthèse de succinyl-CoA. En temps normal, l’enzyme méthylmalonyl-CoA mutase requiert la présence de la vitamine B12 pour convertir par isomérisation le méthylmalonyl-CoA en succinyl-CoA(1, 11). Le méthylmalonyl-CoA est un métabolite intermédiaire intracellulaire issu de la dégradation de certains acides aminés. En cas d’inactivation fonctionnelle de la vitamine B12 par le N2O, celui-ci s’accumule et les concentrations de son dérivé extracellulaire, l’AMM, s’élève dans les fluides biologiques (Figure 1). Actuellement, l’impact clinique de l’augmentation de l’AMM lié à une consommation de N2O reste inconnu.
Diagnostic et dosages sanguins
En raison de la courte demi-vie du N2O dans l’organisme, son dosage sanguin pour mettre en évidence une consommation s’avère inutile. Vu qu’il s’agit d’une inactivation fonctionnelle et non d’une réelle carence mais aussi que certains consommateurs se supplémentent eux même en vitamine B12, les taux de vitamine B12 peuvent rester normaux en cas de consommation de N2O. Le dosage de marqueurs fonctionnels comme l’homocystéine a donc toute son importance, son augmentation étant actuellement le meilleur marqueur d’une consommation de N2O récente (10).
L’AMM constitue un autre marqueur biochimique pour évaluer le fonctionnement du métabolisme de la vitamine B12. Ce dosage plasmatique est utile pour confirmer que la sévérité clinique est lié à une inactivation de la voie des cobalamines et d’avancer l’hypothèse étiologique d’intoxication au N2O (1, 10, 14). Malheureusement, son augmentation en cas de consommation de N2O n’est pas systématique et est surtout retrouvée chez des patients avec atteintes cliniques importantes (10, 14). Ce dosage plasmatique est malheureusement peu disponible pour le moment, cependant selon une étude récente, il est possible de réaliser le ratio plasmatique homocystéine/méthionine qui est comme l’AMM témoin d’une sévérité clinique importante (13). Un dosage d’AMM urinaire existe également et est généralement plus disponible que l’AMM plasmatique pour évaluer le statut vitaminique B12 mais celui-ci est moins sensible et est surtout préconisé lors d’une suspicion de maladie héréditaire du métabolisme (15).
Discussion
Nous avons documenté le cas d’un patient présentant une myéloneuropathie liée à la consommation abusive de N2O. L’inactivation fonctionnelle en vitamine B12 induite par le N2O et la carence en vitamine B12 pourraient être responsables de la symptomatologie observée à l’admission. La carence en vitamine B12 peut être expliquée par la mauvaise compliance du patient vis-à-vis des suppléments vitaminiques prescrits après le bypass gastrique. Une carence en vitamine B12 peut également entraîner une augmentation modérée de l’homocystéine et provoquer des symptômes neurologiques similaires (10).
Par ailleurs, le diagnostic de syndrome de Guillain-Barré posé en 2021 pourrait être remis en question au vu du contexte de consommation de N2O (1, 9), d’autant plus de l’absence de dissociation albumino-cytologique à la ponction lombaire et d’un taux d’homocystéine déjà élevé (41,8 µmol/L, intervalle de référence < 15 µmol/L). La vitamine B12 était alors normale (443 pg/mL, intervalle de référence : 197-771 pg/mL). Le traitement par immunoglobulines intraveineuse n’avait d’ailleurs pas apporté d’amélioration clinique. Ces éléments suggèrent que la consommation excessive de N2O a joué un rôle majeur dans la symptomatologie du patient, tant en 2021 qu’actuellement. Le dosage de l’AMM plasmatique pour confirmer l’étiologie n’a pas pu être effectué chez ce patient. Le dosage urinaire, bien que moins sensible, s’est révélé positif chez ce patient appuyant l’hypothèse étiologique de l’intoxication au N2O. En outre, la brûlure rapportée dans ses antécédents médicaux est un argument en faveur d’une consommation antérieure de N2O.
Ce cas illustre l’importance de considérer la consommation de N2O dans le diagnostic différentiel des patients présentant un tableau de neuropathie périphérique ou de myélopathie, surtout chez un sujet jeune. Il est essentiel de sensibiliser les professionnels de la santé à la problématique de la consommation de N2O et d’intégrer cette question à l’anamnèse des patients présentant des troubles sensitivo-moteurs d’apparition subaiguë (1, 9). Un dépistage précoce et une prise en charge adéquate de l’inactivation fonctionnelle en vitamine B12 peuvent contribuer à améliorer les résultats cliniques et à prévenir les complications à long terme chez ces patients.
Conclusion
Nous avons documenté le cas d’un patient présentant une neurotoxicité liée à l’utilisation du N2O. L’inhalation prolongée de ce gaz peut entraîner une altération de la fonction de la vitamine B12, qui est un cofacteur essentiel à divers processus physiologiques au niveau du système nerveux. Actuellement, l’élévation de l’homocystéine plasmatique constitue le meilleur marqueur biochimique disponible en laboratoire pour orienter vers le diagnostic d’intoxication au N2O. Il convient de souligner qu’il existe souvent une idée erronée selon laquelle le dosage de la vitamine B12 peut permettre de diagnostiquer une intoxication au N2O, alors que les niveaux de cette vitamine peuvent se révéler normaux dans de tels cas. Enfin, le dosage de l’AMM plasmatique peut être effectué en laboratoire afin d’orienter le diagnostic. Un dosage d’AMM urinaire, plus fréquemment disponible en laboratoire (via l’analyse des acides organiques urinaires) peut également s’avérer utile mais est moins sensible. Il est important de noter que cette intoxication doit être considérée dans le diagnostic différentiel d’une polyneuropathie ou d’une myélopathie dans les populations les plus à risque, afin de fournir une prise en charge adaptée et un suivi adéquat.
Recommandations pratiques
Devant un tableau de neuropathie périphérique ou médullaire, nous recommandons d’interroger le patient sur une possible consommation de N2O. Afin d’orienter le diagnostic, nous proposons d’effectuer des dosages plasmatiques d’homocystéine et d’acide méthylmalonique.
Conflits d’intérêts Les auteurs ne déclarent aucun conflit d’intérêt.
Affiliations
1. Service de Biochimie Médicale, Laboratoire des Cliniques universitaires Saint-Luc, Bruxelles, Belgique
2. Service de Neurologie, Cliniques universitaires Saint-Luc, Bruxelles, Belgique
3. Service d’hormonologie, métabolisme, nutrition, oncologie, CHU de Lille, 59000 Lille, France
Correspondance
Dr Lidvine Boland
Cliniques universitaires Saint-Luc et UCLouvain
Service de Biochimie Médicale
10 Avenue Hippocrate
B-1200 Brussels, Belgium
lidvine.boland@saintluc.uclouvain.be
Références
- Qin X, Kang L, Liu X, Jin J, Hu F, Lu W, et al. Acute nitrous oxide-induced neuropathy mimicking Guillain-Barré syndrome. J Peripher Nerv Syst. 2022;27(3):189-96. Epub 20220607. doi: 10.1111/jns.12503. PubMed PMID: 35611446.
- Xiang Y, Li L, Ma X, Li S, Xue Y, Yan P, et al. Recreational Nitrous Oxide Abuse: Prevalence, Neurotoxicity, and Treatment. Neurotox Res. 2021;39(3):975-85. Epub 20210326. doi: 10.1007/s12640-021-00352-y. PubMed PMID: 33770366.
- Dujeu M. PC, Lebacq T., Desnouck V., Moreau N., Holmberg E., Castetbon K. Consommations de tabac, alcool, cannabis et autres produits illicites. Comportements, santé et bien-être des élèves en 2018 – Enquête HBSC en Belgique francophone. Service d’Information, Promotion, Éducation Santé (SIPES), École de Santé Publique, Université libre de Bruxelles). 2020.
- Randhawa G, Bodenham A. The increasing recreational use of nitrous oxide: history revisited. Br J Anaesth. 2016;116(3):321-4. Epub 20150830. doi: 10.1093/bja/aev297. PubMed PMID: 26323292.
- Chen JHC, Eriksson S, Mohamed H, Bhatti S, Frew Q, Barnes D. Experiences of frostbite injury from recreational use of nitrous oxide canisters in a UK burns center: not a laughing matter. J Plastic, Reconstructive Aesthetic Surg. 2023;83:282-8.
- Chan SA, Alfonso KP, Comer BT. Upper aerodigestive tract frostbite from inhalation of automotive nitrous oxide. Ear Nose Throat J. 2018;97(9):E13-e4. doi: 10.1177/014556131809700903. PubMed PMID: 30273435.
- Wagner SA, Clark MA, Wesche DL, Doedens DJ, Lloyd AW. Asphyxial deaths from the recreational use of nitrous oxide. J Forensic Sci. 1992;37(4):1008-15. PubMed PMID: 1506823.
- Marotta DA, Kesserwani H. Nitrous Oxide Induced Posterior Cord Myelopathy: Beware of the Methyl Folate Trap. Cureus. 2020;12(7):e9319. Epub 20200721. doi: 10.7759/cureus.9319. PubMed PMID: 32850197; PubMed Central PMCID: PMC7444745.
- Beal JC, Cheng Y, Merchant S, Zarnegar R. An Acute, Severe Axonal Sensorimotor Polyneuropathy in the Setting of Nitrous Oxide Abuse. Neurohospitalist. 2020;10(4):293-6. Epub 20200309. doi: 10.1177/1941874420910648. PubMed PMID: 32983349; PubMed Central PMCID: PMC7495705.
- Grzych G, Deheul S, Gernez E, Davion JB, Dobbelaere D, Carton L, et al. Comparison of biomarker for diagnosis of nitrous oxide abuse: challenge of cobalamin metabolic parameters, a retrospective study. J Neurol. 2023;270(4):2237-45. Epub 20230124. doi: 10.1007/s00415-023-11570-z. PubMed PMID: 36690804.
- Joncquel Chevalier-Curt M, Grzych G, Tard C, Lannoy J, Deheul S, Hanafi R, et al. Nitrous oxide abuse in the emergency practice, and Review of toxicity mechanisms and potential markers. Food Chem Toxicol. 2022;162:112894. Epub 20220225. doi: 10.1016/j.fct.2022.112894. PubMed PMID: 35219765.
- Chanarin I. The effects of nitrous oxide on cobalamins, folates, and on related events. Crit Rev Toxicol. 1982;10(3):179-213. doi: 10.3109/10408448209037455. PubMed PMID: 6127188.
- Gernez E, Deheul S, Tard C, Joncquel M, Douillard C, Grzych G. Plasma Methionine and Clinical Severity in Nitrous Oxide Consumption. Toxics. 2022;11(1). Epub 20221223. doi: 10.3390/toxics11010012. PubMed PMID: 36668738; PubMed Central PMCID: PMC9866764.
- Grzych G, Gernez E, Deheul S, Kim I. [Methylmalonic acid: Specific marker of chronic nitrous oxide abuse?]. Rev Med Interne. 2022;43(3):197-8. Epub 20220127. doi: 10.1016/j.revmed.2022.01.001. PubMed PMID: 35094872.
- Obeid R, Geisel J, Herrmann W. Comparison of two methods for measuring methylmalonic acid as a marker for vitamin B12 deficiency. Diagnosis (Berl). 2015;2(1):67-72. doi: 10.1515/dx-2014-0030. PubMed PMID: 29540015.