NOUVEAUTÉS PHARMACOLOGIQUES DANS LE DOMAINE DE LA RYTHMOLOGIE
A. Le Praxbind©
C’est le nom commercial donné à l’idarucizumab. Il s’agit de fragments d’anticorps monoclonaux humanisés et administrés chez le patient pour contrecarrer les effets du Pradaxa© (dabigatran), et ce sans augmentation en retour du risque thrombotique. Les deux molécules sont issues des travaux de recherche de Boehringer Ingelheim. Pour rappel, le Pradaxa© est un anticoagulant oral, inhibiteur direct de la thrombine et donné en prévention des complications thromboemboliques de la FA, dans la thrombose veineuse profonde (prévention et traitement) et dans l’embolie pulmonaire. Le Praxbind© se présente dans des flacons de 50ml, qui contiennent 2.5g d’anticorps. Les deux principales indications de l’antidote sont :
• le contrôle urgent de saignements menaçant le pronostic vital de la victime ;
• le contrôle de la coagulation en vue d’une procédure invasive urgente (chirurgicale ou autre) qui peut s’accompagner d’un saignement.
La dose à administrer en intraveineux est de 5g. Une deuxième dose est à envisager en cas de persistance du saignement ou en cas de deuxième intervention chirurgicale. L’agent neutralisant du Pradaxa© est remboursé en Belgique depuis le 1er septembre 2016. B.
Le Brinavess©
Il s’agit du Vernakalant. Cette molécule a des propriétés antiarythmiques ciblant les oreillettes (allongement de la période réfractaire des cellules atriales). Elle n’est toutefois qu’utile dans la conversion RAPIDE de fibrillations auriculaires (FA) (pas le flutter atrial !) soutenues et récentes datant de moins de 7 jours. Le médicament se présente dans des flacons à diluer de 10ml (200mg), et 25ml (500mg). Il s’administre en intraveineux, sous monitoring continu dans une structure médicale adaptée. La dose recommandée lors de la première perfusion de 15 minutes à la pompe est de 3mg/kg. La dose maximale si le patient pèse plus de 113 kilos est de 339mg. Si au terme de cette première perfusion le patient reste en FA, une deuxième perfusion de max 2mg/Kg peut être administrée (en 10 minutes). La dose maximale si le patient pèse plus de 113 kilos est de 226mg. À noter qu’aucune adaptation de dose n’est nécessaire en cas d’insuffisance rénale ou hépatique. Ses principales contre-indications sont :
• <18 ans.
• La sténose aortique serrée.
• QT/QTc long.
• Une hypotension artérielle (<100mmHg).
• Une insuffisance cardiaque (NYHA classe III-IV).
• Une bradycardie, des troubles de la conduction auriculo-ventriculaire.
• L’administration d’autres antiarythmiques dans les 4 heures qui précèdent
LES NOUVELLES RECOMMANDATIONS EUROPÉENNES
Nous résumons ci-dessous les messages essentiels des quatre recommandations publiées cette année par la société européenne de cardiologie.
A. Prise en charge des dyslipidémies (1)
Le risque cardiovasculaire (CVD) d’un patient est fonction de l’ensemble de ses facteurs de risques. Les patients avec une maladie cardiovasculaire avérée, présentant un diabète, une insuffisance rénale chronique et d’autres facteurs de risque individuels sont considérés comme ayant un risque cardiovasculaire élevé (c’est-à-dire un risque estimé à 10 ans de décès cardiovasculaire > 10%) Pour toutes les autres personnes, l’utilisation du système SCORE est proposée pour l’évaluation du risque cardiovasculaire.
1. Dosage de lipides
Le calcul du risque cardiovasculaire à l’aide des tables SCORE se base principalement sur le dosage du cholestérol total, néanmoins le dosage du LDL-cholestérol est l’analyse de choix pour le dépistage, de diagnostic et le suivi des patients avec une dyslipidémie. Les triglycérides (TG) ajoutent des informations sur le risque et sont utiles pour le diagnostic et le choix du traitement. Le taux de Cholestérol non-HDL est un facteur de risque indépendant et doit être considéré comme un marqueur de risque, en particulier chez les patients avec un taux de TG élevé.
2. Traitement des dyslipidémies en fonction du risque cardiovasculaire
La première étape dans la prise en charge des dyslipidémies passe par des modifications du style de vie (alimentation, activité physique, arrêt du tabagisme). L’initiation du traitement médicamenteux dépend à la fois du taux de LDL cholestérol et des facteurs de risque cardiovasculaire du patient : chez un patient avec un score de risque <1, le traitement sera proposé si le taux de LDL cholestérol est > 190 mg/dl par contre, il sera proposé dès 100 mg/dl si le score de risque est <5.
En outre, le taux cible de LDL cholestérol dépend du risque cardiovasculaire global :
- chez les patients présentant un risque CV très élevé, l’objectif est de viser un taux de LDL cholestérol <70mg/dl ou une réduction d’au moins 50% si le LDL cholestérol initial est compris entre 70 et 135mg ;
- chez les patients présentant un risque CV élevé, un objectif sera d’obtenir un taux de LDL cholestérol < 100mg/dl ou une réduction d’au moins 50% si le LDL cholestérol initial est compris entre 100 et 200 mg/dl ;
- chez les sujets à risque faible ou modéré, un objectif sera d’obtenir LDL-C <115mg/dl.
3. Traitement pharmacologique
Les statines restent le traitement de référence mais, vu la variabilité de la réponse, une titration sera souvent utile. Si la dose de statine la plus élevée tolérée n’atteint pas l’objectif, une association médicamenteuse avec l’ézétimibe ou un inhibiteur de l’absorption du cholestérol doit être envisagée. Chez les patients à risque très élevé, avec des taux de LDL cholestérol restant élevés en dépit d’un traitement avec la dose maximale tolérée (ou avec l’intolérance aux statines) et en combinaison avec l’ézétimibe, un inhibiteur de PCSK9 peut être considéré.
Chez les patients à haut risque avec triglycérides > 200 mg/dl, malgré le traitement par statine, le fénofibrate peut être ajouté en association avec des statines.
Les statines ne sont pas recommandées chez les patients en insuffisance rénale chronique ou dialysés sans atteinte cardiovasculaire ou chez les patients avec une sténose aortique ou avec une insuffisance cardiaque non ischémique en l’absence d’indication spécifique pour leur utilisation.
Les lipides et les enzymes hépatiques / musculaires doivent être surveillés 8 (± 4) semaines après le début du traitement avec ajustement du traitement jusqu’à atteindre la plage cible. En cas d’élévation importante des enzymes hépatiques (≥ 3x limite supérieure de la normale) ou des enzymes musculaires (CK) (≥ 4x limite supérieure de la normale), le traitement doit être arrêté. Un essai prudent de réintroduction à plus faible dose peut être proposée après normalisation des enzymes et sous contrôle biologique.
4. L’hypercholestérolémie familiale (FH)
FH est sera suspecté chez les patients présentant un maladie coronaire avant l’âge de 55 ans pour les hommes et de 60 ans pour les femmes, chez les sujets ayant des parents atteints de maladie cardiovasculaire prématurée, chez les sujets ayant des parents porteurs de xanthomes tendineux et chez les sujets avec un taux de LDL cholestérol > 190mg/dl pour un adulte et > 140mg/dl pour un enfant. Leur traitement nécessite l’association de statine à forte doses d’ézétimide et souvent d’un inhibiteur de PCSK9 si le LDL Cholestérol cible n’est pas atteint avec la dose maximale tolérée de statine et d’ézétimibe
B. Prise en charge de la fibrillation auriculaire
Les points suivants sont mis en évidence par les nouvelles recommandations (2) concernant la prise en charge de la fibrillation auriculaire (FA).
1. Une FA paroxystique « silencieuse » est diagnostiquée chez un nombre croissant de personnes présentant un accident vasculaire cérébral (AVC). Un dépistage occasionnel de la FA par la prise du pouls ou un enregistrement ECG est recommandé chez les patients de plus de 65 ans (classe I, niveau d’évidence B). Un dépistage systématique de l’ECG peut être envisagé pour détecter la FA chez les patients de plus de 75 ans ou ceux à haut risque d’AVC (classe IIB, niveau d’évidence B). Des épisodes de fibrillation auriculaires doivent être recherchés lors de l’interrogation des pace maker et des défibrillateurs implantés. Il est nécessaire de documenter un épisode de FA d’au moins 30 secondes pour initier un traitement.
2. Chez les patients obèses présentant de la FA, la perte de poids associée à la prise en charge d’autres facteurs de risque devraient être envisagés (Classe IIa, niveau d’évidence B). Une perte de poids de 10-15kg avec prise en charge des autres facteurs de risque, entraine une réduction des épisodes de FA et des symptômes liées à la FA. Un syndrome d‘apnée du sommeil doit être recherché chez ces patients (classe IIa, niveau d’évidence B). Le traitement du syndrome des apnées du sommeil permet de réduire les récidives de FA et d’améliorer l’efficacité du traitement de FA (classe IIa, niveau d’évidence B).
3. Une anticoagulation orale doit être envisagée chez les tous patients dont le score CHA2DS2-VASc est de 1 pour les hommes et de 2 pour les femmes (classe IIa, niveau d’évidence B). Chez un patient, en FA, en l’absence de contre-indications, l’utilisation des NOACs (apixaban, dabigatran, edoxaban ou rivaroxaban) est recommandées plutôt que celle des antagonistes de la vitamine K (classe I, niveau d’évidence A). Les NOACs ne doivent pas être utilisés chez les patients porteurs d’un valve mécanique (classe III, niveau d’évidence B) ou sténose mitrale modérée à sévère (classe III, niveau d’évidence C). Les patients avec un flutter doivent être anticoagulés comme les patients en FA.
4. L’anticoagulation pour la prévention de l’AVC doit être poursuivie après une ablation même réussie (chirurgicale ou par cathétérisme) chez les patients présentant un risque élevé d’AVC (classe IIa, niveau d’évidence C). Après l’occlusion chirurgicale ou l’exclusion de l’auricule gauche, il est recommandé de poursuivre l’anticoagulation chez les patients à risque de FA pour la prévention de l’AVC (classe I, niveau d’évidence B).
5. Une anticoagulation avec de l’héparine ou de l’héparine de bas poids moléculaire immédiatement après un AVC ischémique n’est pas recommandée chez les patients en FA (classe III). Chez les patients présentant un AVC ischémique modéré à important alors qu’ils sont anticoagulés, l’anticoagulation doit être interrompue entre 3 et 12 jours en fonction d’une évaluation multidisciplinaire des risques liés à l’AVC et de saignement (classe IIa, niveau d’évidence C).
6. Chez les patients en FA à risque d’AVC, lors de l’implantation d’une endoprothèse coronaire (stent) dans le cadre d‘un syndrome coronarien aigu, une triple anticoagulation (aspirine, clopidogrel et anticoagulant oral) doit être instaurée pour une durée de 1 à 6 mois en prévention des récidive d’accidents ischémiques coronaires et cérébraux. (Classe IIa, niveau d’évidence C). La durée de la thérapie de la triple thérapie sera adaptée en fonction des risques de saignement et de récidive. (Classe IIa, niveau d’évidence B).
7. La dronédarone, la flecainide, la propafénone ou le sotalol sont recommandés pour la prévention des récidives de FA symptomatique chez les patients présentant une fonction ventriculaire gauche normale et sans hypertrophie ventriculaire gauche (classe I, niveau d’évidence A). L’amiodarone est recommandée pour la prévention des récidives de FA symptomatique chez les patients atteints d’insuffisance cardiaque (classe I, niveau d’évidence B).
8. L’ablation par cathétérisme de la FA est recommandée chez les patients qui présentent des récidives de FA symptomatique sous traitement anti arythmique (Classe I, niveau d’évidence A). L’ablation de la FA par cathétérisme doit être considérée en première intention pour prévenir la récidive de la FA chez certains patients présentant une FA paroxystique symptomatique comme alternative à la thérapie médicamenteuse antiarythmique. (Classe IIa, niveau d’évidence B). Une ablation par cathétérisme ou par chirurgie peut être proposée chez les patients symptomatiques présentant une FA permanente ne répondant pas ou mal au traitement antiarythmique afin d‘améliorer les symptômes en tenant compte des préférences du patient, des avantages et risques potentiels liés à la procédure (Classe IIa, niveau d’évidence C).
C. Prise en charge de l’insuffisance cardiaque
Les points suivants sont mis en évidence dans les nouvelles recommandations (3) sur le diagnostic et la prise en charge de l’insuffisance cardiaque.
1. Le diagnostic de l’insuffisance cardiaque repose sur cinq éléments clés : l’anamnèse, l’examen clinique, histoire du patient, le taux sérique de BNP ou NT-ProBNP et échocardiographie. Un taux sérique de BNP < 35 pg/mL ou de NT-proBNP < 125 pg/mL permet d’éliminer le diagnostic d’insuffisance cardiaque. À noter toutefois que ces deux biomarqueurs ont une valeur prédictive négative élevée, mais que leur valeur prédictive positive est faible. Aucun remboursement de ces deux tests n’existe en Belgique.
2. Nouvelle catégorie dans la classification de l’insuffisance cardiaque. Cette classification se base sur la fraction d’éjection mesurée par échocardiographie :
- Fraction éjection du ventricule gauche <40% : HFrEF, insuffisance cardiaque à fraction d’éjection réduite
- Fraction éjection du ventricule gauche entre 40 et 49% : HFmrEF, insuffisance cardiaque à fraction d’éjection modérément réduite.
- Fraction éjection du ventricule gauche ≥50% : HFpEF, insuffisance cardiaque à fraction d’éjection préservée
Actuellement, cette nouvelle catégorie est surtout théorique et n’a pas d’implication thérapeutique.
3. Importance des comorbidités. Les comorbidités peuvent compliquer le diagnostic de l’insuffisance cardiaque (par exemple la dyspnée chez les patients BPCO), aggraver les symptômes (cachexie), ou leur traitement peuvent aggraver l’insuffisance cardiaque (par exemple les anti-inflammatoires non stéroïdiens (AINS)). Les comorbidités suivantes doivent rester à l’esprit du médecin : maladie coronaire, diabète, cachexie, néoplasie, atteinte système nerveux central (AVC, dépression, atteinte autonomique), dysfonction érectile, gouttes arthrite, hyper ou hypokaliémie dyslipidémie, hypertension artérielle, carence en fer et anémie, atteinte pulmonaire (asthme, BPCO), obésité, trouble du sommeil (apnées...), atteinte valvulaire. Le cas échéant, elles seront traitées de façon agressive.
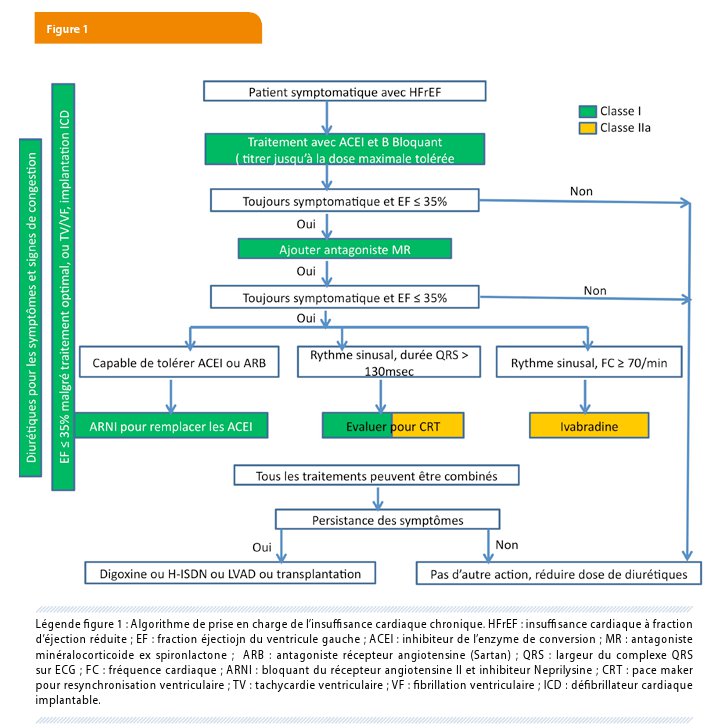
4. Traitement chronique : proposition d’un algorithme pratique pour la prise en charge des patients (Figure 1). Apparition dans le traitement chronique de l’inhibiteur de l’angiotensine / inhibiteur de la néprilysine (ARNI) sacubitril / valsartan et ivabradine comme nouveaux composants importants dans le traitement des patients avec HFrEF. L’ivabradine est recommandée chez les patients qui restent symptomatiques en dépit d’une thérapie adaptée, y compris le titrage à un dosage bêta-bloquant maximum et avec une fréquence cardiaque persistante d’au moins 70 battements / min. La resynchronisation ventriculaire par pacing peut être envisagée chez certains patients avec un QRS > 130 msec.
D. Recommandations concernant la prévention cardiovasculaire
Ces nouvelles recommandations (4) proposent une action au niveau individuel pour réduire le risque cardiovasculaire mais insistent également sur des mesures de santé publique : arrêt du tabac (et de son exposition), pratique régulière du sport et ceci dès l’enfance, diminution de la consommation des boissons alcoolisées... Les restrictions sur les cigarettes électroniques sont mentionnées en raison de l’incertitude quant son innocuité. Elles insistent sur le rôle important des professionnels de la santé non seulement en tant que promoteurs de cette approche mais aussi en tant qu’exemple.
Outre les facteurs de risques classiques utilisés pour le calcul du risque cardiovasculaire (table Score), d’autres facteurs de risques pourraient également jouer un rôle dans l’évaluation du risque de maladie cardiovasculaire : le statut socio-économique, l’isolement social ou le manque de soutien social; les antécédents familiaux de maladie cardiovasculaire prématurée; l’indice de masse corporelle et l'obésité centrale; le score calcique coronaire en tomodensitométrie; la présence de plaques athéromateuse au niveau des carotides, l’indice de tension artérielle bras cheville...
Les patients qui ont reçu un traitement anticancéreux par chimiothérapie ou radiothérapie ont un risque accru de maladie cardiovasculaire. Dans cette population, l’incidence accrue des maladies cardiovasculaires est corrélée avec les traitements donnés et la dose administrée (et leur combinaison). Par conséquent, les patients recevant une chimiothérapie de type I (induisant potentiellement des effets cardiotoxiques irréversibles), doivent être considérés comme à haut risque cardiovasculaire pour la prévention de la dysfonction ventriculaire gauche (Classe IIa, niveau d’évidence B). La polyarthrite rhumatoïde augmente le risque cardiovasculaire (X1.5) indépendamment des facteurs de risques traditionnels surtout si la maladie est très active (Classe IIa, niveau d’évidence B).
Enfin, ces recommandations mettent l’accent sur le risque cardiovasculaire dans certains groupes de populations comme les personnes jeunes ou les personnes âgées, les femmes et les minorités ethniques :
_ Certaines personnes jeunes doivent être traitées pour un facteur de risque unique si la tension artérielle dépasse 180/110 mmHg ou ont un taux de cholestérol > 8mmol/l. Une hypercholestérolémie familiale doit être recherchée chez toute personne qui a une histoire familiale de maladie cardiovasculaire à un âge jeune.
- Chez les personnes âgées, la gestion des risques cardiovasculaires reste controversée. Les recommandations sur le contrôle des facteurs de risque sont à mettre en balance avec le confort de vie et les effets indésirables.
- Des complications obstétricales comme la pré éclampsie et l’hypertension de grossesse sont associées avec un risque accru de complications cardiovasculaires au long terme dans la vie de la femme.
- Le risque de maladie cardiovasculaire varie considérablement entre les ethnies : les Sud-Asiatiques et les Africains sub-sahariens ont un risque plus élevé alors que les Chinois et les Sud-Américains ont un risque plus faible.
Les recommandations insistent également sur le contrôle des facteurs de risque dans différentes pathologies cardiovasculaires :
- Fibrillation auriculaire : l’hypertension artérielle chez les patients atteints de fibrillation auriculaire double le risque de complications cardiovasculaire et doit être traitée.
- Insuffisance cardiaque chronique : la prévention doit débuter le plus tôt possible et nécessite d’intégrer les différents aspects.
- Maladie coronarienne : les mesures de prévention cardiovasculaire sont cruciales pour les résultats à court et à long terme.
- La maladie cérébrovasculaire: la gestion du risque cardiovasculaire chez les patients avec un accident ischémique transitoire ou accident vasculaire cérébral ischémique est généralement comparable à celle chez les patients coronariens.
- L’atteinte des artères périphériques (PAD): celle-ci est souvent asymptomatique. Le traitement préventif est identique à celui de la maladie coronaire.
Affiliations
Université catholique de Louvain, IREC
Avenue Hippocrate 55 bte B1.55.02 B-1200 Bruxelles
Cliniques universitaires Saint Luc
Département de Pathologie cardiovasculaire
Cardiologie
avenue Hippocrate 10, B-1200 Bruxelles, Belgique.
Correspondance
Pr. Agnès Pasquet
agnes.pasquet@uclouvain.be
Références
- Alberico L. Catapano, Ian Graham et al. 2016 ESC Guidelines for the management of dyslipidaemia. Eur Heart J 2016; 37 (39): 2999-3058.
ouvrir dans Pubmed - Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016; 37 (38): 2893-2962.
ouvrir dans Pubmed - 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC, Eur Heart J (2016) 37 (27): 2129-2200MF Piepoli, AW Hoes, et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J 2016; 37: 2315–238.
ouvrir dans Pubmed