Introduction
Fin décembre 2019, plusieurs cas de pneumonies inexpliquées surviennent concomitamment dans la ville de Wuhan, dans la Province Chinoise du Hubei, 7e ville chinoise, peuplée de 11 millions d’habitants. Le cluster semble centré sur le South China Seafood Market, un vaste marché de fruits de mer et d’animaux vivants. Le 30 décembre, l’administration de Wuhan émet un premier avis d’alerte avec des recommandations concernant la prise en charge de cette infection. La première mention de cette épidémie hors de Chine date également du 30 décembre 2019, au travers d’un Post sur la lettre d’information ProMED-MAIL (1). L’étiologie en reste indéterminée, et la question d’une origine bactérienne (peste, legionellose), ou d’une infection virale (précédent SARS-CoV) est posée. Le lendemain, un symposium urgent est tenu dans plusieurs hôpitaux de la ville de Wuhan à propos du traitement de cette pneumonie, et le bureau régional de l’Organisation Mondiale de la Santé (OMS) est informé de 44 cas de pneumonies inexpliquées, dont 11 patients dans un état grave. Des analyses ultérieures démontreront que le virus circule déjà depuis plusieurs semaines. Le 1er janvier, le marché de Wuhan est fermé pour raisons sanitaires. Le virus sera identifié rapidement comme appartenant à la famille des Coronaviridae (2), apparenté au virus du syndrome respiratoire aigu sévère (SARS). Le virus sera plus tard baptisé severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2), tandis que la maladie qu’il engendre recevra le nom de COVID-19 pour Coronavirus disease 2019 (3).
Rapidement, l’infection se répand en Chine. Le 30 janvier, l’OMS déclare l’infection officiellement comme une urgence de santé publique de portée internationale. La maladie se répand rapidement hors de Chine, et le 25 février, pour la première fois, le nombre de nouveaux diagnostics hors de Chine excède le nombre de diagnostics en Chine. L’OMS déclare l’état de pandémie le 11 mars 2020. L’Europe est frappée de plein fouet, avec au premier rang des pays atteints l’Italie suivie par l’Espagne, la France, la Grande-Bretagne.
Épidémiologie et transmission
La maladie se caractérise par une transmission interhumaine élevée, avec un taux de reproduction (R0 dans l’absolu, ou Rt à un moment précis) élevé. Des valeurs de l’ordre de 2,2 à 3,3 sont généralement citées, mais des chiffres aussi haut que 3 à 4 ont été évoqués pour la phase ascendante de l’épidémie à la mi-janvier dans la région de Wuhan, ce qui signifie alors qu’une personne en infecte en moyenne trois à quatre (4). Ce taux de reproduction est dépendant des mesures de santé publiques prises pour diminuer la transmission du virus. Les mesures de distanciation sociale, par exemple, ont pour objectif d’amener le Rt en dessous de 1, niveau sous lequel une transmission soutenue du virus n’est plus possible (5). En l’absence de vaccin, ces mesures prises par de nombreux pays se sont avérées efficaces à ce stade pour freiner ou arrêter la propagation du virus de manière à ne pas saturer le système hospitalier surtout, bien qu’elles n’aient malheureusement pas in fine d’effet rémanent, faisant craindre une nouvelle flambée après leur levée (4).
Le mode de transmission du SARS-CoV-2 reste incomplètement compris. Bien qu’il soit vraisemblable que la dichotomie traditionnelle gouttelettes-aérosol soit une réduction un petit peu simpliste (6), il n’en reste pas moins que la voie principale de transmission interhumaine du SARS-CoV-2 se fasse via les plus grosses gouttelettes respiratoires (définies classiquement comme des particules de taille supérieures à 5 à 10 μm) qui sont émises et se répandent dans un périmètre restreint (environ 2 mètres) par les individus lorsqu’ils toussent, éternuent ou parlent. Les individus s’infectent soit par inhalation, soit par contact de ces gouttelettes avec les muqueuses (7). Il est possible que la transmission se fasse également dans une certaine mesure par voie aérienne (génération d’aérosols) (8) mais l’incertitude subsiste à ce sujet. Une attention particulière doit néanmoins être portée aux risques de contamination en lien avec les procédures à risque de générer une aérosolisation telles que l’aérosolthérapie, la ventilation artificielle (invasive ou non) ou l’oxygénothérapie notamment à débit élevé.
Le virus a également été retrouvé dans de nombreux autres échantillons (sang, selles, salive, urines, sécrétions lacrymales et conjonctivales, sperme), mais la contribution des modes de transmission non respiratoire à l’épidémie reste inconnue, et si tel en était le cas, probablement marginale (9).
À côté des contacts directs, la transmission peut également se faire par contact indirect, les mains se contaminant avec les surfaces. L’importance de ce mode de transmission est inconnue, mais le risque est probablement surtout présent dans les milieux de soins ou au domicile des malades. Le virus peut survivre plusieurs heures sur les surfaces extérieures ; la durée de persistance n’est pas bien connue, et dépend de l’inoculum initial, du type de surface, de la température et de l’humidité ambiante. À titre d’exemple, il a été montré (condition de laboratoire et avec un pulvérisateur à haut débit) une stabilité du virus de l’ordre de 4 heures sur le cuivre, 24 heures sur le carton, et jusqu’à 72 heures sur le plastic et l’acier inoxydable (8). Il est par contre bien établi que le virus est sensible au savon et aux désinfectants usuels (10).
L’une des caractéristiques importantes qui participe à la transmission élevée du SARS-CoV-2 est le fait qu’il puisse être transmis par des personnes avant l’apparition des symptômes (présymptomatiques). En effet, la charge virale est déjà très élevée dans les voies respiratoires supérieures environ 2 à 3 jours avant l’apparition des symptômes pour atteindre son pic 1 jour avant les symptômes et décroître ensuite progressivement. Il a été estimé qu’un peu moins de la moitié (44%) des transmissions se fait à la phase pré-symptomatique (11).
On ne sait pas précisément combien de temps les patients peuvent rester contagieux. Si le virus peut parfois être détecté par RT-PCR plusieurs semaines (jusqu’à environ 6 semaines), il semble généralement ne plus être cultivable à partir du courant de la deuxième semaine (9-10 jours) (12,13) (Figure 1). Il convient donc de rappeler que l’on détecte par PCR de l’ARN et non un virus en état de se répliquer. Une PCR positive ne renseigne donc pas forcément sur l’infectivité du virus (contagiosité).
Il a par ailleurs été bien démontré que certaines personnes infectées peuvent être porteuses asymptomatiques du virus, et peuvent transmettre le virus. Leur contribution relative à l’épidémie reste cependant inconnue.
La durée d’isolement (confinement) recommandée reste l’objet de discussions. Actuellement, les recommandations belges préconisent pour les patients COVID-19 hospitalisés 14 jours d’isolement à partir du premier jour du début des symptômes (à la condition que les symptômes respiratoires s’améliorent et que la fièvre ait disparu depuis au moins 3 jours), une durée portée à 28 jours pour les patients séjournant aux soins intensifs sauf si les contrôles de PCR sont négatifs à deux reprises (14). Un isolement plus court, de 7 jours (moyennant les mêmes conditions d’afébrilité et d’amélioration respiratoire), est préconisé pour les patients non hospitalisés (15).
Le CDC américain recommande de lever l’isolement à partir de 10 jours à dater du début des symptômes, y compris pour les patients hospitalisés, moyennant les mêmes conditions (au moins 3 jours sans fièvre) (13). Une levée d’isolement sur base du suivi de PCR peut aussi être proposée surtout chez des patients immunodéprimés pouvant excréter plus longtemps le virus (13).
Physiopathologie
Les coronavirus sont des virus à ARN simple brin enveloppés. Ils infectent une grande variété d’espèces et sont divisés en quatre genres ; α, β, γ et δ en fonction de leur structure génomique. Les coronavirus humains tels que 229E et NL63 sont responsables d’affections respiratoires bénignes et appartiennent au coronavirus α. En revanche, le SARS-CoV, le coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV) et le SARS-CoV-2 responsable du COVID-19 sont classés parmi les coronavirus β, dit émergents. Les coronavirus ont quatre protéines structurales ; Spike (S), membrane (M), enveloppe (E) et nucléocapside (N). Le récepteur permettant l’entrée du virus dans les cellules qu’il infecte est une molécule présente à leur surface : l’enzyme ACE2. Néanmoins, l’entrée du SARS-CoV-2 dans les cellules cibles se fait également grâce à l'intervention d’une enzyme cellulaire appelée TMPRSS2 (Type II transmembrane serine protease) (16) qui coopère avec ACE2 pour favoriser l’entrée du virus dans la cellule. On peut ainsi imaginer l’ACE2 comme une serrure et TMPRSS2 comme la clé avec laquelle le virus peut l’ouvrir pour rentrer. L’ACE2 est une protéine largement exprimée dans le cœur, les vaisseaux, les intestins, les poumons (en particulier dans les pneumocytes de type 2 et les macrophages), les reins, les testicules et le cerveau. Sa présence dans ces différents organes semble expliquer la variété des tableaux cliniques et des complications liées au COVID-19 (17). Son rôle physiologique est de dégrader l’angiotensine II, afin d’en limiter les effets négatifs (vasoconstriction, inflammation, thrombose) liés à la liaison aux récepteurs AT1. L’entrée du SARS-CoV2 dans la cellule régule à la baisse les récepteurs ACE2, qui perdent dès lors leur capacité de dégradation de l’angiotensine II. C’est cette perte d’expression et d’activité de l’ACE2 qui pourrait être à l’origine de l’inflammation pulmonaire importante et des phénomènes micro-thrombotiques observés (18).
Pronostic
La proportion de patients asymptomatiques parmi les patients infectés est inconnue et varie de 5% à 75% dans la littérature. Elle a été estimée à 46.5 % des malades dans le bateau de croisière Diamond Princess (19) (pour un total de 3711 passagers et membres d’équipage) mais des chiffres plus élevés (jusqu’à 75%) ont été rapportés (20,21).
Parmi les malades (symptomatiques), il est difficile de prédire la sévérité de l’infection. On estime que 80% des malades ont une présentation modérée, 15% une sévère, et 5% sont définis comme critiques (22) (avec insuffisance respiratoire, choc ou défaillance multisystémique) (Tableau 1). De nombreux facteurs de risque ont été identifiés dans de larges cohortes, et incluent en premier lieu l’âge avancé (>65 ans), le sexe masculin et les comorbidités telles que les maladies cardiovasculaires, le diabète, l’hypertension artérielle, les cancers, les maladies respiratoires chroniques (essentiellement la BPCO), l’immunodépression ou encore l’obésité (22,23). Rapidement, tenant compte de la place centrale d’ACE2 dans l’infection COVID-19, il a été postulé que les traitements par inhibiteurs de l’enzyme de conversion (IEC) et les sartans pouvaient être responsables de la sévérité décrite chez les patients hypertendus (24). Cette hypothèse semble actuellement battue en brèche, des études récentes montrant que la mortalité était non affectée ou même diminuée par ces traitements (25).
L’importance de l’âge est majeure : ainsi, en Chine, un taux de mortalité de 0,32% chez les moins de 60 ans, 6,4% chez les plus de 60 ans, et 13,4% au-delà de 80 ans a été mis en évidence (26). A contrario, parmi les enfants, bien que de rares présentations sévères et des décès aient été décrits, les taux d’hospitalisation sont faibles et la très grande majorité des enfants présente un tableau clinique banal (27). La contribution respective des enfants à la transmission interhumaine et à la dynamique pandémique reste discutée (28,29).

Présentation clinique
La période d’incubation de la maladie peut s’étendre jusqu’à deux semaines. Les symptômes apparaissent néanmoins chez la plupart des malades endéans les 4 à 5 jours de la contamination (30,31). À 11 jours 97.5% des personnes ont développé des symptômes.
La présentation classique de la maladie est celle d’une pneumonie, avec fièvre, toux et dyspnée. L’absence de fièvre au départ n’exclut cependant pas le diagnostic : ainsi, dans une large série américaine, seul un peu plus de 30% des malades présentaient une température >38°C au départ (32). La très grande majorité des patients développera néanmoins de la fièvre au cours de l’infection (30). Le clinicien veillera à toujours mesurer la saturation du patient qu’il examine, car l’hypoxie peut parfois être très bien tolérée : on a décrit chez un nombre significatif de patients un aspect d’« hypoxémie silencieuse » (33).
En dehors de la pneumonie, les symptômes de présentation sont variables (Tableau 2).
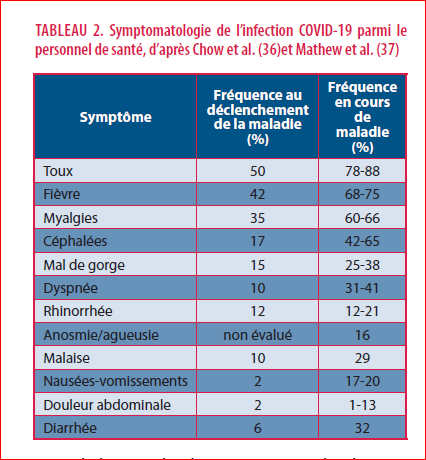
La maladie peut se présenter comme une infection des voies respiratoires supérieures dite banale, et prendre un aspect cliniquement difficilement distinguable d’une autre virose. Dans certains cas rares, le tableau initial peut aussi être dominé ou limité à une symptomatologie digestive (34). Les anomalies du goût et de l’odorat, allant de la perturbation discrète à l’anosmie et/ou l’agueusie complète, ont été bien décrites. Elles peuvent précéder les autres symptômes, ou êtres les seules manifestations de l’infection dans de rares cas (environ 3% des malades dans une série italienne (35). Des éruptions cutanées et des atteintes oculaires (conjonctivite) sont également possibles.
Enfin, des présentations atypiques ne sont pas rares, notamment chez la personne âgée, et le clinicien devra rester vigilant et envisager le diagnostic devant un syndrome gériatrique (chute, delirium, déclin fonctionnel).
La maladie prend volontiers un cours bi-phasique (Figure 1) : après un début modéré, les symptômes s’aggravent et la dyspnée s’installe vers la fin de la première semaine. C’est fréquemment à ce moment-là que les patients avec des présentations sévères sont hospitalisés (18). Dans les cas les plus sévères, l’insuffisance respiratoire s’installe et les patients présentent un tableau d’ARDS. Cette seconde phase de la maladie se présente fréquemment sous la forme d’un tableau très inflammatoire, voire dans les cas les plus sévères, sous forme d’une tempête cytokinique, ce qui fait penser qu’il y a une place dans le traitement pour les médications immunomodulatrices (voir ci-dessous) (38). Les complications cardio-vasculaires (39) et thrombo-emboliques (40) de la maladie ne sont pas rares dans les formes sévères, ce qui est probablement à mettre en liaison avec l’atteinte endothéliale. Une série autopsique allemande a ainsi démontré une thrombose veineuse profonde chez 7 patients sur 12. Pour 4 des malades, l’embolie pulmonaire était la cause directe du décès (41).

Diagnostic
Selon l’un des traditionnels postulats de Koch, l’isolation et la culture du pathogène en laboratoire à partir d’un échantillon d’organe malade est le « gold standard » du diagnostic d’une maladie infectieuse. Toutefois, cette méthode de détection est lente et nécessite un équipement et des techniques de culture spécifiques qui sont limitées à certains types de laboratoires (niveau de sécurité élevée : L3 et L4). Face à cette pandémie, sur le terrain, une technique plus rapide et plus accessible était indispensable pour identifier, isoler et traiter sans tarder les patients atteints.
RT-PCR
L’alternative, devenant l’examen de choix pour le diagnostic, est la recherche directe de l’ARN viral par PCR (Polymerase Chain reaction). Cette recherche se fait sur un frottis nasopharyngé ou oropharyngé. Dans certains cas, celle-ci pourra être réalisée sur des prélèvements par lavage broncho-alvéolaire toutefois il s’agit d’un examen invasif et aérosolisant, réservé à certaines situations cliniques particulières. La sensibilité de la PCR varie selon les études entre 59 et 83% (42,43). Un premier résultat négatif n’exclut donc pas totalement le diagnostic. De même, étant donné l’évolution de la charge virale au cours du temps, si la PCR est réalisée de manière trop précoce ou au-delà d’une semaine de symptômes le résultat peut s’avérer également négatif.
CT- scan
Le scanner thoracique s’est imposé rapidement parmi les outils diagnostiques de première ligne. En effet, les anomalies observées dans les cas confirmés (44) ont permis d’établir des critères diagnostiques classant les patients en différentes catégories : de peu probable à suspect en passant par possible, avec une sensibilité allant jusque 98%. (43,45) ainsi qu’en fonction de l’étendue des lésions qui prédominent à titre de verre dépoli dans les zones basales et postérieures. Grâce à une filière dédiée, les Cliniques universitaires Saint-Luc (CUSL) ont donc rapidement intégré le scanner dans l’algorithme de prise en charge initiale au moment du pic épidémique (Figure 2). Celui-ci supplante dans certains cas très suspects la PCR, conformément à la définition de cas émise par l’institut de santé publique Belge (Sciensano) dans ses recommandations. La performance du scanner dépend cependant de la probabilité pré-test: l'image n'est pas facilement distinguable de certaines autres pneumonies virales ou atypiques.
Sérologies
Pour compléter l’arsenal d’outils diagnostiques, il y a lieu d’évoquer la sérologie. Comme pour la PCR, il faut tenir compte de la fenêtre temporelle puisque les anticorps IgM (et les IgA) commencent à apparaître à partir du 5e jour, et les IgG du 10e jour (46,47). Pour des patients dont les symptômes sont anciens (> une semaine), à un moment où justement la charge virale diminue et fait chuter la sensibilité de la PCR, en combinaison avec le scanner, la recherche de ces anticorps trouve toute sa place pour aider le clinicien dans le diagnostic du COVID-19. Elle trouve surtout sa place pour déterminer la séroprévalence de la maladie au sein des populations (enquêtes épidémiologiques).
Biologies (anomalies évocatrices)
Il existe également plusieurs indices biologiques utilisés en première ligne permettant, si ce n’est de confirmer le diagnostic, à tout le moins d’ajouter des arguments en faveur d’une suspicion d’infection à COVID-19. En plus d’un syndrome inflammatoire (CRP > 5 mg/dl) la lymphopénie, et l’éosinopénie en valeur absolue sont deux anomalies de l’hémogramme très régulièrement retrouvées. Le rapport neutrophile sur lymphocyte (NLR) semble se démarquer comme un facteur pronostic. Une majoration des LDH, isolée ou avec cytolyse hépatique fait partie, si ce n’est des critères diagnostics, certainement des critères de sévérité (48). Il en va de même des anomalies suggestives d’hémophagocytose (élévation persistante de la CRP ainsi que de la ferritine et des triglycérides, diminution du fibrinogène) par les macrophages suractivés.
Traitement
À l’heure actuelle, il est important de rappeler qu’aucun traitement spécifique permettant de guérir l’infection n’est disponible. La prise en charge d’un patient avec une pneumonie à COVID-19 est avant tout supportive : traitement symptomatique de la fièvre, hydratation, etc. Les formes mineures peuvent être prises en charge à domicile. En cas d’hypoxémie par contre une oxygénothérapie sera nécessaire ; c’est le motif principal d’hospitalisation.
L’oxygénothérapie
Le traitement de support respiratoire du patient avec une pneumonie à COVID-19 a fait l’objet d’une stratégie thérapeutique propre aux CUSL. Plusieurs interfaces d’administration sont disponibles et adaptées régulièrement aux besoins en oxygène du patient (Figure 3). Tout d’abord, les lunettes à oxygène qui permettent un débit entre 0,5 et 3l/min. Ensuite le masque facial avec Double Trunk Mask (DTM) équipé de deux tuyaux latéraux qui se positionne en sus des lunettes à oxygène, permet une augmentation de la FiO2 pour le même débit d’oxygène. Finalement, le masque réservoir pour des débits plus élevés (>10 l/min). Le recours à une ventilation non-invasive est aussi possible afin d’augmenter la pression expiratoire à visée de recrutement alvéolaire : la CPAP (Continous Positive Airway Pressure) soit via valve de Boussignac soit par machine à turbine classique est utilisée chez patients très hypoxémiques, tachypnéiques ou éventuellement en cas de toux incoercible (observations cliniques). En cas d’échec des mesures d’oxygénation mise en place en unité COVID, le patient est admis aux soins intensifs pour d’autres types d’oxygénation ou de ventilation nécessitant un monitoring rapproché (OptiFlow, ventilation invasive).

La chloroquine-l’hydroxychloroquine
Ces deux molécules utilisées respectivement dans le traitement du paludisme et des maladies inflammatoires ont montré leur activité in vitro sur le virus, en bloquant son entrée dans la cellule et son endocytose par différents mécanismes (49,50). C’est de Chine que sont parvenues les premières informations d’efficacité clinique potentielle de la chloroquine avec amélioration radiographique, amélioration de la clairance virale et diminution de la progression de la maladie sur base de données préliminaires de 100 patients (51). Par la suite, plusieurs études successives du groupe du Pr. Raoult (52,53) sont venues étayer la thèse d’un effet sur la clearance virale et d’une efficacité clinique. Toutefois, ces résultats n’ont pas pu être reproduits à grande échelle et ces études ont été fortement critiquée pour leur méthodologie. Très récemment, une étude observationnelle de 1376 patients, n’a pas mis en évidence ni une efficacité de l’hydroxychloroquine (HCQ) ni un effet plus délétaire sur un outcome composite (intubation ou décès toute cause) (54). Il convient de rappeler que ces médicaments ont un risque faible de toxicité cardiaque et sont contrindiqués en cas d’ allongement de l’espace QTc. Dans les unités COVID, nous avons décidé de suivre les recommandations belges émises le 13 mars recommandant l’usage de HCQ chez les patients COVID-19 hospitaliser (sauf contre-indication) (55).
L’azithromycine
L’azithromycine (AZM) est un antibiotique connu pour ses propriétés anti-inflammatoires. C’est à nouveau l’équipe marseillaise de Didier Raoult qui est à l’origine de données sur une petie série sans bras comparateur suggérant une efficacité clinique et virologique (diminution de la charge virale) grâce à l’association de l’hydroxychloroquine et de l’azithromycine (53). Par ailleurs, il s’agit d’une molécule qui allonge également l’espace QT chez des patients à risque (âge, antécédents cardiaques,…). Nous avons décidé, aux CUSL, de réserver ce traitement à certains types de patients : sévérité clinique, radiologique ou biologique, et absence de commorbidités cardiaques ; un contrôle ECG étant réalisé après 24 heures de bithérapie, pour s’assurer de l’absence d’allongement du QTc au delà de 500 msec. Une étude est actuellement en cours en Belgique (EudraCT Nbr: 2020-001614-38) à laquelle nous participons.
Le remdesivir
Le remdesevir est un nouvel analogue nucléosidique ayant une activité in vitro contre le SARS-CoV-2 (49). Il a, au départ, été utilisé pour traiter le virus Ebola mais sans succès. Ce traitement a été approuvé par la FDA début mai 2020 au Etats Unis pour des cas de pneumonie à COVID-19 sévères. Hors étude clinique, il n’est pas disponible en Belgique et les données sur son efficacité restent contradictoires et parcellaires, à ce jour.
Des premières données lors d’un usage compassionnel chez des patients atteints de formes sévères de COVID-19, ont montré à une amélioration clinique chez 36 des 53 patients (68%) (56).
Selon les résultats préliminaires de l’analyse intermédiaire d’un essai internationnal randomisé contrôlé sur 1063 malades (Adaptive COVID-19 Treatment Trial, or ACTT), publiés récemment par le National Institute of Allergy and Infectious Diseases aux Etats-Unis (non peer-review), le remdesivir en comparaison au placebo aurait un effet favorable sur le temps de récupération (sortie de l’hôpital ou fin de l’oxygénorequérance) avec une médiane significative de 4 jours en moins (57). À noter également une tendance, mais non significative à ce stade, à une baisse de la mortalité de 3%.
Par contre, dans un essai randomisé en double aveugle en Chine portant sur 237 patients atteints de COVID-19 sévère, le délai d’amélioration clinique n’était pas statistiquement différent avec le remdesivir par rapport au placebo (58). La mortalité à 28 jours et le temps de clairance virale étaient similaires également dans les deux groupes. Par ailleurs, le remdesivir a été arrêté précocement en raison d’événements indésirables (notamment des symptômes gastro-intestinaux, des élévations des enzymes hépatiques ou de la bilirubine et une aggravation de l’état cardiopulmonaire) dans 12% des cas (contre 5% dans le groupe placebo). Plusieurs limites à cette étude : celle-ci a été arrêtée précocement par manque de recrutement, des thérapies concomitantes (lopinavir-ritonavir, interféron alpha-2b et / ou corticostéroïdes) ont été utilisées chez de nombreux patients de l’étude, et les groupes n’étaient pas correctement matchés avec plus de comorbidités dans le groupe remdesivir (hypertension, diabète sucré et maladie coronarienne).
Le lopinavir-ritonavir
Cet inhibiteur de protéase possède une activité in vitro contre le Sars-CoV (59). Il n’a malheureusement pas fait la preuve de son efficacité contre le COVID-19, puisque dans une étude randomisée sur 199 patients, comparé au traitement standard, le temps de résolution clinique, ni la clearance virale ni la mortalité n’ont été diminuées (60).
Il faut signaler que des vastes études internationales (Discovery, Recovery, Solidarity) sont en cours dans lesquelles ces différentes molécules (Remdesevir, lopinavir/ritonavir, Hydroxychloroquine) sont évaluées.
Les anti-interleukine
Étant donné que le COVID-19 provoque une tempête cytokinique (élévations de cytokines inflammatoires comme l’IL6, des marqueurs inflammatoires comme la ferritine, la CRP ou les D-Dimères), l’idée de bloquer la cascade inflammatoire est évidemment une piste très intérressante chez les patients présentant ces signes de tempête.
Le tocilizumab est un inhibiteur du récepteur de l’IL-6 utilisé dans le traitement de maladies auto-immunes comme la polyarthrite rhumatoïde, la maladie de Horton, ou la maladie de Still. Dans un petite étude observationnelle (21 patients) en Chine, l’administration d’une dose unique intraveineuse de tocilizumab s’est traduite par une amélioration clinique chez 91% des patients (61). Une étude réalisée par l’assistance publique des hôpitaux parisiens semble promotteuse et les résultats sont attendus sous peu. Le sarilumab et le siltuximab sont d’autres anti-IL-6 en cours d’évaluation dans plusieurs études internationnales. Ces trois anti-IL-6 ne sont pas disponibles en Belgique hors étude (COVID-aid).
Corticostéroïdes
Une méta-analyse incluant 11 études (5 249 sujets) sur l’impact de la corticothérapie sur les résultats des personnes infectées par le SRAS-CoV-2, le SRAS-CoV ou le MERS-CoV vient récemment d’être publiée (62). Parmi ces études, deux portaient principalement sur de l’association des corticostéroïdes et la clairance virale et 10 ont exploré l’impact des corticostéroïdes sur la mortalité, la durée d’hospitalisation, l’utilisation de la ventilation mécanique et un critère d’évaluation composite. L’utilisation de corticostéroïdes a été associée à une clairance retardée du virus avec une différence moyenne de 3,78 jours, une durée d’hospitalisation prolongée et une augmentation de l’utilisation de la ventilation mécanique.
Il n’y a pas eu de réduction significative des décès avec un rapport de risque relatif (RR) = 1,07 (IC 90% = 0,81; 1,42; I2 = 80%). Cette analyse conclut donc que l’utilisation de corticostéroïdes chez les sujets infectés par le SRAS-CoV-2, le SRAS-CoV et le MERS-CoV n’est pas bénéfique, mais s’agissant (excepté pour une étude dans le SRAS-CoV) d’études observationnelles il est difficile d’exclure que la prescription de corticoïdes par les médecins ne soit en fait qu’une conséquence de la sévérité de la maladie.
Wang et al., quant à eux, ont démontré que chez les patients atteints de pneumonie sévère au COVID-19, de faibles doses de corticostéroïdes administrées précocement et brièvement (1-2mg/kg/j durant 5-7 jours) étaient associées à une amélioration plus rapide des symptômes cliniques et à une amélioration scanographique des images pulmonaires (63). Cependant, il s’agissait d’une recherche observationnelle rétrospective monocentrique avec une petit nombre de patients (n=46 dont 26 traités par corticoïdes). Aux CUSL, en plus du traitement standard par hydroxychloroquine, des corticostéroïdes (méthylprednisolone 0,5 mg / kg pendant 3 à 5 jours) étaient parfois ajoutés après évaluation clinique chez les patients pour lesquels il y avait une contre-indication à l’azythromycine ou chez les patients présentant une aggravation des symptômes respiratoires et un besoin accru d’oxygène malgré le traitement initial par hydroxychloroquine.
Il faut aussi mentionner que les corticoïdes inhalés, largement utilisés pour le traitement de l’asthme et d’autres maladies pulmonaires obstructives, pourraient avoir un impact bénéfique en réduisant l’expression de l’ACE2 dans les cellules bronchiques probablement en limitant la production des interférons (64).
Le plasma de convalescent
L’utilisation de plasma de patient convalescent dans le COVID-19 a été décrite dans quelques séries de cas. Une étude décrit cinq malades avec un COVID-19 sévère, sous ventilation mécanique, avec charge virale élevée, chez qui l’administration de plasma convalescent a permis de diminuer la charge virale nasopharyngée, le score de sévérité, et amélioré l’oxygénation 12 jours après la perfusion (65). Dans un autre série de six malades, qui ont recu le plasma plus tardivement, cinq sont décédés malgré une clairance virale dans les trois jours de traitement (66). En Belgique, des études cliniques devraient également voir le jour pour ce type de traitement (Dawn plasma).
Autres Médications
Anti-inflammatoires non steroidiens (AINS)
La problématique de l’usage des Anti-inflammatoires non stéroidiens (AINS) a été médiatisée par le ministre francais de la santé qui a affirmé sur Twitter que l’utilisation des AINS était responsable de l’aggravation du COVID-19. Cependant, aucune preuve scientifique n’indique que la consommation d’AINS place les patients qui ont une infection légère ou asymptomatique à risque de développer un syndrome respiratoire aigu sévère. Les personnes qui prennent des AINS pour d’autres raisons ne devraient pas cesser de le faire de peur d’augmenter leur risque de complications lié au COVID-19 (62).
Nous ne savons pas avec certitude si les AINS peuvent entraîner une aggravation des symptômes COVID-19, et les prostaglandines (PG), telles que la PGE2, la PGD2 et la prostacycline (PGI2) peuvent à la fois favoriser et limiter l’inflammation. Dans le même ordre d’idée, les patients atteints d’infections à SARS-CoV-2 cliniquement compliquées devraient-ils recevoir des AINS comme traitement ? Non. Il n’y a aucune preuve de bénéfice. Si un tel patient devait également avoir une mauvaise fonction rénale, le maintien du débit sanguin rénal devient extrêmement dépendant des PG vasodilatateurs, tels que la PGE2 et la PGI2. Une telle situation pourrait également prédisposer le patient aux complications gastro-intestinales et cardiovasculaires des AINS (67,68).
Suivi ambulatoire
En principe, tous les patients non gériatriques COVID-19 seront revus en consultation 6 semaines après leur sortie de l'hôpital. Un suivi est prévu en fonction de l'évolution clinique. En cas d'hospitalisation de longue durée pour COVID-19 (post-USI), les patients pourront bénéficier d'un programme de rééducation adapté. Quels examens doivent être effectués ou sont nécessaires pour un suivi standard? Certainement une spirométrie avec mesure de la capacité de diffusion et des volumes pulmonaires, force de serrage à la main (par manomètre), test de marche de 6 minutes, et un CT-scan thoracique. Les anomalies biologiques sanguines et urinaires constatées durant l'hospitalisation seront contrôlées également lors de la consultation. Un suivi diététique et/ou psychologique doit être envisagé au cas par cas.
Affiliations
1) Service de Médecine interne et maladies infectieuses, Cliniques universitaires Saint-Luc, B-1200 Bruxelles
2) Institut de recherche expérimentale et clinique, IREC, UCLouvain, B-1200 Bruxelles
3) Service de médecine Physique et réadaptation, division de kinésithérapie, Cliniques universitaires Saint-Luc, B-1200 Bruxelles
4) Service de Microbiologie, Cliniques universitaires Saint-Luc, B-1200 Bruxelles
5) Service de Pneumologie, Cliniques universitaires Saint-Luc, B-1200 Bruxelles
Correspondance
Pr. Jean-Cyr Yombi.
Cliniques universitaires Saint-Luc
Service de Médecine interne et maladie infectieuses
Avenue Hippocrate 10
B- 1200 Bruxelles
jean.yombi@uclouvain.be
Références
- https://promedmail.org/promed-post/?id=20191230.6864153.
- Wu F, Zhao S, Yu B, et al. A new coronavirus associated with human respiratory disease in China. Nature. 2020;579(7798):265-269.
- Gorbalenya AE, Baker SC, Baric RS, et al. The species Severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARS-CoV-2. Nature Microbiol. 2020;5(4):536-544.
- Pan A, Liu L, Wang C, et al. Association of Public Health Interventions With the Epidemiology of the COVID-19 Outbreak in Wuhan, China. JAMA. 2020.
- Inglesby TV. Public Health Measures and the Reproduction Number of SARS-CoV-2. JAMA. 2020. May 1.doi: 10.1001/jama.2020.7878.
- Bourouiba L. Turbulent Gas Clouds and Respiratory Pathogen Emissions: Potential Implications for Reducing Transmission of COVID-19. JAMA. 2020. Mar 26. doi: 10.1001/jama.2020.4756.
- WHO. Modes of transmission of virus causing COVID-19: implications for IPC precaution recommendations. 29 March 2020.
- van Doremalen N, Bushmaker T, Morris DH, et al. Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV-1. N Engl J Med. 2020;382(16):1564-1567.
- https://bestpractice.bmj.com/topics/en-gb/3000168/pdf/3000168.pdf. 07 may 2020.
- Ren SY, Wang WB, Hao YG, et al. Stability and infectivity of coronaviruses in inanimate environments. World J Clin Cases. 2020;8(8):1391-1399.
- He X, Lau EHY, Wu P, et al. Temporal dynamics in viral shedding and transmissibility of COVID-19. Nature Med. 2020;26(5):672-675.
- Wolfel R, Corman VM, Guggemos W, et al. Virological assessment of hospitalized patients with COVID-2019. Nature. 2020. Apr 1.doi: 10.1038/s41586-020-2196-x.
- Centers for Disease C. Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19. 03 MAY 2020.
- https://COVID-19.sciensano.be/sites/default/files/COVID19/COVID-19_proce... version du 8 mai 2020. 08 MAY 2020.
- https://COVID-19.sciensano.be/sites/default/files/COVID19/COVID-19_proce.... 08 MAY 2020.
- Ziegler CGK, Allon SJ, Nyquist SK, et al. SARS-CoV-2 receptor ACE2 is an interferon-stimulated gene in human airway epithelial cells and is detected in specific cell subsets across tissues. Cell.
- Varga Z, Flammer AJ, Steiger P, et al. Endothelial cell infection and endotheliitis in COVID-19. Lancet. 2020;395(10234):1417-1418.
- Zou X, Chen K, Zou J, Han P, Hao J, Han Z. Single-cell RNA-seq data analysis on the receptor ACE2 expression reveals the potential risk of different human organs vulnerable to 2019-nCoV infection. Front Med. 2020. Mar 12;1-8. doi: 10.1007/s11684-020-0754-0.
- Mizumoto K, Kagaya K, Zarebski A, Chowell G. Estimating the asymptomatic proportion of coronavirus disease 2019 (COVID-19) cases on board the Diamond Princess cruise ship, Yokohama, Japan, 2020. Euro Surveill. 2020;25(10).
- https://www.cebm.net/COVID-19/COVID-19-what-proportion-are-asymptomatic/. 6 April 2020.
- Day M. COVID-19: identifying and isolating asymptomatic people helped eliminate virus in Italian village. BMJ. 2020;368:m1165.
- Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72314 Cases From the Chinese Center for Disease Control and Prevention. JAMA. 2020. Feb 24.doi: 10.1001/jama.2020.2648.
- Preliminary Estimates of the Prevalence of Selected Underlying Health Conditions Among Patients with Coronavirus Disease 2019 — United States FM, 2020. MMWR Morb Mortal Wkly Rep 2020;69:382–386. DOI: http://dx.doi.org/10.15585/mmwr.mm6913e2external.
- COVID-19? Pac-pAiaaprfff. BMJ 2020;368:m810.
- Li J, Wang X, Chen J, Zhang H, Deng A. Association of Renin-Angiotensin System Inhibitors With Severity or Risk of Death in Patients With Hypertension Hospitalized for Coronavirus Disease 2019 (COVID-19) Infection in Wuhan, China. JAMA Cardiology. 2020. Apr 23;e201624.doi: 10.1001/jamacardio.2020.1624.
- Verity R, Okell LC, Dorigatti I, et al. Estimates of the severity of coronavirus disease 2019: a model-based analysis. Lancet Infectious Diseases. 2020 Mar 30;S1473-3099(20)30243-7.
- Ludvigsson JF. Systematic review of COVID-19 in children shows milder cases and a better prognosis than adults. Acta Paediatr. 2020;109(6):1088-1095.
- Brodin P. Why is COVID-19 so mild in children ? Acta Paediatr. 2020;109(6):1082-1083.
- Kam KQ, Yung CF, Cui L, et al. A Well Infant with Coronavirus Disease 2019 (COVID-19) with High Viral Load. Clin Infect Dis. 2020. Feb 28;ciaa201. doi: 10.1093/cid/ciaa201.
- Guan W-j, Ni Z-y, Hu Y, et al. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med. 2020. N Engl J Med. 2020 Apr 30;382(18):1708-1720.
- Li Q, Guan X, Wu P, et al. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia. N Engl J Med. 2020. Mar 26;382(13):1199-1207.
- Richardson S, Hirsch JS, Narasimhan M, et al. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area. JAMA. 2020.
- https://www.medscape.com/viewarticle/928803?src=wnl_tp10n_200508_mscpedi....
- Cheung KS, Hung IF, Chan PP, et al. Gastrointestinal Manifestations of SARS-CoV-2 Infection and Virus Load in Fecal Samples from the Hong Kong Cohort and Systematic Review and Meta-analysis. Gastroenterol. 2020. Apr 3;S0016-5085(20)30448-0.
- Spinato G, Fabbris C, Polesel J, et al. Alterations in Smell or Taste in Mildly Symptomatic Outpatients With SARS-CoV-2 Infection. JAMA. 2020. Apr 22;e206771.doi: 10.1001/jama.2020.6771.
- Chow EJ, Schwartz NG, Tobolowsky FA, et al. Symptom Screening at Illness Onset of Health Care Personnel With SARS-CoV-2 Infection in King County, Washington. JAMA. 2020. pr 17;e206637.doi: 10.1001/jama.2020.6637.
- Characteristics of Health Care Personnel with COVID-19 — United States FA, 2020. MMWR Morb Mortal Wkly Rep 2020;69:477–481. DOI: http://dx.doi.org/10.15585/mmwr.mm6915e6external. µ
- Mehta P, McAuley DF, Brown M, Sanchez E, Tattersall RS, Manson JJ. COVID-19: consider cytokine storm syndromes and immunosuppression. Lancet. 2020;395(10229):1033-1034.
- Wang D, Hu B, Hu C, et al. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China. JAMA. 2020. Feb 7;323(11):1061-1069.
- Klok FA, Kruip M, van der Meer NJM, et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res. 2020. Apr 10:S0049-3848(20)30120-1.
- Wichmann D, Sperhake J-P, Lütgehetmann M, et al. Autopsy Findings and Venous Thromboembolism in Patients With COVID-19: A Prospective Cohort Study. Ann Intern Med. 2020. May 6. doi: 10.7326/M20-2003.
- Ai T, Yang Z, Hou H, et al. Correlation of Chest CT and RT-PCR Testing in Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases. Radiology. 2020:200642.
- Long C, Xu H, Shen Q, et al. Diagnosis of the Coronavirus disease (COVID-19): rRT-PCR or CT? Eur J Radiol. 2020;126:108961.
- Shi H, Han X, Jiang N, et al. Radiological findings from 81 patients with COVID-19 pneumonia in Wuhan, China: a descriptive study. Lancet Infect Dis. 2020;20(4):425-434.
- Fang Y, Zhang H, Xie J, et al. Sensitivity of Chest CT for COVID-19: Comparison to RT-PCR. Radiology. 2020:200432.
- Xiang F, Wang X, He X, et al. Antibody Detection and Dynamic Characteristics in Patients with COVID-19. Clin Infect Dis. 2020. Apr 19;ciaa461.
- Sethuraman N, Jeremiah SS, Ryo A. Interpreting Diagnostic Tests for SARS-CoV-2. JAMA. 2020. May 6. doi: 10.1001/jama.2020.8259.
- Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 Mar 28;395(10229):1054-1062.
- Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Research. 2020;30(3):269-271.
- Yao X, Ye F, Zhang M, et al. In Vitro Antiviral Activity and Projection of Optimized Dosing Design of Hydroxychloroquine for the Treatment of Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2). Clin Infect Dis. 2020. Mar 9;ciaa237. doi: 10.1093/cid/ciaa237.
- Gao J, Tian Z, Yang X. Breakthrough: Chloroquine phosphate has shown apparent efficacy in treatment of COVID-19 associated pneumonia in clinical studies. BioScience Trends. 2020;14(1):72-73.
- Gautret P, Lagier J-C, Parola P, et al. Hydroxychloroquine and azithromycin as a treatment of COVID-19: results of an open-label non-randomized clinical trial. Int J Antimicrobial Agents. 2020:105949.
- Gautret P, Lagier JC, Parola P, et al. Clinical and microbiological effect of a combination of hydroxychloroquine and azithromycin in 80 COVID-19 patients with at least a six-day follow up: A pilot observational study. Travel Med Infect Dis. 2020:101663.
- Geleris J, Sun Y, Platt J, et al. Observational Study of Hydroxychloroquine in Hospitalized Patients with COVID-19. N Engl J Med. 2020. May 7. doi: 10.1056/NEJMoa2012410.
- https://COVID-19.sciensano.be/sites/default/files/COVID19/COVID-19_Inter.... March 2020.
- Grein J, Ohmagari N, Shin D, et al. Compassionate Use of Remdesivir for Patients with Severe COVID-19. N Engl J Med. 2020. Apr 10;NEJMoa2007016.
- https://www.niaid.nih.gov/news-events/nih-clinical-trial-shows-remdesivi... accessed on April 29, 2020.
- Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet.2020; doi.org/10.1016/S0140-6736(20)31022-9.
- Groneberg DA, Poutanen SM, Low DE, Lode H, Welte T, Zabel P. Treatment and vaccines for severe acute respiratory syndrome. Lancet Infect Dis. 2005;5(3):147-155.
- Cao B, Wang Y, Wen D, et al. A Trial of Lopinavir–Ritonavir in Adults Hospitalized with Severe COVID-19. N Engl J Med. 2020. May 7;382(19):1787-1799.
- Xu X, Han M, Li T, et al. Effective treatment of severe COVID-19 patients with tocilizumab. Proc Natl Acad Sci U S A. 2020. Apr 29;202005615.
- Li H, Chen C, Hu F, et al. Impact of corticosteroid therapy on outcomes of persons with SARS-CoV-2, SARS-CoV, or MERS-CoV infection: a systematic review and meta-analysis. Leukemia. 2020. May 5;1-9. doi: 10.1038/s41375-020-0848-3.
- Wang Y, Jiang W, He Q, et al. Early, low-dose and short-term application of corticosteroid treatment in patients with severe COVID-19 pneumonia: single-center experience from Wuhan, China. medRxiv. 2020:2020.2003.2006.20032342.
- Maes T, Bracke K, Brusselle GG. COVID-19, Asthma, and Inhaled Corticosteroids (ICS): Another Beneficial Effect of ICS? [published online ahead of print, 2020 May 21]. Am J Respir Crit Care Med. 2020;10.1164/rccm.202005-1651ED. doi:10.1164/rccm.202005-1651ED
- Shen C, Wang Z, Zhao F, et al. Treatment of 5 Critically Ill Patients With COVID-19 With Convalescent Plasma. JAMA. 2020;323(16):1582-1589.
- Zeng QL, Yu ZJ, Gou JJ, et al. Effect of Convalescent Plasma Therapy on Viral Shedding and Survival in COVID-19 Patients. J Infect Dis. 2020. Apr 29;jiaa228. doi: 10.1093/infdis/jiaa228.
- FitzGerald GA. Misguided drug advice for COVID-19. Science. 2020;367(6485):1434.
- Fang L, Karakiulakis G, Roth M. Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection? Lancet Respir Med. 2020;8(4):e21.
