Myélome multiple : avancées thérapeutiques d’une maladie chronique
Marie Christiane Vekemans
Le myélome multiple (MM) représente 10% des hémopathies malignes. Son pronostic a été révolutionné grâce à l’usage des immunomodulateurs, des inhibiteurs du protéasome et des anticorps monoclonaux. Malheureusement, malgré le recours à ses 3 classes thérapeutiques, le MM reste une maladie incurable. Les efforts de la communauté scientifique portent sur le développement de stratégies visant à contrôler profondément la maladie au diagnostic de manière à retarder la rechute, et en cas de rechute, proposer des alternatives innovantes permettant, par exemple, de réarmer le système immunitaire afin de contrôler et détruire les cellules tumorales.
Schémas à quatre drogues pour les patients éligibles à la greffe, en première ligne thérapeutique
La triple combinaison Velcade-lenalidomide-dexame-thasone (VRD) est largement utilisée comme traitement d’induction chez les patients atteints de MM, en première ligne thérapeutique. Différents agents peuvent être ajoutés à ce back-bone, afin d’obtenir des réponses plus profondes et plus durables.
Le daratumumab et l’isatuximab sont deux anticorps monoclonaux dirigés contre le récepteur CD38 présent à la surface des cellules myélomateuses, de bons candidats pour remplir cette mission compte tenu de leur profil de sécurité favorable. Leur usage a fait l’objet de communications lors du dernier congrès de la Société Américaine d’Hématologie à Atlanta en décembre 2021.
L’efficacité de l’isatuximab a été étudiée dans une étude de phase III (1), où 662 patients nouvellement diagnostiqués avec un MM et éligibles à l’autogreffe, ont été randomisés pour recevoir le VRD comme traitement d’induction, avec ou sans isatuximab. L’association Isa-VRD s’est révélée très efficace. 77.3% des patients atteignent au moins une très bonne réponse partielle (VGPR) (diminution du pic de > 90%) (contre 60.5% avec VRD) et 50.1% atteignent une maladie résiduelle (MRD) négative (mesurée par cytométrie - NGF avec une sensibilité à 10-5)(contre 35.6% avec VRD), et cela, quel que soit le sous-groupe concerné.
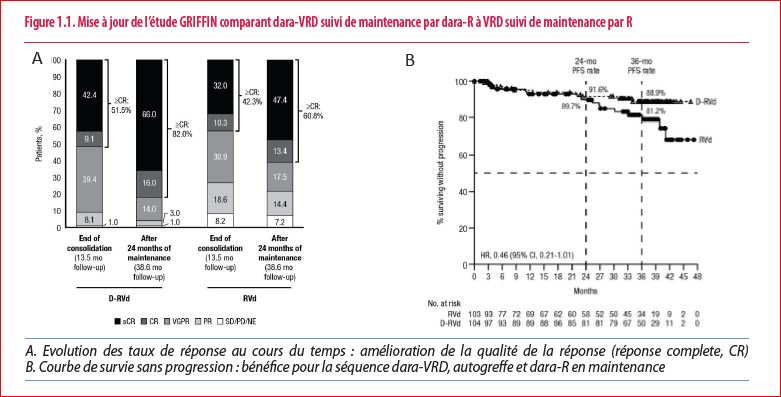
L’étude GRIFFIN a elle, étudié l’ajout de daratumumab au VRD (2). Cette étude de phase II avait déjà démontré que la quadruple association permettait d’améliorer de manière significative les taux de réponse complète stringente (sCR)(pas de protéine monoclonale détectable dans le sang, normalisation du rapport kappa/lambda et absence des cellules myélomateuses dans la moelle) après 4 cycles d’induction, suivi d’autogreffe et de 2 cycles de consolidation (3). Durant le congrès, les investigateurs ont rapporté les résultats du traitement de maintenance de 2 ans, prévoyant l’administration de dara-R chez les patients randomisés dans le bras dara-VRD ou R chez les patients randomisés dans le bras VRD. Pour les 207 patients ayant terminé cette phase de traitement, la maintenance par dara-R permet d’amener plus de patients en sCR (66% versus 47%), mais aussi en MRD négative (64.4% versus 30.1%) (Figure 1.1). La quadruple combinaison a 3x plus de chance de maintenir cette MRD négative au-delà de 12 mois, ce qui nous permet d’espérer des périodes sans progression plus longues. Une étude similaire de phase III, l’étude CEPHEUS, est actuellement en cours et devrait confirmer ces excellents résultats.
Guider le traitement sur la maladie résiduelle
L’étude MASTER est un essai américain de phase III qui a le mérite de proposer une stratégie thérapeutique basée sur la réponse au traitement. Elle propose un autre schéma à quatre drogues, associant daratumumab-carfilzomib-lénalidomide-dexaméthasone (dara-KRd) administré pour 4 cycles d’induction, suivi d’autogreffe et de 2 cycles de consolidation (4). À chaque phase de traitement, le statut MRD est déterminé en biologie moléculaire par NGS, et guide la suite de la prise en charge. Deux mesures de MRD négatives consécutives permettent de suspendre le traitement et de placer le patient en surveillance.
Les premiers résultats sont encourageants. 86 % des patients atteignent une réponse complète ou mieux, 80%, une MRD négative mesurée avec un seuil de sensibilité à 1 x 10-5, 66%, une MRD négative mesurée avec un seuil de sensibilité à 1 x 10-6. Il s’agit des taux de MRD négatives les plus élevés observés à ce jour chez les patients nouvellement diagnostiqués avec un MM.
On note un approfondissement de la réponse à chaque phase de traitement, phénomène observé quelles que soit les anomalies génétiques impliquées au départ. L’autogreffe augmente le taux de MRD négative après l’induction, avec un impact particulièrement significatif dans le sous-groupe de patients présentant un statut cytogénétique défavorable.
Chez les patients dont le traitement a été stoppé, aucun décès n’a été déploré des suites d’une progression de l’affection myélomateuse. Quasi aucun patient atteignant une MRD négative n’a progressé ou vu réapparaître une maladie résiduelle après arrêt du traitement, alors qu’il présentait 0/1 anomalie génétique défavorable au diagnostic.
Cette stratégie thérapeutique permet d’entrevoir le suivi de la MRD comme alternative à l’administration indéfinie d’un traitement de maintenance.
Premier traitement par CAR-T approuvé pour les myélomes en phase avancée
L’Abecma est le premier CAR-T (chimeric antigen receptor T) avalisé par l’Agence Européenne du Médicament pour le traitement des MM en rechute ou réfractaire après un minimum de quatre lignes de traitement incluant un immunomodulateur, un inhibiteur du protéasome et un anticorps monoclonal anti-CD38.
La technique des CAR-T se base sur la collecte de lymphocytes T d’un patient, leur modification en laboratoire de façon à leur faire exprimer un récepteur capable de reconnaître un antigène de surface des cellules tumorales, et leur réinjection chez le patient de manière à tuer les cellules malignes.
Ce domaine de l’immunothérapie est en pleine expansion, ce type de traitement permettant d’obtenir des taux de réponse (y compris MRD négative) très élevés, dans une population de patients réfractaires à de multiples lignes de traitement, dont le pronostic est souvent extrêmement réservé.
L’essai CARTITUDE-1 étudie un autre CAR-T, le cilta-cel, et porte sur 97 patients pour lesquels on bénéficie d’un suivi médian de 18 mois (5). Après une seule infusion de cilta-cel, le taux de réponse globale avoisine les 98%, avec des taux de sCR de 80.4%, et la plupart des patients atteignent une MRD négative. Les malades qui maintiennent la MRD négative au-delà de 6 voir 12 mois, ont évidemment les meilleurs taux de survie.
Si on compare les résultats obtenus dans l’essai CARTITUDE-1 aux données de vie réelle collectées en Belgique (traitements conventionnels administrés dans le même contexte de rechute, registre BELCOMM), après ajustement, l’administration de CAR-T offre 3x plus de chances d’obtenir une réponse, et 11x plus de chances d’atteindre une VGPR, en comparaison des traitements standard (Figure 1.2) (6).
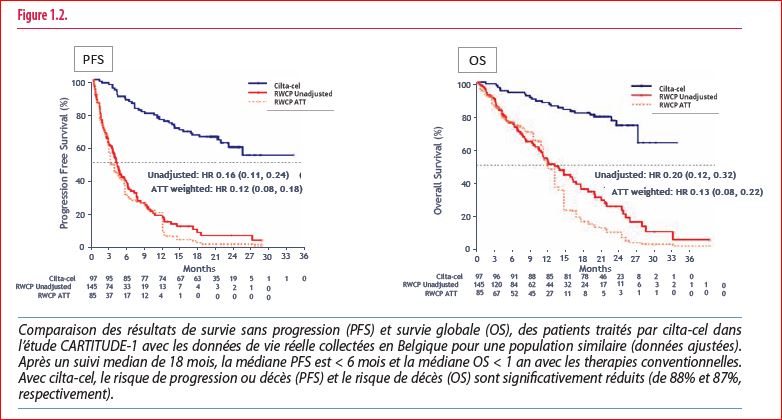
Les CAR-T feront, sans aucun doute, partie de l’arsenal thérapeutique que nous pourrons proposer aux patients dans l’avenir, y compris à des stades bien plus précoces de leur affection.
Place à l’immunothérapie chez les patients atteints de myélome multiple en rechute ou réfractaire
Les anticorps bispécifiques, aussi appelés bispecific T-cell engagers, sont aussi un mode d’immunothérapie permettant de rediriger les cellules T vers les cellules tumorales.
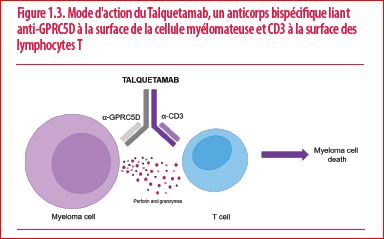
À l’inverse des CAR-T, ils sont composés de deux anticorps différents fusionnés, leur permettant de se lier d’un côté aux cellules myélomateuses, et de l’autre côté, aux cellules du système immunitaire (Figure 1.3). La plupart des anticorps bispécifiques ciblent BCMA (B-cell maturation antigen), un récepteur présent à la surface des cellules myélomateuses.
Le Talquetamab est un anticorps bispécifique qui cible une autre protéine que BCMA, GPRC5D (G protein-coupled receptor family C group 5 member D), une cible très prometteuse car fortement exprimée à la surface des cellules myélomateuses, mais peu présente à la surface des tissus sains.
Les résultats des doses recommandées pour la phase 2 ont été rapportés chez 95 patients, la plupart d’entre eux ‘triple-class’ réfractaires. Administré 2x par semaine en SC à la dose de 800 µg/kg, le taux de réponse globale est de 71% (≥ VGPR, 53%), avec des réponses durables s’approfondissant au cours du temps, moyennant les effets secondaires habituels observés (syndrome de relargage des cytokines, diminution de la leucocytose, sensibilité aux infections, troubles cutanés et désordres du goût) (7).
Dans une autre étude de phase 1, le Talquetamab a pas été combiné au daratumumab chez 29 patients atteints de MM, exposé à ≥ 6 lignes antérieures de traitement. Sur 21 patients évaluables, 17 présentent une réponse, sans majoration des toxicités habituellement observées avec ces 2 drogues données en monothérapie (8).
CELMoDs, une nouvelle classe de médicaments immunomodulateurs
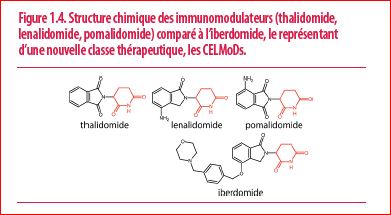
L’iberdomide fait partie d’une nouvelle classe de médicaments appelées CELMoDs (cereblon E3 ligase modulators) (Figure 1.4). Apparenté au lénalidomide et au pomalidomide, l’iberdomide est un agent plus puissant de par ses propriétés tumoricides et immuno-stimulantes comparé aux IMiDs.
Durant le congrès, ont été présentés les résultats d’une étude de phase 1/2 étudiant l’iberdomide combiné à la dexaméthasone chez les patients lourdement pré-traités (≥ 6 lignes antérieures de traitement). Le taux de réponse globale est de 26.2%, pour une durée moyenne de réponse de 7 mois, une médiane de survie sans progression (PFS) de 3 mois, et une survie médiane de 11.2 mois. Des résultats similaires ont été observés dans la cohorte préalablement exposée à un agent anti-BCMA (9).
Les effets secondaires habituels portent sur des anomalies de l’hémogramme, avec un risque accru d’infections.
Une étude de phase 3 comparant iberdomide-daratumumab-dexaméthasone à daratumumab-Velcade-dexaméthasone est en cours chez les patients en phase avancée.
Encore une nouvelle classe de médicaments, les immunocytokines
Les immunocytokines sont des composés hybrides associant cytokines et anticorps monoclonal (Figure 1.5). Le modakafusp alfa fusionne 2 molécules d’interféron alpha-2b modifiées à la portion Fc d’un anticorps monoclonal humanisé IgG4 anti-CD38. Cette construction permet de délivrer de l’interféron aux cellules myélomateuses CD38+, de façon à empêcher leur division tout en boostant les cellules immunes combattant le myélome.
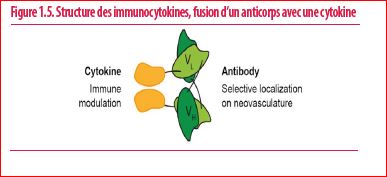
Dans une étude de phase I (10), le modakafusp alfa permet d’obtenir des taux de réponse globale de 42 %, même chez les patients réfractaires aux anticorps monoclonaux anti-CD38 ou traités par anti-CD38 dans leur dernière ligne thérapeutique, car la fixation de ce composé se fait sur un épitope différent que celui utilisé par les anti-CD38 habituels. La PFS médiane est de 5.7 mois et une médiane de réponse de 7.4 mois. 20 % des patients répondent encore après thérapies ciblant BCMA.
Références
- Goldschmidt H. , Mai E.K. , Nievergall E. et al. Addition of isatuximab to lenalidomide, bortezomib and dexamethasone as induction therapy for newly-diagnosed, transplant-eligible multiple myeloma patients: the phase III GMMG-HD7 trial. ASH. 2021; #463.
- Laubach JP, Kaufman JL, Sborov DW, et al. Daratumumab (dara) plus lenalidomide, bortezomib, and dexamethasone (RVd) in patients (pts) with transplant-eligible newly diagnosed multiple myeloma (NDMM): updated analysis of GRIFFIN after 24 months of maintenance.ASH. 2021; #79.
- Voorhees P, Kaufman JL, Laubach J et al. Daratumumab, lenalidomide, bortezomib and dexamethasone for transplant-eligible newly diagnosed multiple myeloma: the GRIFFIN trial. Blood. 2020; 136(8):936-945.
- Costa LJ, Chhabra S, Callander NS, et al. Daratumumab, Carfilzomib, lenalidomide and dexamethasone (dara-KRd), autologous transplantation and MRD response-adapted consolidationand treatment cessation. Final primary endpoint analysis of the MASTER trial. ASH. 2021, #481.
- Martin T, Usmani SZ, Berdeja JG, et al. Updated results from CARTITUDE-1 : phase 1b/2 study of ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T cell therapy, in patients with relapsed/refractory multiple myeloma. ASH. 2021, #549.
- Vekemans MC, Delforge M, Depaus J, et al. Ciltacabtagene autoleucel for patients with tripl-class exposed multiple myéloma: adjusted comparison of CARTTUDE-1 patients outcomes versus Real-world clinical practice in Belgium. Proceedings of the 37th General Annual Meeting of the BHS. 2022; oral presentation.
- Updated phase 1 results from MonumenTAL-1 : first-in-human study of Talquetamab, a G-protein-coupled receptor family C group 5 member D x CD3 bispecific antibody, in patients with relapsed/refractory multiple myeloma. ASH. 2021, #158.
- Chari A, Hari P, Bahlis NJ et al. Phase 1b results of subcutaneous talquetamab plus daratumumab in patients with relapsed/refractory multiple myeloma. ASH. 2021, #161.
- Lonial S, Popat R, Hulin C, et al. Iberdomide (IBER) in combination with dexamethasone (DEX) in patients with relapsed/refractory multiple myeloma (RRMM): results from the dose-expansion phase of the CC-220-MM-001 trial. ASH.. 2021, #162.
- Vogl DT, Kaufman JL, Holstein SA, et al. Modakafusp alfa (TAK-573), an immunocytokine, shows clinical activity in patients with relapsed/refractory multiple myeloma; updated results from a first-in-human phase 1 study. ASH. 2021, #898.
La leucémie myéloïde chronique : un traitement par inhibiteur de tyrosine kinase à vie ?
Violaine Havelange
La prise en charge des patients souffrant de leucémie myéloïde chronique (LMC) a profondément changé ces dernières années. La plupart des patients souffrant d’une LMC en phase chronique ont une espérance de vie quasiment identique à celle de la population normale. Les inhibiteurs de tyrosine kinase (ITK) de première génération (imatinib) depuis 2001 et ensuite de seconde génération (dasatinib, nilotinib, and bosutinib) et de troisième génération (ponatinib) ont révolutionné le pronostic de ces patients. Cependant, ces thérapies ‘ciblées’ ont des effets secondaires qui altèrent, à des degrés divers, la qualité de vie de ces patients.
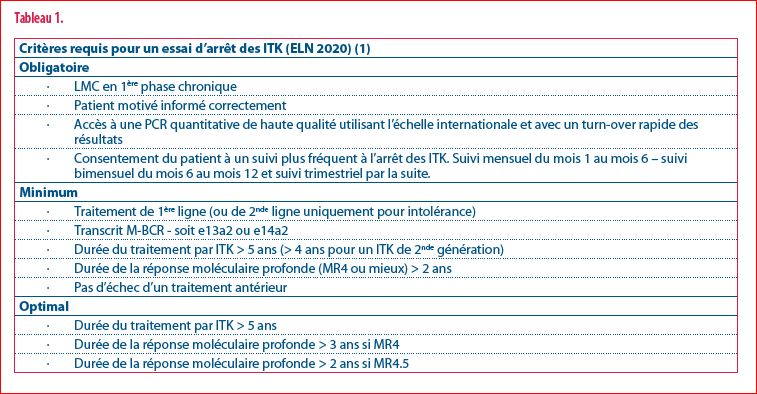
Un nouveau but du traitement confirmé par un panel d’experts européens en 2020 (European LeukemiaNet) (1) est actuellement de pouvoir arrêter les ITK et d’obtenir une rémission prolongée à l’arrêt du traitement. Un essai d’arrêt d’ITK peut être discuté avec le patient et réalisé dans certaines conditions après l’obtention et la durée suffisante d’une réponse moléculaire profonde (Tableau 1) (1). La réponse moléculaire profonde est définie par un taux de transcrit résiduel BCR-ABL ≤ 0.01% soit une baisse de minimum 4 log (MR4 ou plus) mesurée par PCR quantitative selon l’échelle internationale. L’étude STIM1 publiée en 2010 a mis en évidence que 38% des patients avec une LMC et un transcrit BCR-ABL non détecté pendant 2 ans restaient en rémission 77 mois après l’arrêt des ITK (2). Parmi les nombreuses études suivantes, une étude multicentrique académique européenne (EURO-SKI) a étudié l’arrêt des ITK chez 755 patients et a mis en évidence une survie sans rechute moléculaire de la LMC chez 50% des patients à 2 ans de l’arrêt des ITK (3). Les critères minimums d’arrêt sont un traitement par ITK de 3 ans et une réponse moléculaire profonde de minimum 1 an (Tableau 1). En moyenne, 50-60% des patients vont rechuter à l’arrêt des ITK. 80% des rechutes ont lieu dans les 6 premiers mois suivant l’arrêt. Les ITK doivent être repris dès la perte de réponse moléculaire majeure (soit un transcrit BCR-ABL > 0.1% mesuré selon l’échelle internationale) et permettent l’obtention rapide d’une nouvelle réponse moléculaire profonde chez presque tous les patients. De rares cas de progression en phase blastique ont été rapportés mais on ignore si cette évolution a été favorisée par l’arrêt des ITK. 25% des patients vont présenter des douleurs musculosquelettiques ou articulaires quelques semaines ou mois après l’arrêt des ITK, possiblement dues à l’arrêt des effets ‘off target’ des ITK. Ces douleurs sont modérées et transitoires mais nécessitent parfois la prise d’anti-inflammatoires.
Si l’on considère qu’une réponse moléculaire profonde est obtenue chez 40% des patients avec une LMC nouvellement diagnostiquée et que 50% resteront en rémission à l’arrêt des ITK ; cela représente 20% des patients nouvellement diagnostiqués.
L’arrêt des ITK nécessite un suivi rapproché de la maladie résiduelle. En Belgique, depuis le 1er juillet 2021, l’Inami rembourse ces tests PCR rapprochés. Le groupe d’experts européen recommande un suivi mensuel les 6 premiers mois, un suivi bimensuel du mois 6 au mois 12 et ensuite une reprise du suivi trimestriel à vie (1).
Les recherches en cours cherchent à définir les facteurs pronostiques d’un succès de l’arrêt du traitement et surtout à augmenter le pourcentage de patients qui restera en rémission à l’arrêt (4).
Divers facteurs pronostiques prédictifs d’un succès de l’arrêt ont été décrits. Selon l’étude EURO-SKI, la durée de traitement par ITK, la réponse moléculaire profonde et un traitement par interféron augmentaient les succès à l’arrêt (3). La durée de la réponse moléculaire profonde est actuellement décrite comme le facteur le plus important. La probabilité de rester en réponse à l’arrêt des ITK augmenterait de 3% par année supplémentaire de traitement (3). La profondeur de la réponse moléculaire influence également le taux de succès. Plusieurs études ont montré que les ITK de seconde génération permettaient d’obtenir davantage de réponse moléculaire profonde que l’imatinib mais ces résultats n’ont pas été confirmés par l’étude allemande CML-study 4 qui a montré un taux de réponse moléculaire profonde similaire à 10 ans de traitement (5).
La rechute à l’arrêt des ITK chez 50% des patients serait due à la persistance de cellules souches leucémiques (CSL) quiescentes qui expriment faiblement BCR-ABL. Différents groupes de recherche tentent d’isoler ces CSL par des techniques telles que la PCR génomique, la PCR digitale, la cytométrie de flux. Une étude récente a mis en évidence la persistance du BCR-ABL principalement dans les lymphocytes B à l’arrêt des ITK.
Plusieurs études cliniques actuellement en cours ont pour objectif d’éliminer ces CSL pour maintenir la rémission à l’arrêt des ITK. Des traitements associant du ruxolitinib ou un inhibiteur de BTK ou un inhibiteur de bcl2 avec un ITK sont en cours d’étude (4).
Certains mécanismes immunitaires seraient éteints durant le traitement par ITK. A l’arrêt des ITK, on observe une augmentation des cellules NK, une diminution des cellules T régulatrices et des cellules dendritiques plasmocytoïdes CD86+. Les CSL persistantes exerceraient un contrôle immunologique chez des patients en rémission à l’arrêt des ITK. Un traitement de maintenance par interferon permettrait de maintenir une rémission à l’arrêt des ITK. Des études cliniques combinant un inhibiteur du checkpoint et un ITK sont également en cours d’évaluation sur la stabilité de la rémission à l’arrêt mais les risques d’effets indésirables ne doivent pas être négligés.
En conclusion, la prise en charge des patients souffrant de LMC en phase chronique est en pleine évolution. Lors du diagnostic, l’hématologue peut maintenant aborder l’objectif de pouvoir potentiellement arrêter le traitement par ITK aux effets secondaires importants. Des études sont en cours pour isoler et cibler ces CSL persistantes qui seraient à l’origine des rechutes.
Références
- Hochhaus A, Baccarani M, Silver RT, Schiffer C, Apperley JF, Cervantes F, et al. European LeukemiaNet 2020 recommendations for treating chronic myeloid leukemia. Leukemia. 2020;34(4):966-984. doi: 10.1038/s41375-020-0776-2.
- Mahon FX, Réa D, Guilhot J, Guilhot F, Huguet F, Nicolini F, et al.; Intergroupe Français des Leucémies Myéloïdes Chroniques.Discontinuation of imatinib in patients with chronic myeloid leukaemia who have maintained complete molecular remission for at least 2 years: the prospective, multicentre Stop Imatinib (STIM) trial. Lancet Oncol. 2010 ;11(11):1029-35.
- Saussele S, Richter J, Guilhot J, Gruber FX, Hjorth-Hansen H, Almeida A, et al.; EURO-SKI investigators. Discontinuation of tyrosine kinase inhibitor therapy in chronic myeloid leukaemia (EURO-SKI): a prespecified interim analysis of a prospective, multicentre, non-randomised, trial. Lancet Oncol. 2018;19(6):747-757. doi: 10.1016/S1470-2045(18)30192-X.
- Hochhaus A, Ernst T.TKI discontinuation in CML: how do we make more patients eligible? How do we increase the chances of a successful treatment-free remission? Hematology Am Soc Hematol Educ Program. 2021;2021(1):106-112. doi: 10.1182/hematology.2021000238.
- Kalmanti L, Saussele S, Lauseker M, Müller MC, Dietz CT, Heinrich L, et al. .Safety and efficacy of imatinib in CML over a period of 10 years: data from the randomized CML-study IV. Leukemia. 2015;29(5):1123-32. doi: 10.1038/leu.2015.36.
L’émergence de nouveaux traitements dans la myélofibrose
Violaine Havelange, Stefan N. Constantinescu
La myélofibrose (MF) est une des trois néoplasies myéloprolifératives philadelphie négative la plus fréquente. La myélofibrose est soit primitive, soit secondaire à une polycythemia vera ou à une thrombocytémie essentielle. Les mutations drivers (JAK2, CALR, MPL) et d’autres mutations impliquées dans des néoplasies myéloïdes vont entraîner une prolifération des progéniteurs myéloïdes en absence de cytokines, une émergence de clones des cellules souches mutées et en même temps une augmentation de l’expression de cytokines inflammatoires et une fibrose dans l’environnement ‘niche’ de la moelle osseuse.
Les manifestations cliniques de la MF incluent des symptômes constitutionnels médiés par les cytokines (fièvre, perte de poids, sudations nocturnes), des cytopénies dues à un échec progressif de la moelle, une hématopoïèse extra-médullaire et des symptômes mécaniques dus à la splénomégalie (1,2). La MF est un groupe de maladies hétérogènes avec des taux de progression de transformation blastique et de décès variables dépendant de facteurs pronostiques cliniques et génétiques.
Le seul traitement curatif est l’allogreffe de cellules souches périphériques mais celle-ci reste associée à un taux élevé de morbidité et de mortalité.
Les inhibiteurs de JAK (JAK1 et JAK2) – ruxolitinib (Jakavi ®) et fedratinib permettent de diminuer les symptômes constitutionnels et la splénomégalie chez des patients non candidats à l’allogreffe (3). Le momelotinib et le pacritinib sont 2 autres inhibiteurs de JAK en cours d’étude de phase III qui pourraient être bénéfiques en cas d’anémie ou de thrombopénie. Les inhibiteurs de JAK ne sont pas curatifs mais apportent un bénéfice clinique pendant plusieurs années. La moitié des patients vont présenter une nouvelle progression de la maladie (symptômes et splénomégalie) après 2- 3 ans de traitement par ruxolitinib.
De nouvelles molécules sont en cours d’étude clinique dans la prise en charge de ces patients (2,4,5) (Figure 3.1). Le but de ces nouveaux traitements est d’obtenir un effet synergique ou additionnel au ruxolitinib pour approfondir et allonger la réponse sur les symptômes et la splénomégalie chez des patients encore non traités. En plus de l’activation constitutive de la voie JAK-STAT, l’activation d’autres voies de signalisation affectant la prolifération, la survie et la production de cytokines inflammatoires, serait impliquée dans la progression de la maladie et dans la résistance au ruxolitinib (4). Une question majeure sera l’effet de ces nouvelles molécules sur les taux de transformation blastique de la myélofibrose.
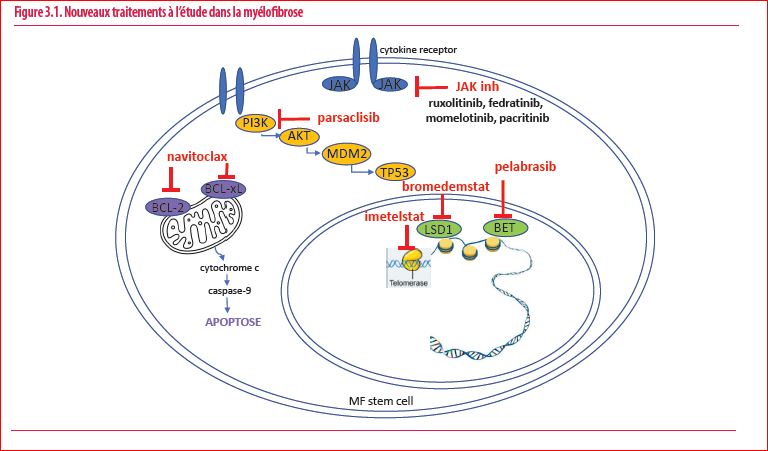
- Le pelabrasib (CPI-0610) est un inhibiteur oral des protéines BET (protéines à Bromodomain et domaine Extra-Terminal) qui va modifier l’expression de gènes impliqués dans la voie NF-kb. Le pelabrasib va supprimer la production de cytokines, normaliser la différenciation mégacaryocytaire et promouvoir la différenciation érythrocytaire. Il a été administré en monothérapie ou ajouté au ruxolitinib chez des patients réfractaires ou intolérants (6,7). Des résultats encourageants sur les symptômes, la splénomégalie mais également sur les besoins transfusionnels, le degré de fibrose et le taux de cytokines inflammatoires ont été observés. L’effet secondaire principalement rapporté était une thrombocytopénie. L’étude MANIFEST-2 de phase 3 randomisée, en cours, étudie l’effet de l’adjonction du pelabrasib au ruxolitinib chez des patients MF non traités.
- Le navitoclax est un inhibiteur oral de BCL-XL, BCL2, et BCL-W, des protéines de la famille anti-apoptotiques - BCL2. Dans une étude de phase 2, le navitoclax a été ajouté au ruxolitinib et a permis d’obtenir une réponse sur la rate et sur les symptômes chez 30% des patients (8). Une réduction du degré de fibrose ≥ 1, une leucoréduction et une diminution des besoins transfusionnels ont également été observées. La thrombocytopénie était l’effet secondaire principalement rapporté. Une étude de phase 3 est, en cours, en combinaison avec le ruxolitinib en 1ère ligne (TRANSFORM-1) ou en 2ème ligne (TRANSFORM-2) de traitement.
- Le luspatercept est un agent maturant de l’érythropoïèse qui lie et inhibe les ligands de la superfamille du TGF- β, réduit la signalisation aberrante de Smad2/3 et favorise l’érythropoïèse et donc la maturation des globules rouges dans leurs stades terminaux. Dans une étude de phase 2, chez les patients MF transfusion dépendants, 36% sous ruxolitinib et 19% sans ruxolitinib sont devenus indépendants des transfusions avec une durée médiane de réponse de 55 et 59 semaines respectivement (9). L’effet secondaire principal était une hypertension chez 13% des patients. Une étude de phase 3 (INDEPENDANCE) étudie actuellement l’effet du luspatercept chez des patients présentant une anémie transfusion dépendante sous inhibiteur de JAK.
- Le parsaclisib est un inhibiteur oral hautement sélectif de PI3Kδ en cours d’investigation chez des patients souffrant de MF. L’adjonction de parsaclisib au ruxolitinib entraînerait une diminution de la taille de la rate et des symptômes chez une partie de ces patients (10). Les effets secondaires principaux étaient une thrombopénie, de la fatigue, des infections, une hypertension et une majoration des tests hépatiques. Des études de phase 3 randomisées en 1ère ou 2ème ligne de traitement sont en cours.
- L’imetelstat est un inhibiteur de l’activité de la télomérase qui a montré son efficacité (réduction de la taille de la rate et des symptômes) dans une étude randomisée de phase 2 chez des patients en rechute/réfractaires au ruxolitinib. Une diminution de la fibrose médullaire ainsi qu’une diminution de la fréquence allélique de la mutation driver ont été observées chez 40% des patients (11). La toxicité était surtout hématologique chez un tiers des patients.
- Le bromedemstat est un inhibiteur oral de la lysine-specific demethylase-1 (LSD1) qui modifie la chromatine. La LSD1 lie GFIb, un facteur de transcription clé impliqué dans la différenciation et la maturation des mégacaryocytes. Dans une étude de phase 2 chez des patients résistants au ruxolitinib, une diminution de la splénomégalie a été observée chez 81% des patients et des symptômes chez 30% des patients (12). 26% des patients ont présenté une amélioration d’au moins un grade au niveau de la fibrose et 42% une réduction du pourcentage d’allèles mutés de la mutation driver.
En conclusion, la myélofibrose reste une pathologie difficile à traiter. L’allogreffe est la seule option curative mais tous les patients ne peuvent pas en bénéficier suite à leur âge ou leurs comorbidités. De nouveaux agents thérapeutiques sont très promoteurs non seulement au niveau de leur efficacité sur les symptômes et la splénomégalie mais également au niveau de leur potentiel effet anti-fibrotique et réducteur sur le clone muté.
Références
- Tefferi A. Primary myelofibrosis: 2021 update on diagnosis, risk-stratification and management. Am J Hematol. 2021 Jan;96(1):145-162.
- Tefferi A, Gangat N, Pardanani A, Crispino JD. Myelofibrosis: genetic characteristics and the emerging therapeutic landscape. Cancer Res. 2021 Dec 15 : canres.2930.2021.
- Devos T, Selleslag D, Granacher N, Havelange V, Benghiat FS. Updated recommendations on the use of ruxolitinib for the treatment of myelofibrosis.Hematology. 2022 Dec;27(1):23-31.
- England J, Gupta V. Novel therapies vs hematopoietic cell transplantation in myelofibrosis: who, when, how? Hematology Am Soc Hematol Educ Program. 2021 Dec 10;2021(1):453-462. doi: 10.1182/hematology.2021000279.
- Bankar A, Gupta V. Investigational non-JAK inhibitors for chronic phase myelofibrosis. Expert Opin Investig Drugs. 2020 May;29(5):461-474.
- Talpaz M, Rampal R, Verstovsek S, et al. CPI-0610, a Bromodomain and Extraterminal Domain Protein (BET) Inhibitor, As Monotherapy in Advanced Myelofibrosis Patients Refractory/Intolerant to JAK Inhibitor: Update from Phase 2 MANIFEST Study. Blood. 136, 2020
- Verstovsek S, Mascarenhas J, Kremyanskaya M, et al.: CPI-0610, Bromodomain and Extraterminal Domain Protein (BET) Inhibitor, As “Add-on” to Ruxolitinib, in Advanced Myelofibrosis Patients with Suboptimal Response: Update of MANIFEST Phase 2 Study. Blood. 136, 2020.
- Mascarenhas J, Harrison C, Andrea P, et al.: CPI-0610, a Bromodomain and Extraterminal Domain Protein (BET) Inhibitor, in Combination with Ruxolitinib, in JAK-Inhibitor-Naïve Myelofibrosis Patients: Update of MANIFEST Phase 2 Study. Blood. 136, 2020
- Harrison CN, Garcia, JS., Mesa RA., et al.: Results from a Phase 2 Study of Navitoclax in Combination with Ruxolitinib in Patients with Primary or Secondary Myelofibrosis Blood 134, 2019
- Gerds AT, Vannucchi AM, Passamonti F, et al. Duration of Response to Luspatercept in Patients (Pts) Requiring Red Blood Cell (RBC) Transfusions with Myelofibrosis (MF) – Updated Data from the Phase 2 ACE-536-MF-001 Study. Blood. 136:47-48, 2020
- Yacoub A, Stouffs M, Zhou F, et al: Abstract CT253: A Randomized, Double-Blind, Placebo-Controlled Phase 3 Study of Parsaclisib Plus Ruxolitinib in Patients with Myelofibrosis Who Have Suboptimal Response to Ruxolitinib. Cancer Research. 2021; 81: CT253-CT253.
- Mascarenhas J, Komrokji RS, Palandri F, et al. Randomized, Single-Blind, Multicenter Phase II Study of Two Doses of Imetelstat in Relapsed or Refractory Myelofibrosis. J Clin Oncol. 2021; JCO2002864.
- Gill H, Yacoub A, Pettit K, et al. A Phase 2 study of the LSD-1 inhibitor IMG-7289 (Bomedemstat) for the treatment of advanced myelofibrosis. EHA2021 Virtual Congress Abstract Book. HemaSphere. 2021 ; 5 : e566.
CAR-T cells ou autogreffe pour les rechutes de lymphomes agressifs ?
Xavier Poiré, Sarah Bailly, Catherine Lambert, Nicole Straetmans, Eric Van Den Neste
Cette question a déjà été abordée dans les éditions des années précédents de ce numéro consacré aux innovations. En bref rappel, les CAR-T sont des lymphocytes isolés et cultivés en laboratoire auxquels on fait exprimer un récepteur spécifique d’une tumeur (Figure 4.1).
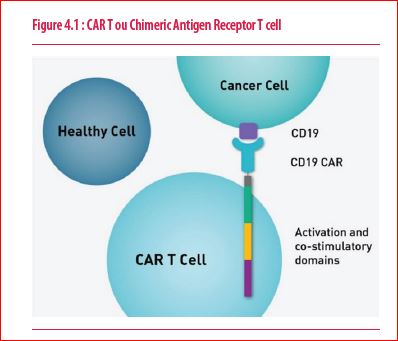
On obtient ainsi un médicament cellulaire capable de « tuer » la cible tumorale. Actuellement, nous avons de plus en plus d’expériences avec deux d’entre eux qui ciblent, via le CD19, les lymphomes agressifs. Depuis juillet 2019, les cliniques universitaires Saint-Luc ont la chance d’être un des quatre centres belges à pouvoir appliquer cette thérapeutique innovante. Actuellement, ce traitement n’est disponible que pour les lymphomes agressifs ayant échoué à moins 2 lignes de traitements. Des rémissions à long terme sont observées dans 40% des cas. Comme devant tout nouveau traitement efficace, la question se pose de l’intérêt de l’introduire plus précocement dans l’histoire de la maladie. Lors du dernier congrès d’hématologie américain (American Society of Hematology, ASH) en décembre à Atlanta, les résultats de 3 études prospectives ont été rapportés.
Les lymphomes B diffus à grandes cellules sont les lymphomes agressifs les plus fréquents. Le traitement de première ligne par immuno-chimiothérapie, le célèbre R-CHOP, permet une rémission prolongée dans près de 70% des cas. Pour les patients en rechute ou réfractaires à cette première ligne, l’approche standard reste une chimiothérapie de rattrapage à base de sels de platine, suivie chez les patients répondeurs, d’une intensification thérapeutique et d’une autogreffe de cellules souches hématopoïétiques. Au total, cette approche ne permet des rémissions prolongées que dans 20% des cas et s’accompagne d’une toxicité immédiate mais également d’une toxicité à long terme. Ce traitement standard a ainsi été comparé à l’administration de CAR T dans 3 études internationales prospectives et randomisées : ZUMA-7, TRANSFORM et BELINDA. ZUMA-7 utilise le CAR T Yescarta® ou Axi-cel. Une inclusion de 359 patients de 59 ans d’âge médian a montré un avantage des CAR-T en termes de survie sans événement et de taux de rémission. TRANSFORM n’a inclus que 92 patients dans chaque bras. Le CAR-T utilisé était le Liso-cel ou Breyanzi®. A nouveau, un avantage significatif en taux de rémission et en survie sans événement a été avancés en faveur des CAR-T. Enfin, l’étude BELINDA randomise le CAR-T Tisa-cel ou Kymriah® versus l’autogreffe de cellules souches hématopoïétiques. Dans cette étude ayant inclus 322 patients, aucun avantage des CAR-T n’a pu être avancé. Le tableau 4.1 reprend les résultats des différentes études.
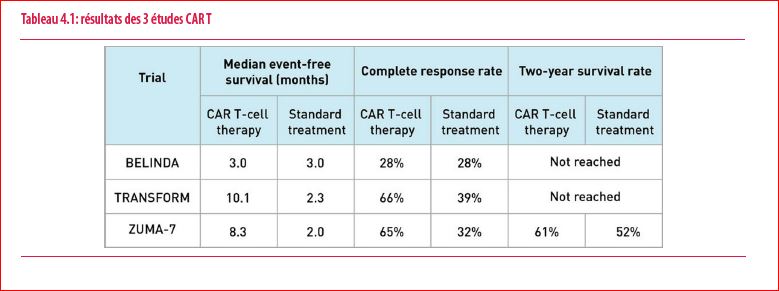
Il est bien-sûr impossible de faire une comparaison directe entre ces 3 études et on ne peut certainement conclure de ces résultats que le CAR-T de BELINDA ou Kymriah est moins efficace que les autres dans cette indication. Une comparaison prospective des différents CAR-T disponibles serait certainement bienvenue mais on sait comment il est difficile de mettre en place des études comparant des médicaments innovants différents. Il est certain que ces trois CAR-T partagent certaines similarités mais ils sont définitivement trois produits différents en particulier en ce qui concerne leur domaine de co-stimulation. Ce dernier est primordial pour l’expansion et la survie des CAR-T in vivo. Par contre, on peut dégager des différences significatives en terme de méthodologie entre les 3 études. L’étude ZUMA-7 n’autorisait aucune chimiothérapie d’attente avant l’infusion des CAR-T alors que l’étude TRANSFORM autorisait un maximum d’un cycle de chimiothérapie d’attente. Ceci est important car le temps de production des CAR-T varie entre 4 et 8 semaines, temps pendant lequel le patient doit rester plus ou moins stable et ne pas présenter de progression trop importante de sa maladie. Dans l’étude BELINDA, il était possible d’administrer autant de chimiothérapie d’attente que nécessaire avant l’infusion des CAR-T. Il est donc possible que les différences de résultats observés soient secondaires à l’inclusion de lymphomes plus agressifs dans l’études BELINDA que dans les autres études. En ce qui concerne les toxicités, elles restaient dans les taux attendus avec ce type de traitement.
Malgré ces remarques, il est fort probable que les CAR-T vont prendre une place de plus en plus importante dans l’arsenal thérapeutique des lymphomes agressifs en seconde ligne. Néanmoins, il est encore trop tôt pour conclure que les CAR-T vont définitivement remplacer la procédure d’intensification thérapeutique avec autogreffe de cellules souches hématopoïétiques. Il faudra certainement définir des facteurs cliniques et biologiques qui nous permettront de mieux identifier quels sont les patients qui bénéficieront le mieux d’une attitude par rapport à une autre. Et enfin de rajouter que l’autogreffe a un coût de 30 à 40 000 EUR contre 250 000 EUR pour les CAR-T. Même si la vie n’a pas de prix, c’est un facteur qu’il faut conserver dans l’équation quand on évalue le réel bénéfice.
Références
- Locke F et al. Primary Analysis of ZUMA-7: a phase 3 randomized trial of axicabtagene ciloleucel (Axi-cel) versus standard-of-care therapy in patients with relapsed/refractory large B-cell lymphoma. ASH Annual Meeting 2021, Atlanta.
- Kamdar et al. Lisocabtagene maraleucel (Liso-cel), a CD19-directed chimeric antigen receptor (CAR) T cell therapy, versus standard of care (SOC) with salvage chemotherapy (CT) followed by autologous stem cell transplantation (ASCT) as second-line (2L) treatment in patients with relapsed or refractory (R/R) large B-cell lymphoma (LBCL): results from the randomized phase 3 Transform study. ASH Annual Meeting 2021, Atlanta.
- Tisagenlecleucel versus standard of care as second-line therapy of primary refractory or relapsed aggressive B-cell non-Hodgkin lymphoma: analysis of the phase III Belinda study. ASH Annual Meeting 2021, Atlanta.
La mutation TP53 en danger dans les leucémies myéloïdes aiguës et les syndromes myélodysplasiques
Xavier Poiré, Nicole Straetmans
La présence d’une mutation de TP53 assombrit le pronostic de plusieurs tumeurs malignes. Dans le contexte des leucémies myéloïdes aiguës et des syndromes myélodysplasiques, on retrouve ce type de mutations dans environ 20% des cas. La présence de mutations de TP53 est associée à une survie à long terme largement inférieure à 6 mois après thérapie standard. Chez les répondeurs, seule une consolidation par allogreffe de cellules souches hématopoïétiques permet une survie prolongée dans près de 20% des cas. TP53 est le gardien du génome, envoyant la cellule en apoptose dès qu’il détecte des dommages au niveau de l’ADN. C’est ainsi qu’en présence d’une ou plusieurs mutations de TP53, les dommages infligés par la chimiothérapie standard ne sont pas détectés et la cellule cancéreuse ne meurt donc pas. La présence de mutations de TP53 est donc associée à un taux élevé de patients réfractaires à la chimiothérapie standard et de nouvelles thérapeutiques sont urgemment en demande dans ce sous-groupe de malades.
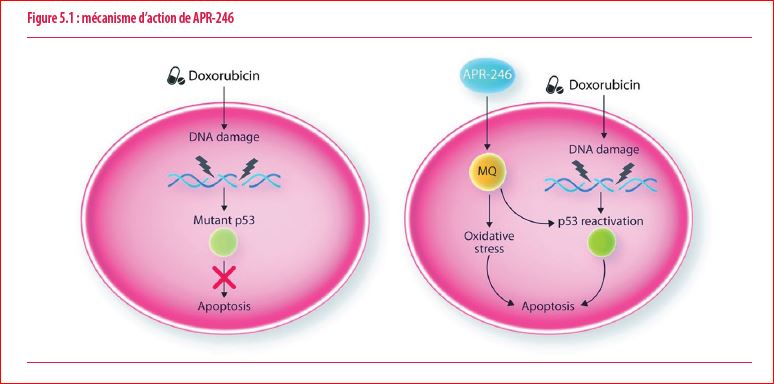
L’APR-246 ou éprénatopopt est la première molécule du genre. Elle se fixe au TP53 mutant, le stabilise et restaure son activité (Figure 5.1). La cellule cancéreuse peut donc à nouveau entrer en apoptose. Cette molécule a été testée en monothérapie avec certains résultats encourageants, mais c’est en combinaison qu’on attendait l’essentiel d’activité. Nous avons ainsi 3 études rapportées lors du congrès de décembre dernier à Atlanta. Une première étude apporte les résultats à long-terme de 100 patients atteints de syndrome myélodysplasique ou de leucémie myéloïde aiguë, et traités par l’association de APR-246 et azacitidine. Le taux de réponse globale était de 70% avec une survie médiane de 12 mois. Parmi les patients en réponse et bénéficiant d’une consolidation par allogreffe de cellules souches hématopoïétiques, le gain en survie était significatif avec une médiane non atteinte après un suivi médian de 28 mois. Comme l’allogreffe de cellules souches hématopoïétiques reste à ce jour la meilleure stratégie thérapeutique pour les leucémies myéloïdes aiguës et syndromes myélodysplasiques avec mutations TP53, cette même association d’APR-246 et azacitidine a été essayée en maintenance après greffe chez 33 patients. D’une part, cette association était correctement tolérée et d’autre part, une survie sans rechute à un an de 58% a été mise en évidence, ce qui est assez exceptionnel pour ce type de maladie. Enfin, l’APR-246 a été associé à l’azacitidine et au venetoclax dans une étude de phase I. Au total, 47 patients ont été inclus et aucune toxicité limitante n’a été détectée. En terme d’efficacité, un taux de rémission complète y compris avec récupération hématologique incomplète a été observé dans 53% ce qui est très élevé compte tenu de la population à très haut risque incluse dans cette étude.
Les leucémies myéloïdes aiguës et syndromes myélodysplasiques avec mutation TP53 restent une population difficile à traiter avec des taux de réponse faibles et de courte durée. L’avènement de l’APR-246 va probablement nous permettre d’avoir plus de répondeurs parmi ces patients. Une consolidation par allogreffe de cellules souches hématopoïétiques sera probablement toujours nécessaire car la durée de réponse à cette nouvelle thérapeutique reste à démontrer.
Références
- Sallman et al. Long term follow-up and combined phase 2 results of eprenetapopt (APR-246) and azacitidine (AZA) in patients with TP53 mutant myelodysplastic syndromes (MDS) and oligoblastic acute myeloid leukemia (AML). ASH Annual Meeting 2021, Atlanta.
- Mishra et al. Phase II trial of eprenetapopt (APR-246) in combination with azacitidine (AZA) as maintenance therapy for TP53 mutated AML or MDS following allogeneic stem cell transplantation (SCT). ASH Annual Meeting 2021, Atlanta.
- Garcia-Manero et al. Phase I and expansion study of eprenetapopt (APR-246) in combination with venetoclax (VEN) and azacitidine (AZA) in TP53-mutant acute myeloid leukemia (AML). ASH Annual Meeting 2021, Atlanta.
PF4, Facteur XI, Antithrombine : « Stars » 2021 de la coagulation sanguine
Cédric Hermans
PF4 : Implication dans les thromboses associées aux vaccins COVID-19 à vecteur adénoviral
Si les bénéfices des vaccins contre le SARS-Cov-2 ne sont plus à démontrer, le début de leur utilisation a été terni par la survenue d’accidents thrombotiques rares mais exceptionnellement sévères chez des personnes récemment vaccinées. Endéans quelques semaines, plusieurs groupes en Norvège, Allemagne et Royaume Uni, ont rapporté des cas de thromboses veineuses cérébrales et/ou viscérales associées à une thrombopénie et à la présence d’anticorps anti-PF4. Ce nouveau syndrome appelé VITT (Vaccine-Induced Immune Thrombotic Thrombocytopena) a été initialement observé après administration du vaccin d’Astra Zeneca mais aussi chez des personnes ayant reçu le vaccin de Johnson & Johnson, deux vaccins utilisant un vecteur adénoviral.
On comprend aujourd’hui que le VITT est une affection auto-immune caractérisée par le développement d’anticorps activant les plaquettes sanguines, avec pour conséquence la survenue de thromboses artérielles et veineuses. Une coagulopathie de consommation caractérise le VITT associant thrombopénie, réduction du fibrinogène et majoration des D-Dimères. Très rapidement, il a été mis en évidence que les patients avec VITT développent des anticorps anti-PF4 à un titre élevé.
Les anticorps anti-PF4 sont classiquement recherchés lors d’une suspicion de thrombopénie chez les patients traités par héparine pour exclure un HIT (héparine induced thrombocytopenia), une complication observée surtout après administration d’héparine non fractionnée et expliquée par le développement d’anticorps contre un néo-antigène formé par l’association de molécules d’héparine (chargées électriquement négativement) et le PF4 (chargé positivement). Le PF4 est physiologiquement présent dans les granules alpha des plaquettes sanguines. Lors de l’activation des plaquettes sanguines, le PF4 est libéré et neutralise les glycosaminoglycans chargés négativement physiologiquement présents à la surface des cellules endothéliales qu’ils dotent de propriétés anticoagulantes. Même si les mécanismes ne sont pas élucidés, il est fort probable qu’un composé du vecteur adénoviral se fixe au PF4 et suscite, comme pour l’héparine, la formation d’un nouvel antigène et la production d’anticorps anti-PF4 (Figure 6.1).
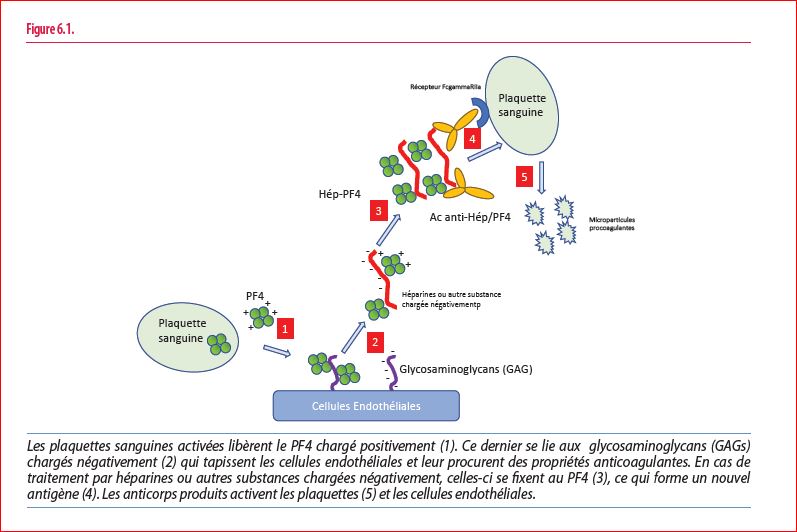
Chez les patients qui développent un VITT, comme ceux bien plus fréquents qui ont un HIT, les anticorps anti-PF4 se fixent aux plaquettes (via le récepteur FcgammaRIIA) qu’ils activent, ce qui contribue à la formation de thrombi. Ce mécanisme rend compte de l’approche thérapeutique qui, outre le recours à l’anticoagulation (idéalement sans héparine) fait appel à l’administration d’immunoglobulines intraveineuses, éventuellement d’échanges plasmatiques, d’immunosuppresseurs, autant de stratégies pour maîtriser la réaction immunitaire.
Le VITT apporte une nouvelle illustration de l’implication du PF4 dans certains processus thrombotiques. Pour rappel, au-delà du HIT, l’implication d’anticorps anti-PF4 en dehors de l’exposition à l’héparine a été antérieurement décrite parmi des patients avec complications thrombotiques et thrombocytopénie, dans le décours d’intervention chirurgicale (arthroplastie du genou) ou pris en charge pour des problèmes infectieux. D’autres molécules que l’héparine peuvent se fixer au PF4 et générer la formation d’anticorps anti-PF4. Il s’agit de médicaments (pentosan polysulfate, chondroïtine hypersulphatée) ou des molécules polyanioniques naturelles (lipopolysaccharide bactérien, ADN/ARN). Ces données suggèrent l’importance de considérer la recherche d’anticorps anti-PF4 chez tout patient avec thrombose et thrombocytopénie.
FXI : Nouvelle cible des anticoagulants
Le facteur XI (FXI) de la coagulation fait partie des facteurs dits « de la phase de contact » avec un rôle dans le processus d’hémostase longtemps sous-estimé. Des études épidémiologiques et de récents travaux avec un modèle murin ont cependant pointé ce facteur comme pouvant être le graal du traitement anticoagulant, et dont l’inhibition permettrait de prévenir les thromboses sans augmenter le risque hémorragique.
Parmi les différentes méthodes étudiées pour diminuer l’effet du FXI, un anticorps monoclonal – l’abélacimab – a récemment fait l’objet d’une étude de phase 2. Dans cet essai de détermination de dose, l’abélacimab a été comparé à l’énoxaparine dans une population de patients à faible risque chez qui une prothèse totale de genou était programmée. Il convient de souligner que, dans ce contexte, l’incidence de thromboses veineuses profondes (TVP) et d’embolies pulmonaires symptomatiques est faible et ce sont les TVP asymptomatiques mises en évidence par phlébographie du membre concerné qui ont fait l’objet du critère de jugement principal.
Les 412 patients inclus ont été randomisés entre le traitement classique par énoxaparine 1 ×/jour et l’une des 3 doses d’abélacimab administrée en dose intraveineuse (IV) unique en postopératoire. Alors que la faible dose (30 mg) d’abélacimab s’est montrée non inférieure à l’énoxaparine, avec 13 % de thromboses, les deux autres doses (75 et 150 mg) ont été associées à la survenue d’une thrombose chez respectivement 5 et 4 % des patients seulement, par rapport à 22 % dans le groupe énoxaparine (p < 0,001). L’incidence des événements hémorragiques était similaire dans les groupes : 2 %, 2 % et 0 % dans les groupes traités par 30, 75 et 150 mg d’abélacimab, alors qu’il n’y a eu aucun événement dans le groupe énoxaparine.
Cette étude vient conforter les résultats obtenus dans le même contexte clinique avec un oligonucléotide antisens diminuant la production de FXI, mais qui devait être injecté en sous-cutané 9 fois (dont 8 dans les 36 jours précédents la chirurgie). Cela reste bien sûr une étude de phase 2, avec de petits collectifs, sans critères de jugement d’efficacité clinique, le tout dans un marché où les anticoagulants actuellement disponibles sont déjà très efficaces et sûrs. Les études de phase 3 en cours apporteront le fin mot de cette histoire qui démarre tout de même avec des premiers résultats encourageants.
Déficit en Antithrombine induit par ARN interférent et prévention des hémorragies des patients hémophiles
Le traitement classique de l’hémophilie, du moins sans sa forme sévère, caractérisée par un déficit complet en facteur VIII (FVIII) (hémophilies A) ou IX (FIX) (hémophilie B) de la coagulation, repose sur l’administration intraveineuse régulière du facteur qui fait défaut. Le but de ce traitement est de maintenir en permanence une petite quantité de FVIII ou FIX dans le sang et de prévenir les hémorragies. Ce traitement est contraignant (injections intraveineuses régulières) et n’est pas dénué d’effets secondaires sous forme de développement d’allo-anticorps neutralisant le FVIII ou rarement FIX administré. De multiples stratégies de traitement alternatif sont en cours d’étude ou de validation. Une de ces approches, originale, est de réduire l’inhibition naturelle de la coagulation et de promouvoir ainsi la formation de thrombine et la capacité de coagulation. En d’autres termes, il s’agit d’induire chez les patients hémophiles un état thrombophilique afin de rebalancer la coagulation. Une des cibles de cette approche est l’antithrombine, l’inhibiteur le plus important de la coagulation.
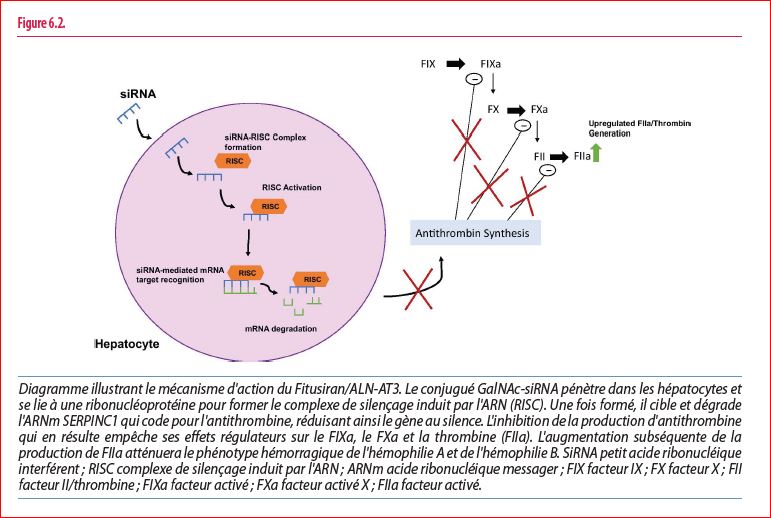
L’approche proposée pour réduire la concentration de l’antithrombine est d’administrer par voie sous-cutanée un ARN interférent (fitusiran) qui réduit la synthèse et donc la concentration circulante d’antithrombine (Figure 6.2). L’intention est de rééquilibrer l’hémostase chez les patients hémophiles, A ou B, avec ou sans inhibiteur.
Deux études de phase III rendues publiques en décembre 2021 ont comparé un traitement prophylactique mensuel par fitusiran (80 mg) à l’utilisation à la demande de concentrés de facteur de coagulation, pour l’étude ATLAS-A/B, et à l’utilisation à la demande d’agents de bypass du FVIII ou FIX (complexe prothrombinique activé ou rFVIIa), dans le cadre de l’étude ATLAS-INH. Dans ces deux études cliniques, le traitement prophylactique par fitusiran a permis d’obtenir une réduction des taux de saignements annualisés de plus de 89 % comparativement aux groupes témoins, soit une amélioration statistiquement et cliniquement significative des saignements comparativement aux traitements à la demande, ainsi qu’une amélioration significative de la qualité de vie, chez les patients sans et avec inhibiteur.
Il s’agit de résultats prometteurs même si on peut questionner le protocole de l’étude qui a comparé un traitement à la demande au fitusiran et non pas un traitement régulier préventif. Une autre préoccupation est la survenue d’accidents thrombotiques, très rares dans ces deux études, mais antérieurement rapportés avec le fitusiran.
Références
- Klok FA, Pai M, Huisman MV, Makris M. Vaccine-induced immune thrombotic thrombocytopenia. Lancet Haematol. 2022 Jan;9(1):e73-e80. doi: 10.1016/S2352-3026(21)00306-9. Epub 2021 Nov 11.
- Warkentin TE, Greinacher A. Spontaneous HIT syndrome: Knee replacement, infection, and parallels with vaccine-induced immune thrombotic thrombocytopenia. Thromb Res. 2021 Aug;204:40-51. doi: 10.1016/j.thromres.2021.05.018. Epub 2021 Jun 9.
- Verhamme P, Yi BA, Segers A, Salter J et al. Abelacimab for Prevention of Venous Thromboembolism. N Engl J Med. 2021 Aug 12;385(7):609-617. doi: 10.1056/NEJMoa2105872. Epub 2021 Jul 19.
- Pasi KJ, Lissitchkov T, Mamonov V, et al. Targeting of antithrombin in hemophilia A or B with investigational siRNA therapeutic fitusiran-Results of the phase 1 inhibitor cohort. J Thromb Haemost. 2021 Jun;19(6):1436-1446. doi: 10.1111/jth.15270. Epub 2021 May 18.
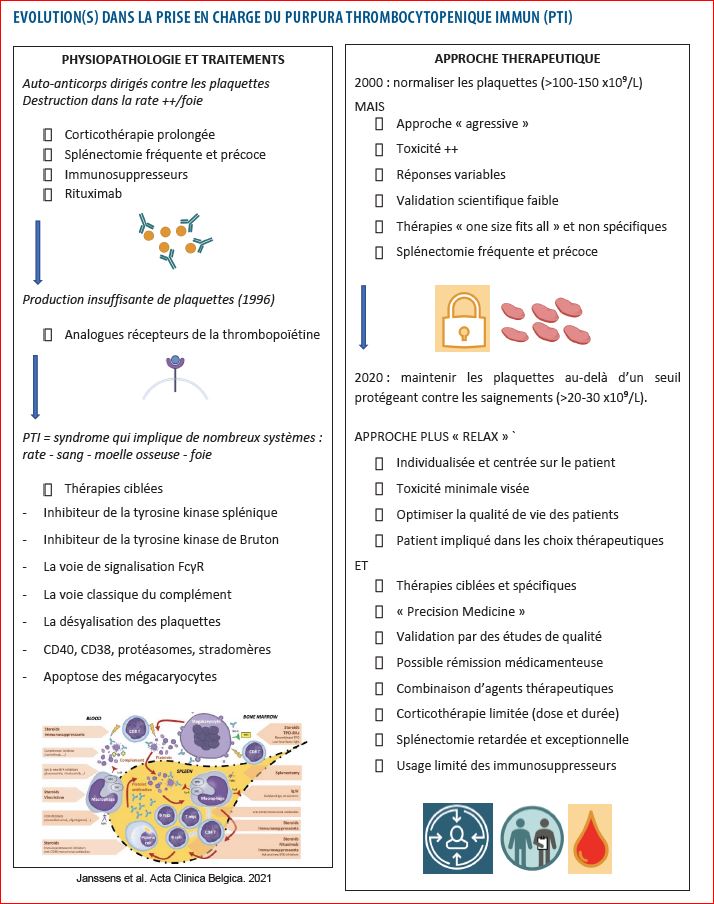
Prise en charge du purpura thrombocytopénique immune (PTI)
Catherine Lambert
Affiliations
1. Service d’Hématologie – Cliniques universitaires Saint-Luc – 1200 Bruxelles
2. Institut de Duve, Université catholique de Louvain et Ludwig Cancer Research Bruxelles.
3. Walloon Excellence in Life Sciences and Biotechnology (WELBIO), Brussels, Belgium
Correspondance
Pr. Cédric Hermans
Cliniques universitaires Saint-Luc
Service d’hématologie
Avenue Hippocrate 10
B-1200 Bruxelles
cedric.hermans@uclouvain.be