Apnées obstructives liées sommeil : nouveaux traitements de type médicamenteux
Charlotte Smetcoren, Gimbada Benny Mwenge
Les traitements mécaniques de l’apnée obstructive du sommeil (AOS) (CPAP, ou orthèse d’avancée mandibulaire) sont limités par une observance faible. Les limites de la CPAP font des agents pharmacologiques un avantage car les médicaments sont plus facilement acceptables et constituent une option alternative pour les patients. L’obésité est un facteur de risque de l’AOS chez 45 % des patients. Des essais randomisés ont évalué l’efficacité des traitements amaigrissants (Phentermine 15 mg + Topiramate 92 mg / Liraglutide) pendant 28 à 32 semaines respectivement, démontrant une réduction de l’indice d’apnée-hypopnée (IAH) significative par rapport au placebo, attribué essentiellement à la perte de poids. Cependant ces dernières années, la littérature rapporte que la contribution de facteurs non anatomiques (endotypes, liés aux mécanismes sous-jacents) est nécessaire pour que l’apnée obstructive se développe chez au moins 70 % des patients (1). L’expansion de la thérapie pharmacologique non mécanique pour l’AOS peut ainsi constituer une option non invasive pour les patients.
Une stratégie consiste à augmenter le tonus musculaire dilatateur des voies respiratoires supérieures pendant le sommeil. Une seule étude d’un jour d’administration a démontré qu’une dose d’atomoxétine-oxybutynine au coucher a réduit l’IAH de 63 % (-16 événements/h). D’autres études évaluant l’activation pharmacologique du noyau moteur hypoglosse pour l’apnée obstructive du sommeil sont en cours (2).
Environ 30 à 50 % des patients atteints AOS ont des seuils d’excitation cérébrale respiratoire bas, ce qui les rend sujets à des réveils nocturnes fréquents et prématurés, entraînant une fragmentation du sommeil, une instabilité respiratoire et une altération des muscles dilatateurs des voies aériennes supérieures. Cependant les études montrent que bien que les benzodiazépines fonctionnent augmentant le seuil d’éveil chez des patients sélectionnés, cet effet n’était pas systématiquement corrélé à l’amélioration de la sévérité de l’IAH (3).
Enfin, l’instabilité ventilatoire contribue à la pathogenèse du syndrome des apnées obstructives du sommeil chez 30 % des patients. Un individu ayant un contrôle ventilatoire instable présente des baisses périodiques de la commande respiratoire qui va diminuer l’activation des muscles dilatateurs des voies respiratoires supérieures conduisant à une répétition d’événements respiratoires. L’anhydrase carbonique (AC) est un régulateur important de la ventilation, avec 15 isoformes différentes exprimées dans les tissus humains (e.a. reins, érythrocytes, ainsi que l’endothélium et chimiorécepteurs centraux/périphériques). En induisant une acidose métabolique rénale et d’autres effets complexes, les inhibiteurs de AC (IAC) tels que l’acétazolamide augmentent la ventilation, ce qui atténue les fluctuations de CO2 et donc de la commande respiratoire. Les méta-analyses ont démontré par le passé une réduction de 38 % des IAH (-10 évènements par heure), mais avec une grande variabilité interindividuelle.
Plus récemment, une des isoformes, le sulthiame, s’est avéré être un stimulant respiratoire plus efficace avec des effets plus constants et prononcés. Dans un essai de phase II, tous les sujets (68) atteints d’OSA modéré/sévère ont connu des réductions prononcées de l’IAH d’une ampleur similaire après 4 semaines de traitement (-20 évènements/heures) (4). Notons qu’il est probable que cette bonne réponse du Sulthiame soit expliquée par les critères d’inclusion sélectionnant les patients atteints d’OSA modéré à sévère mais dont le BMI est inférieur à 35 kg/m2, pouvant expliquer une contribution plus grande de la commande ventilatoire dans la pathogenèse de l’OSA. Une étude multicentrique de 12 semaines randomisée en double aveugle est actuellement ouverte aux CuSL qui évaluera également les bénéfices en termes de somnolence et de fonction cardio-vasculaire.
Références
- Walter T McNicholas. Obstructive Sleep Apnoea: Focus on Pathophysiology Adv Exp Med Biol.2022;1384:31-42.
- https://clinicaltrials.gov/ct2/show/NCT03858751? cond=hypoglossal&draw=3&rank=20 ; https://beta.clinicaltrials.gov/study/NCT03858751
- Enrique Arredondo ,Monica DeLeon , Ishimwe Masozera , Ladan Panahi , George Udeani , Nhan Tran , et al. Overview of the Role of Pharmacological Management of Obstructive Sleep Apnea Medicina (Kaunas) 2022; 58(2): 225.
- Hedner J, Stenlöf K, Zou D, Hoff E, Hansen C, Kuhn K, et al. A Randomized Controlled Clinical Trial Exploring Safety and Tolerability of Sulthiame in Sleep Apnea. Am J Respir Crit Care Med. 2022;205(12):1461-1469.
L’immunothérapie dans le cancer du poumon : de plus en plus souvent, de plus en plus tôt
Thierry Pieters
Depuis 6 ans, l’immunothérapie par inhibition des points de contrôle PD-1/PD-L1 (ICI) a modifié complètement la prise en charge des cancers du poumon, principalement les carcinomes bronchiques non à petites cellules (CBNPC). Dans les stades IV A ou B, métastatiques donc, en seconde puis en première ligne, l’ICI a permis une amélioration fondamentale du pronostic vital.
En 2022, les résultats de survie à 5 ans de deux études de phase 3 avec le pembrolizumab, un anti-PD1, en première ligne (pendant 2années) en association avec la chimiothérapie (pour 4 cycles) (KEYNOTE-189 et KEYNOTE-407, respectivement pour les CBNPC non-squameux et squameux sans altération EGFR ou ALK) ont été communiqués (1,2). Après un suivi respectif de 64.6 mois et 56.9 mois, la survie médiane est de 22 mois vs 10.6 mois (HR 0.60) et de 17.2 vs 11.5 mois (HR 0.61) par rapport à la chimiothérapie seule et la survie à 5 ans de 19.4 vs 11.3% et 18.4 vs 9.7%. Cela signifie qu’un patient sur 5 est toujours en vie après 5 années. Cela est d’autant plus admirable que le cross-over vers l’ICI dans le groupe de patients qui étaient dans le bras chimiothérapie seule était de 57.3 et 50.9% respectivement, soulignant l’importance de donner l’immunothérapie dès la première ligne.
Rapidement, l’intérêt pour l’ICI dans les stades plus précoces du CBNPC a été étudié. C’est notamment le cas pour les stades III A ou B pour lesquels le pronostic vital à 5 ans était figé depuis des décennies à 20-25%. Dans l’étude PACIFIC, le durvalumab, un anti-PD-L1, en traitement adjuvant pendant 1 an après une chimio-radiothérapie concomitante (cCRT) a permis pour la première fois d’améliorer ce constat. La survie. La survie sans progression médiane était de 16.9 mois vs 5.6 mois dans le groupe placebo, la survie médiane de 47.5 vs 29.1 mois et la survie à 5ans est passée à 42.9% pour 33.4% dans le groupe placebo. En 2022, des données de vraie vie (real world) de 1399 patients recrutés dans 290 hôpitaux et 11 pays confirment ce changement de paradigme (3). La survie sans progression (PFS) est de 21.7 mois. La médiane de survie n’est pas encore atteinte. Cependant 71.2% des patients sont en vie à 2 ans. Donnée intéressante, 14.4% des patients ont reçu non pas une cCRT mais une chimio-radiothérapie séquentielle (sCRT). La cCRT n’est pas toujours réalisable pour des raisons propres au patient (fragilité) ou d’organisation des soins. La PFS médiane est numériquement supérieure avec la cCRT (23.7 vs 19.2 mois). Cependant, cette dernière valeur reste nettement supérieure à la PFS du groupe placebo dans l’étude PACIFIC. Une étude de ph3 est en cours pour confirmer l’intérêt de la sCRT par rapport à la cCRT (PACIFIC-5 ; NCT3706690). Il se confirme aussi que l’immunothérapie sera d’autant plus bénéfique qu’elle est débutée au plus près de la fin de la radiothérapie. Dès lors, pourquoi ne pas se poser la question de l’intérêt de l’immunothérapie dès la cCRT ? C’est ce que fait l’étude de ph2 KEYNOTE-799 (NCT03631784) (4). Les données sont encore immatures. La PFS tourne autour de 30 mois. E taux de survie à 2 ans est de 64-71% selon les cohortes.
Actuellement, l’intérêt de l’ICI est évalué dans les CBNPC de stade II ou IIIA résécables. Pourquoi ? Ils représentent près d’un quart des patients et leur pronostic vital n’est que d’environ 50-60% à 5 ans. Le standard de soin actuel qu’est la chimiothérapie adjuvante ou néo-adjuvante n’apporte qu’un bénéfice de survie de 5%. Dans la pratique courante, même si la chimiothérapie adjuvante présente des avantages oncologiques, la majorité des centres utilisent la chimiothérapie adjuvante. Ce paradigme pourrait changer avec l’immunothérapie. Outre sa meilleure tolérance par rapport à la chimiothérapie, elle peut restaurer la fonction anti-tumorale des cellules T, améliorer le taux de résection, donner des informations sur la réponse au traitement et traiter les micro-métastases, et interagir avec la radiothérapie qui peut amplifier l’expression de PD-L1 et ainsi amorcer la réponse à l’immunothérapie.
En traitement adjuvant, IMpower010 est l’étude la plus marquante. Un total de 1280 patients au stade IB à IIIA opérés en résection complète (R0) a été randomisé entre atézolizumab, un anti-PD-L1, pendant 1 an vs placebo après chimiothérapie adjuvante. Pour les stades II et IIIA, la survie médiane sans récidive (disease-free survival ; DFS) pour les expresseurs de PD-L1 ≥1% n’est pas atteinte (HR 0.64 ; p=0.00039). Cet avantage est encore plus impressionnant lorsque le taux de PD-L1 est ≥50% (HR 0.43), ce qui a amené l’EMA et l’INAMI à approuver ce traitement à partir de ce seuil. Par contre, il n’y a pas de bénéfice chez les patients qui ont une mutation EGFR ou ALK. Cette année, une analyse intérimaire de survie a été communiquée (5). Après un suivi médian de 45 mois, une tendance pour une meilleure survie est observée chez les patients exprimant PD-L1 ≥1% (HR {95%CI} : 0.71 {0.49-1.03}). À noter qu’une étude comparable avec pembrolizumab n’a pas montré de supériorité de survie parmi les patients exprimant PD-L1 ≥50%. Aussi dans notre groupe, nous préférons attendre des données de survie globale (overal survival ; OS) et plus matures avant de proposer l’ICI en traitement adjuvant. D’autres études tentent de mieux cibler la population chirurgicale à risque de récidive en étudiant l’ADN circulant (ctDNA) (NCT04367311, NCT 02273375, NCT 04642469). L’idée est d’offrir un traitement adjuvant aux seuls patients chez qui du matériel génique circulant est retrouvé après la chirurgie.
En traitement néoadjuvant, l’étude de ph3 Checkmate-816 compare 3 cycles de nivolumab, un anti-PD1, en association à de la chimiothérapie à base d’un sel de platine à la chimiothérapie seule avant chirurgie de 358 patients au stade IB ou II (35%) à IIIA (6). Avec le nivolumab, 24% des patients présente une réponse complète pour 2.2% dans le bras comparateur (odds ratio 13.94) et la survie sans événement (event-free survival ; EFS) est de 31.6 mois vs 20.8 mois (HR 0.63). A la première analyse intérimaire, l’HR pour le décès est de 0.57 et est non significatif. Petit bémol, seul 83.2% et 75.4% des patients qui reçoivent le traitement adjuvant sont finalement opérés. Un patient sur 4 ou 5 n’a donc pas été opéré alors que tous l’auraient été sans traitement néoadjuvant.
Le monde oncologique attend avec impatience dans ces deux à trois prochaines années la confirmation de l’intérêt de l’ICI dans les stades chirurgicaux ou localement avancés non opérés en association avec la CRT. Le mode d’administration de l’ICI est pour l’heure intraveineux. Des études sont en cours pour valider des injections sous-cutanées. D’autres tentent de combiner différents inhibiteurs de points de contrôle.
Références
- Garassino M et al. KEYNOTE-189 5-year update: First-line pembrolizumab (pembro) + pemetrexed (pem) and platinum vs placebo (pbo) + pem and platinum for metastatic nonsquamous NSCLC. Ann Oncol. 2022; 33 (suppl_7): S448-S554. 10.1016/annonc/annonc1064.
- Novello S et al. 5-year update from KEYNOTE-407: Pembrolizumab plus chemotherapy in squamous non-small cell lung cancer (NSCLC). Ann Oncol. 2022; 33 (suppl_7): S448-S554. 10.1016/annonc/annonc1064.
- Girard N et al. Treatment characteristics ans real-world progression-free survival in patients with unresectable stage III NSCLC who received durvalumab after chemoradiotherapy: findings from the PACIFIC-R study. J Thorac Oncol. https:// doi.org/10.11016/j.jtho.2022.10.003.
- Reck M et al. 2 year update from KEYNOTE-799 : Pembrolizumab plus concurrent chemoradiation therapy (cCRT) for unresectable, locally advanced, stage III NSCLC. Presented at ASCO 2022 ; Abstract 8508.
- Felip A et al. Impower: Updated Data of Phase III Trial of Adjuvant Atezolizumab vs BSC in Resected Stage IB-IIIA NSCLC After Adjuvant Chemotherapy. Presented at WCLC2022 ; Abstract PL03_09.
- Forde PM et al. Neoadjuvant nivolumab plus chemotherapy in resectable lung cancer. N Engl J Med. 2022 ; 386 : 1973-1985.
Allergologie : le cannabis, source d’une vague de maladies allergiques potentiellement sévères
Françoise Pirson
La population utilisant du cannabis à usage récréatif est en constante augmentation dans le monde (surtout pendant la phase de lock-down de la pandémie COVID 19). Dans la vague du « manger sain », les dérivés de chanvre et cannabis sont également proposés à la consommation (thé, graines, huile de chanvre ou cannabis et dérivés à base de cannabis). Or en Belgique, détenir ou cultiver du cannabis reste une infraction punissable. Il y a toutefois un certain laxisme dans les poursuites lorsque le détenteur est majeur et que la quantité détenue est <3 g, et s’il n’y a pas de circonstance aggravante ni trouble à l’ordre public. Les phytocannabinoÏdes CBG-type, CBD-type, THC-type ou CBC-type sont présents en quantité significative dans le cannabis. Le THC a des propriétés psycho-actives, le cannabidiol (CBD, qui contient <0.2 % THC) qui est recherché pour ses effets relaxants est autorisé à la vente en Europe.
L’exposition et la sensibilisation allergique au cannabis peuvent survenir par voie respiratoire, cutanée, et/ou digestive. Les symptômes vont de la rhino-conjonctivite, toux, asthme à l’anaphylaxie alimentaire potentiellement sévère. Plusieurs allergènes ont été identifiés (Tableau 1), dont Can s 3 (une protéine de transfert lipidique). Celui-ci est un allergène majeur en Europe, responsable de réactions allergiques parfois sévères (surtout en présence de cofacteurs tels que l’effort physique, prise d’alcool ou AINS). Les aliments incriminés sont variés (fruits, légumes, céréales, vins, bières…) et contiennent des nsLTP (réaction croisée).

Ces patients peuvent également réagir avec le tabac ou le latex. On comprend donc que le patient peut consulter pour des troubles respiratoires mais aussi allergiques alimentaires multiples et encore des anaphylaxies. Il sera pourtant très difficile de faire le lien avec la consommation (ou exposition passive surtout chez l’enfant) de cannabis car le patient ne dévoilera pas toujours facilement une consommation de substance illicite.
Selon les recommandations récentes (1), l’outil le plus performant du diagnostic reste l’anamnèse fouillée, suivie d’une confirmation par tests cutanés (non standardisés) avec des extraits de feuilles, tiges ou graines de cannabis. Un dosage des IgE spécifiques du chanvre (ImmunoCAP® Thermofischer Scientific, Uppsala, Sweden) et tout récemment rCan s 3 sont disponibles uniquement dans le cadre de la recherche. Il faut interpréter avec prudence les résultats, d’une part à cause de la sensibilisation croisée avec les pollens ou les nsLTP et, d’autre part, les Cross-reactive Carbohydrate Determinants (CCD) qui peuvent donner de faux positifs. Retenons que la recherche de sIgE rPru p 3 (nsLTP de la pêche) ne permet pas de détecter systématiquement la présence d’une sensibilisation à Can s 3 (faux négatifs). Les tests cellulaires d’activation des basophiles ne sont pas disponibles en pratique courante.
Le seul traitement de l’allergie clinique au cannabis est aujourd’hui l’éviction. Pour ceux qui ont eu des réactions sévères avec le cannabis ou des réactions croisées alimentaires sérieuses, la prescription d’une trousse d’urgence avec auto-injecteurs d’adrénaline est requise. Il n’y a pas de traitement curatif. Cette allergie est persistante voire définitive, ce qui est d’autant plus regrettable pour les enfants victimes d’une exposition passive.
Références
- Skypala I, Bernstein J, Klimek L et al. Cannabis-related allergies: an international overview and consensus recommendations. Allergy. 2022 ;77(7):2038-52
Kinésithérapie respiratoire : nouveautés en mouvement
Gregory Reychler
Plutôt que d’apporter de vraies nouveautés, 2022 aura plutôt été l’occasion d’enfoncer le clou ou des clous… L’exercice en tant que soin est sans conteste le sujet le plus « hot topic » en kinésithérapie. En effet, de nombreuses publications ont confirmé la faisabilité et l’intérêt des programmes d’exercice dans la prise en charge des patients respiratoires, initialement étudiés dans la BPCO. Si la BPCO a depuis longtemps contribué à placer la réadaptation pulmonaire sur la carte de la pneumologie, d’autres indications ont emboîté le pas. Le cancer pulmonaire en est le meilleur exemple, que ce soit en préopératoire avec une diminution du risque de complications post-opératoires (1), durant le traitement de chimio-radiothérapie (2), de manière concomitante à une thérapie adjuvante (3), ou pour récupérer de la chirurgie (4). L’entraînement des muscles inspiratoires en préopératoire commence également à prendre de plus en plus de place dans l’arsenal thérapeutique pour ces patients (5).
La COVID-19 est restée un sujet d’actualité en 2022 même si les vraies nouveautés sont rares et les données éparses. Il apparaît néanmoins que pour les patients qui gardent des séquelles à moyen voire long terme, autrement dit les patients souffrant d’affection post-COVID selon la définition de l’OMS, un programme d’exercices physiques s’avère une option intéressante avec des bénéfices sur la capacité fonctionnelle à l’exercice, la dyspnée et la fatigue, seul ou avec ajout d’un entraînement des muscles inspiratoires (6, 7) au vu la dysfonction diaphragmatique démontrée chez certains de ces patients (8). Le relâchement du diaphragme peut sans doute aider aussi certains de ces patients. La télé-réhabilitation qui a subi un énorme coup de boost « grâce » à cette pandémie, a indéniablement un rôle à jouer dans cette prise en charge physique (9, 10) et elle occupera probablement une place de plus en plus importante dans le futur pneumologique pour d’autres pathologies respiratoires. Pour finir avec la COVID-19, il y a eu un vrai questionnement en lien avec la dissémination des particules et le risque de contamination, que ce soit en lien avec la respiration spontanée (et donc le port du masque), la toux ou les techniques aérosolisantes (techniques de désencombrement, VNI, nébulisation). Les données sont encore insuffisantes pour conclure de manière exhaustive sur ce sujet mais il s’avère utile de prendre ceci en considération dans le futur.
Pour la kinésithérapie de désencombrement, un papier méthodologiquement intéressant a montré pour la première fois un bénéfice lié à l’utilisation régulière (3 mois) d’une technique à pression positive oscillante (Acapella®) chez des patients atteints de BPCO, alors que les dernières années, le désencombrement était un peu en perte de vitesse au niveau des recommandations, faute de preuves. Le bénéfice a été retrouvé au niveau de la toux, de la fatigue et de la qualité de vie mais aussi au niveau des exacerbations qui représentent un facteur de risque important de mortalité et un coût sociétal élevé (11).
Références
- Granger C, Cavalheri V. Preoperative exercise training for people with non-small cell lung cancer. Cochrane Database Syst Rev. 2022;9(9):CD012020.
- Borghetti P, Branz J, Volpi G, Pancera S, Buraschi R, Bianchi LNC, et al. Home-based pulmonary rehabilitation in patients undergoing (chemo)radiation therapy for unresectable lung cancer: a prospective explorative study. Radiol Med. 2022;127(12):1322-32.
- GilHerrero L, Courneya KS, McNeely ML, Castellanos M, Gonzalez Marquez AI, Pollan M, et al. Effects of a Clinical Exercise Program on Health-Related Fitness and Quality of Life in Spanish Cancer Patients Receiving Adjuvant Therapy. Integr Cancer Ther. 2022;21:15347354221141715.
- Su XE, Hong WP, He HF, Lin S, Wu SH, Liu F, et al. Recent advances in postoperative pulmonary rehabilitation of patients with non-small cell lung cancer (Review). Int J Oncol. 2022;61(6).
- Jones T, Fayle R. Letter to the editor referencing Effect of inspiratory muscle training associated or not to physical rehabilitation in preoperative anatomic pulmonary resection: a systemic review and meta-analysis. Supportive care in cancer : official journal of the Multinational Association of Supportive Care in Cancer. 2022;31(1):66.
- Del Corral T, Fabero-Garrido R, Plaza-Manzano G, Fernandez-de-Las-Penas C, Navarro-Santana M, Lopez-de-Uralde-Villanueva I. Home-based respiratory muscle training on quality of life and exercise tolerance in long-term post-COVID-19: Randomized controlled trial. Ann Phys Rehabil Med. 2022;66(1):101709.
- Jimeno-Almazan A, Buendia-Romero A, Martinez-Cava A, Franco-Lopez F, Sanchez-Alcaraz BJ, Courel-Ibanez J, et al. Effects of a concurrent training, respiratory muscle exercise, and self-management recommendations on recovery from post-COVID-19 conditions: the RECOVE trial. J Appl Physiol (1985). 2023;134(1):95-104.
- Boussuges A, Habert P, Chaumet G, Rouibah R, Delorme L, Menard A, et al. Diaphragm dysfunction after severe COVID-19: An ultrasound study. Front Med (Lausanne). 2022;9:949281.
- Vieira A, Pinto A, Garcia B, Eid RAC, Mol CG, Nawa RK. Telerehabilitation improves physical function and reduces dyspnoea in people with COVID-19 and post-COVID-19 conditions: a systematic review. J Physiother. 2022;68(2):90-8.
- Carpallo-Porcar B, Romo-Calvo L, Perez-Palomares S, Jimenez-Sanchez C, Herrero P, Brandin-de la Cruz N, et al. Efficacy of an asynchronous telerehabilitation program in post-COVID-19 patients: A protocol for a pilot randomized controlled trial. PLoS One. 2022;17(7):e0270766.
- Alghamdi SM, Alsulayyim AS, Alasmari AM, Philip KEJ, Buttery SC, Banya WAS, et al. Oscillatory positive expiratory pressure therapy in COPD (O-COPD): a randomised controlled trial. Thorax. 2023;78(2):136-43.
BPCO : les nouvelles recommandations internationales GOLD
Giuseppe Liistro
L’actualité sur la bronchopneumopathie chronique obstructive (BPCO) concerne principalement les nouvelles recommandations internationales de la Global Initiative for Chronic Obstructive Lung Disease ou GOLD (1). Cette organisation internationale vise à uniformiser le diagnostic et la prise en charge des patients BPCO en se basant sur des études cliniques de qualité. Ce sont des recommandations et non des directives, qui doivent donc être discutées localement pour leur éventuelle implémentation. Commençons par la nouvelle définition de la BPCO elle-même : la BPCO est une maladie pulmonaire hétérogène caractérisée par des symptômes respiratoires (dyspnée, toux, expectorations) dus à des anomalies des voies respiratoires (bronchite, bronchiolite) et ou des alvéoles (emphysème) qui entraînent une obstruction persistante, souvent progressive, du flux d’air. Cette définition repose toujours sur la spirométrie qui démontre un trouble ventilatoire obstructif peu ou pas réversible sous bronchodilatateurs.
La définition de l’exacerbation de la BPCO est également remaniée : une exacerbation de la BPCO est un événement caractérisé par une dyspnée et/ou une toux et expectorations qui s’aggravent pendant moins de 14 jours. Les exacerbations sont souvent associées à une augmentation de l’inflammation locale et systémique causée par les infections des voies respiratoires, la pollution ou d’autres agressions des poumons. Cette définition fait la différence entre une véritable exacerbation, limitée dans le temps, par rapport à une aggravation de la maladie.
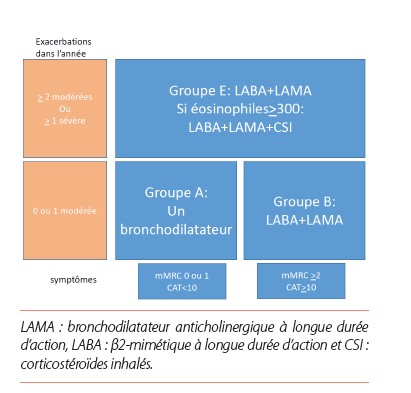
Une autre mise à jour importante concerne la prise en charge pharmacologique initiale de la BPCO, qui se base sur le niveau de la dyspnée, la fréquence des exacerbations et du taux des éosinophiles sanguins (voir schéma). Les symptômes sont évalués par l’échelle mMRC (https://www.inanutshell.ch/fr/calculateurs/echelle-de-dyspnee-mmrc/) et par un questionnaire disponible en ligne, le CAT score (https://www.mdcalc.com/calc/10161/copd-assessment-test-cat) . Le nombre d’exacerbations survenues au cours de l’année écoulée vont également entrer en ligne de compte si elles sont modérées ou sévères (nécessitant une hospitalisation).
Il faut remarquer qu’il n’y a plus de place pour les corticoïdes inhalés (CSI) seuls. Dans le groupe A, le choix est libre pour le bronchodilatateur mais pour les autres groupes, les auteurs privilégient l’association fixe, c’est-à-dire dans un même dispositif de 2 agents bronchodilatateurs à longue durée d’action. En cas d’exacerbations fréquentes ou sévères, le corticostéroïde inhalé est associé, aussi dans le même dispositif vu le gain en termes d’efficacité. Les CSI doivent cependant être évités si les éosinophiles sanguins sont inférieurs à 100 éléments/µL, en cas de pneumonies à répétition ou d’infection à mycobactéries. Enfin, pour les patients du groupe E chez qui les CSI doivent être évités et qui présentent encore des exacerbations malgré l’association fixe LABA+LAMA, l’introduction de l’azithromycine (250 à 500 mg par jour, 3 fois par semaine pendant un an) peut se justifier, en tenant compte bien sûr des effets secondaires et contre-indications.
Référence
- Guidelines GOLD : https://goldcopd.org.
Maladies rares : ERN-LUNG
Sophie Gohy, Antoine Froidure
Le service de pneumologie a intégré l’ERN-LUNG (European Reference Network for rare pulmonary diseases) en janvier 2022, avec une reconnaissance spécifique pour les pathologies interstitielles et la mucoviscidose.
Concernant la mucoviscidose, l’année 2022 a été marquée par le remboursement en Belgique de l’association de 3 modulateurs du CFTR, l’elexacaftor, le tezacaftor et l’ivacaftor (Kaftrio®), dès 12 ans. Actuellement, 85.3% des patients belges possèdent une copie de la mutation F508del, qui est une prérogative pour l’accès au traitement (registre belge de la mucoviscidose 2019). Les données en vie réelle publiées cette année, grâce au remboursement plus précoce dans d’autres pays, montrent des effets très encourageants pour les patients. A côté des améliorations de la qualité de vie, de BMI et de l’état respiratoire (gain de fonction, réduction des exacerbations et du nombre d’antibiothérapies), déjà démontrées dans les études de phase 3 et 4, les symptômes gastro-intestinaux régressent (1). L’imagerie des sinus par scanner montre une réduction du score de Lund-Mackay (2), reflétant l’amélioration de l’atteinte des voies respiratoires supérieures. Le nombre de transplantations pulmonaires pour mucoviscidose a drastiquement diminué en France en 2020 et le nombre de patients sur le chemin de la greffe (référés ou en liste active) passait de 21.6% à 2%, seulement après 3 mois l’introduction du Kaftrio®. L’usage d’oxygène au long cours, d’alimentation entérale et de ventilation non invasive était réduit de 50%, 50% et 30% respectivement (3). La lourdeur des traitements pourra sans doute diminuer notamment concernant l’arrêt des nébulisations qui fluidifient les expectorations (4) et de nouveaux défis apparaitront, liés entre autres à la prise de poids et au vieillissement de la population.
Dans le domaine des pneumopathies interstitielles diffuses (PID), il faut surtout retenir deux évènements à l’échelle nationale et internationale, respectivement : premièrement, le nintédanib (Ofev®), un antifibrosant utilisé comme traitement de la fibrose pulmonaire idiopathique, est désormais remboursé en Belgique pour toutes les PID fibrosantes et progressives, sur base du scanner thoracique, de la clinique et de la fonction respiratoire. Cela concerne une proportion importante de patients souffrant notamment de PID associée à une connectivité, de pneumopathie d’hypersensibilité ou de fibrose dite « inclassifiable » (5). Ce traitement ralentit le déclin de la fonction respiratoire et diminue le risque d’exacerbation. Deuxièmement, le concept récent de PID fibrosante et progressive a été intégré dans la toute nouvelle classification des PID, qui renseigne sur la proportion attendue de PID fibrosante et progressive pour chaque entité clinique (6). Soulignons également la publication des recommandations européennes sur les cryobiopsies transbronchiques comme alternative à la biopsie chirurgicale dans le diagnostic des PID : les cryobiopsies, bien que fournissant un moins bon rendement diagnostique (82% vs 95%) sont plus sûres et grevées de moins de complications (7). Cette technique innovante est réalisée en routine aux Cliniques Saint-Luc depuis 2015. Enfin, la société européenne de pneumologie vient de publier son avis sur le diagnostic et la prise en charge des fibroses pulmonaires familiales (8), avec des propositions sur les panels de gènes à tester, les investigations complémentaires et le conseil génétique.
Toutes ces avancées contribuent à améliorer la prise en charge de nos patients souffrant de maladies pulmonaires rares, au sein des centres de référence.
Références
- Schwarzenberg SJ, Vu PT, Skalland M, Hoffman LR, Pope C, Gelfond D, et al. Elexacaftor/tezacaftor/ivacaftor and gastrointestinal outcomes in cystic fibrosis: Report of promise-GI. J Cyst Fibros. 2022.
- Bec R, Reynaud-Gaubert M, Arnaud F, Naud R, Dufeu N, Di Bisceglie M, et al. Chest computed tomography improvement in patients with cystic fibrosis treated with elexacaftor-tezacaftor-ivacaftor: Early report. Eur J Radiol. 2022;154:110421.
- Burgel PR, Durieu I, Chiron R, Ramel S, Danner-Boucher I, Prevotat A, et al. Rapid Improvement after Starting Elexacaftor-Tezacaftor-Ivacaftor in Patients with Cystic Fibrosis and Advanced Pulmonary Disease. Am J Respir Crit Care Med. 2021;204(1):64-73.
- Mayer-Hamblett N, Ratjen F, Russell R, Donaldson SH, Riekert KA, Sawicki GS, et al. Discontinuation versus continuation of hypertonic saline or dornase alfa in modulator treated people with cystic fibrosis (SIMPLIFY): results from two parallel, multicentre, open-label, randomised, controlled, non-inferiority trials. Lancet Respir Med. 2022.
- Gagliardi M, Berg DV, Heylen CE, Koenig S, Hoton D, Tamirou F, et al. Real-life prevalence of progressive fibrosing interstitial lung diseases. Sci Rep. 2021;11(1):23988.
- Raghu G, Remy-Jardin M, Richeldi L, Thomson CC, Inoue Y, Johkoh T, et al. Idiopathic Pulmonary Fibrosis (an Update) and Progressive Pulmonary Fibrosis in Adults: An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med. 2022;205(9):e18-e47.
- Korevaar DA, Colella S, Fally M, Camuset J, Colby TV, Hagmeyer L, et al. European Respiratory Society guidelines on transbronchial lung cryobiopsy in the diagnosis of interstitial lung diseases. Eur Respir J. 2022;60(5).
- Borie R, Kannengiesser C, Antoniou K, Bonella F, Crestani B, Fabre A, et al. European Respiratory Society Statement on Familial Pulmonary Fibrosis. Eur Respir J. 2022.
Asthme : l’ère des traitements ciblés et des interactions ORL-pneumologie
Charles Pilette
La médecine personnalisée se décline actuellement dans la plupart des maladies respiratoires chroniques ; l’asthme fut une des premières à en bénéficier avec l’approbation EMA/FDA du traitement anti-IgE par omalizumab en 2003 (AMM en Belgique en 2006) pour le traitement de l’asthme allergique sévère, avant les biologiques anti-interleukine (IL)-5 (mépolizumab remboursé en Belgique depuis 2016, benralizumab depuis 2018, et reslizumab depuis 2019) pour le traitement de l’asthme sévère à éosinophiles. La première nouveauté de 2022 dans ce domaine fut l’extension des indications du mépolizumab (NUCALA?) et de l’omalizumab (XOLAIR?) à la rhino-sinusite chronique sévère avec polypes (CRSwNP) (1) ainsi que du mépolizumab à la granulomatose éosinophilique avec polyangéite (EGPA, ou syndrome de Churg-Strauss) et au syndrome hyperéosinophile (SHE). En l’absence d’étude comparative directe, la décision d’une approche anti-IgE ou anti-IL-5 pour traiter l’asthme sévère peut être aidée par les données en vie réelle et l’intégration des facteurs prédictifs de réponse (âge d’apparition, éosinophiles, comorbiditiés comme la CRSwNP) observés dans ces études (2), ainsi que de la réponse constatée au cas par cas. Ces traitements permettent de limiter voire annihiler le recours aux corticoïdes oraux pour traiter ces patients lors d’exacerbations voire en maintenance.
La seconde nouveauté fut le remboursement du vaccin allergénique d’ALK-Abello pour le traitement de l’asthme allergique aux acariens associé à une rhinite (Acarizax®) (3). Il s’agit d’une approche ciblée (sur l’allergie sous-jacente) de patients bien sélectionnés sur base d’une histoire clinique convaincante d’allergie aux acariens (confirmée par tests cutanés et/ou dosage des IgE spécifiques de Dermatophagoides pteronyssinus et D. farinae), avec asthme dont le contrôle reste partiel malgré un traitement de fond par corticoïde inhalé, associé à une rhinite allergique.
Ces évolutions thérapeutiques ont revigoré l’importance d’une collaboration efficace entre médecins ORL et pneumologues pour la prise en charge optimale des maladies respiratoires allergiques et/ou sévères (typiquement CRSwNP et asthme avec/sans hypersensibilité à l’aspirine, i.e. triade de Widal), au travers de discussions multidisciplinaires lors du diagnostic et du suivi de ces patients (4), pour lesquels l’arsenal thérapeutique Belge devrait bientôt s’enrichir du dupilumab (anticorps anti-IL-4Rα) et du tezepelumab (anticorps anti-TSLP) (5).
Références
- Bagnasco D, Canevari RF, Passalacqua G, Caminati M. The new indications for biologicals in type 2 diseases: perspectives. Curr Opin Allergy Clin Immunol. 2022 Dec 1;22(6):402-408.
- Pilette C, Canonica GW, Chaudhuri R, Chupp G, Lee FE, Lee JK, et al. REALITI-A Study: Real-World Oral Corticosteroid-Sparing Effect of Mepolizumab in Severe Asthma. J Allergy Clin Immunol Pract. 2022 Oct;10(10):2646-2656.
- Demoly P, Leroyer C, Serrano E, Le Maux A, Magnier G, Chartier A. The SQ HDM SLIT-Tablet is safe and well tolerated in patients with House Dust Mite allergic rhinitis with or without asthma: A “real-life” French study. Clin Transl Allergy. 2022 Mar;12(3):e12129.
- Torretta S, De Corso E, Nava N, Fraccaroli F, Ferrucci SM, Settimi S, et al. Proposal for a Structured Outpatient Clinic for Dupilumab Treatment in Chronic Rhinosinusitis with Nasal Polyps in the First Year of Treatment. J Pers Med. 2022 Oct 19;12(10):1734.
- Nopsopon T, Lassiter G, Chen ML, Alexander GC, Keet C, Hong H, Akenroye A. Comparative efficacy of tezepelumab to mepolizumab, benralizumab, and dupilumab in eosinophilic asthma: A Bayesian network meta-analysis. J Allergy Clin Immunol. 2022 Dec 17:S0091-6749(22)02498-8.
Affiliations
Service de pneumologie, Cliniques universitaires Saint-Luc, UCLouvain, B-1200 Bruxelles
Correspondance
Pr Charles Pilette
Cliniques universitaires Saint-Luc
Service de pneumologie
Avenue Hippocrate, 10
B-1200 Bruxelles
charles.pilette@uclouvain.be